へ 周期表ファミリー テーブルとギャザーの垂直方向のシーケンスです 化学元素 同様の化学的性質を持っています。 このような類似性は、同じ族にグループ化された元素に同量の価電子が存在するためです。 ファミリには、グループ 1 と 2 (13 ~ 18) の代表的な要素と、グループ 1 ~ 12 の遷移要素が含まれます。
こちらもお読みください:超ウラン元素 — 周期表でウランの後に続く人工の化学元素
この記事のトピックス
- 1 - 周期表ファミリーの概要
- 2 - 周期表ファミリーの構成
-
3 - 周期表ファミリーの命名法
- → 周期表の代表的な元素
- → 周期表遷移元素
- 4 - 周期表ファミリーの化学元素
-
5 - 周期表ファミリーの主な特徴
- → 第 1 族またはアルカリ金属族
- → 第 2 族またはアルカリ土類金属族
- → 3族から12族または遷移金属族
- → 13族またはホウ素族
- → 14 族または炭素族
- → 15 族または窒素族
- → 16 族または酸素族 (カルコゲン)
- → グループ 17 またはハロゲン族
- → グループ 18 または希ガス族
-
6 - 周期表と電子配布
- → 代表的な要素の電子配布
- → 遷移元素の電子配布
- 7 - 周期表のファミリーに関する演習を解く
周期表ファミリーの概要
ファミリは、 周期表.
グループとしても知られる、周期表のファミリーには 1 から 18 までの番号が付けられます。
同じ族の化学元素は同様の化学的性質を持っています。
一連の元素の類似性は、価電子の数が等しいことで説明されます。
代表的な元素はグループ 1、2、13、14、15、16、17、18 に分類されます。 これらの各ファミリーには特定の名前が付いています。
遷移元素は、グループ 3、4、5、6、7、8、9、10、11、および 12 に分割される 1 つのファミリーを形成します。
今はやめないでください... 宣伝の後にはさらに続きがあります ;)
周期表ファミリーの構成
周期表の族 表の垂直方向の順序です、つまり列です。 周期表のグループ、ファミリーとしても知られています。 左から右に 1 から 18 までの番号が付けられます。
同じ列を占める化学元素は、同じファミリーに属するとみなされます。、同じ数の化学的特性が類似しているためです。 電子 で 原子価殻. たとえば、ファミリー 18 のすべての化学元素は価電子殻 (完全殻) に 8 個の電子を持ち、原子価殻に関与することはほとんどありません。 化学結合.
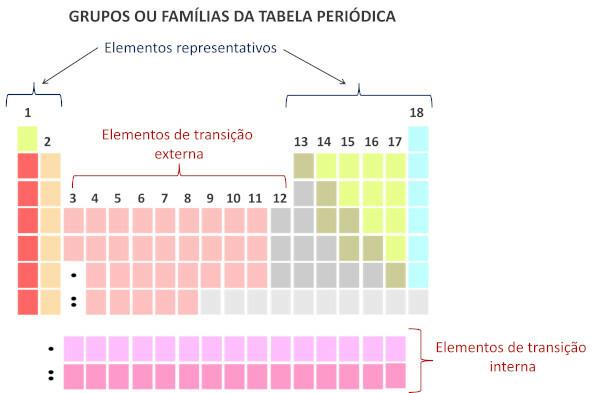
現代のシステムによれば、 国際純粋応用化学連合 (Iupac) では、各グループまたはファミリーは、周期表の左から右に向かって 1 から 18 までの番号で識別されます。
古い IUPAC システムでは英数字システムが採用されており、文字 A と B がそれぞれ代表要素と遷移要素を表すことを強調することが重要です。 現在、このタイプの命名法は使用されなくなりました。
周期表ファミリーの命名法
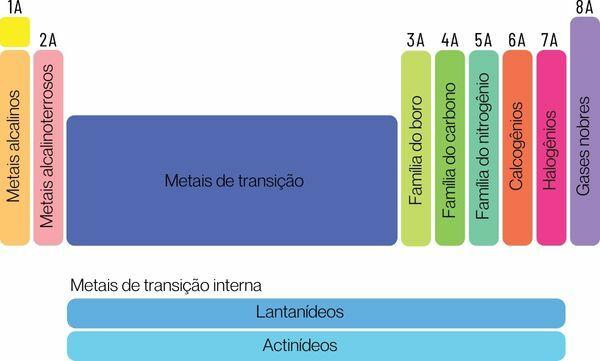
化学元素は、代表元素と遷移元素という 2 つの大きなグループに分類できます。
→ 周期表の代表的な元素
代表的な元素はグループ 1、2、13、14、15、16、17、18 に分類されます。 これらのグループにはそれぞれ特定の名前があり、それによってそれを知ることもできます。 見て:
グループ 1: の家族 金属 アルカリ性。
グループ 2: の家族 アルカリ土類金属.
グループ 13: ホウ素または土金属族。
グループ 14: カーボンファミリー。
グループ 15: 窒素またはプニコゲンファミリー。
グループ 16: 酸素またはカルコゲン族。
グループ 17: の家族 ハロゲン.
グループ18: の家族 希ガス.
→ 周期表遷移元素
あなた 遷移要素グループ 3、4、5、6、7、8、9、10、11、12 に分かれて単一の家族を形成します。. ランタニドおよびアクチニド系列も遷移元素の一部です。
移行要素 すべて金属であり、同様の化学的性質を持っています、価電子殻に異なる電子を持っていても、単一の大きな遷移金属族を形成することになります。
周期表ファミリーの化学元素
各ファミリーまたはグループは、一連の化学元素で構成されています。 各ファミリーを構成する化学元素の説明を参照してください。
グループ 1:リチウム, ナトリウム, カリウム, ルビジウム, セシウム, フランシウム.
グループ 2:ベリリウム, マグネシウム, カルシウム, ストロンチウム, バリウム, 無線.
グループ 3:スカンジウム, イットリウム、ランタニド系およびアクチニド系。
グループ 4: チタン, ジルコニア○, ハフニウム それは ラザフォージウム.
グループ 5:バナジウム, ニオブ, タンタル それは ドブニウム.
グループ6:クロム, モリブデン, タングステン それは シーボーギウム.
グループ 7:マンガン, テクネチウム, レニウム それは ボリオ.
グループ 8: 鉄, ルテニウム, オスミウム それは ハシウム.
グループ9:コバルト、ロジウム、イリジウム、マイトネリウム。
グループ 10:ニッケル、パラジウム、 白金 そしてダルムシュタディオ。
グループ 11: 銅, 銀, 金 そしてレントゲニウム。
グループ 12:亜鉛, カドミウム, 水星 そしてコペルニクス。
グループ 13: ボロン, アルミニウム, ガリウム、インジウム、タリウム。
グループ 14: 炭素, ケイ素、ゲルマニウム、 錫, 鉛 そしてフレロビウム。
グループ 15:窒素, 蛍光体, 砒素, アンチモン それは ビスマス.
グループ 16:空気, 硫黄, セレン, テルル、ポロニウム、リバモリウム。
グループ 17: フッ素, 塩素、臭素、 ヨウ素 そしてアスタチン。
グループ18:ヘリウム, ネオン, アルゴン, クリプトン, キセノン それは ラドン.
重要: 化学元素 水素 は、グループ 1 の隣に位置しているにもかかわらず、同様の化学的性質を共有していないため、アルカリ金属族の一部ではないため、特別なケースです。
さらに詳しく: 周期表の放射性元素は何ですか?
周期表のファミリーの主な特徴
それらは金属固体であり、光沢があり滑らかです。
熱伝導率が高く、 電気伝導率.
もつ 温度 比較的低融点。
彼らは次のものに対して非常に反応性が高い 水.
一価カチオン(電荷+1)を形成する傾向。
それらは金属固体であり、光沢があり、アルカリ金属に比べて硬い。
酸化しやすいのです。
高い熱伝導率と高い電気伝導率を持っています。
アルカリ金属と比較してわずかに高い融解温度を持っています。
これらは水と反応します。
二価カチオン(電荷+2)を形成する傾向。
彼らは周期表上で最大のファミリーです。
硬くて光沢のある金属固体。
高い熱伝導率と高い電気伝導率を持っています。
密集。
融解温度が高い。
異なるものを提示する可能性があります 酸化状態.
→ 13族またはホウ素族
それらは金属の特性と金属の特性の中間の特性を持っています。 金属ではありません.
それらは周囲条件下では固体です。
三価カチオン(電荷+3)を形成する傾向。
→ 14 族または炭素族
金属と非金属の中間的な性質を持っています。
それらは周囲条件下では固体です。
4つの結合を形成する傾向。
それらは周囲条件下では固体です。
炭素とシリコンは鎖結合を形成できます。
→ 15 族または窒素族
金属と非金属の中間的な性質を持っています。
気体である窒素を除く、周囲条件下の固体。
窒素とリンは生物にとって基本的なものです。
ヒ素は非常に有毒です。
→ 16 族または酸素族 (カルコゲン)
それらは異なる特性を持っており、族が下に進むにつれて非金属元素から金属元素に変化します。
気体である酸素を除く、周囲条件下の固体。
二価の陰イオン (電荷 -2) を形成する傾向があります。
→ グループ 17 またはハロゲン族
それらは非金属です。
かなり反応的です。
熱伝導体と電気伝導体が不良です。
周囲条件下では、フッ素と塩素は次のように存在します。 ガス, 臭素は液体、ヨウ素は固体です。
一価の陰イオン (電荷 -1) を形成する傾向があります。
→ グループ 18 または希ガス族
それらは非金属です。
反応性が非常に低いため、不活性ガスと呼ぶことができます。
それらは気体の形で存在します。
形成する傾向がない イオン.
周期表と電子配布
同じ科またはグループに属する化学元素は、次の理由から同様の化学的性質を持っています。 価電子殻内の電子の数が等しい。
価電子殻内の電子の数は、陽イオンまたは陽イオンの形成傾向を決定するため、重要です。 陰イオン、形成される化学結合の種類、化学反応に関与するエネルギーなど 特徴。 価電子の数を求めるには、 を知る必要がある 原子番号 要素を選択して実行します。 電子配布.
→ 代表的な要素の電子配布
代表的な要素 最もエネルギーの高い電子はサブレベルにあります s それは P 電子層(n)の。 次の表は、代表的な要素の各ファミリーに関連付けられた電子構成をまとめたものです。 用語 n は 1 から 7 まで変化し、価電子が占めるエネルギー準位を表します。これは、その元素が存在する周期表の周期 (水平線) に相当します。
代表的な要素の電子配布 | ||
家族やグループ |
電子配布 |
例 |
1 |
私たち1 |
Li (Z=3): 1s2 2秒1 |
2 |
私たち2 |
Be (Z=4): 1s2 2秒2 |
13 |
私たち2 NP1 |
B(Z=5):1秒2 2秒22P1 |
14 |
私たち2 NP2 |
C (Z=6): 1s2 2秒22P2 |
15 |
私たち2 NP3 |
N (Z=7): 1s2 2秒22P3 |
16 |
私たち2 NP4 |
O (Z=8): 1s2 2秒22P4 |
17 |
私たち2 NP5 |
F(Z=9):1秒2 2秒22P5 |
18 |
私たち2 NP6 |
Ne (Z=10): 1s2 2秒22P6 |
→ 遷移元素の電子配布
遷移要素はグループ 3 と 12 に分散されており、 サブレベルがある d それは f 価電子によって占められている:
外部遷移要素: 価電子をサブレベルに保つ d、電子配置を次と等しく保ちます。 私たち2 (n-1)d(1~8). たとえば、元素ニッケル (Z = 28) はグループ 10 に属し、その構成は 1s です。2 2秒2 2P6 3秒2 3p6 4秒2 3D8.
内部遷移要素: それらはグループ 3 の一部ですが、周期表の「内部」にあり、その下の周期 6 (ランタニド) と 7 (アクチニド) に拡張されています。 これらの元素は価電子がサブシェルを占めています f および一般的な電子構成 私たち2 (n-2)f(1~13). たとえば、元素ランタン (Z = 57) はランタニド系列の最初の元素であり、その電子配置は 1s です。2 2秒2 2P6 3秒2 3p6 4秒2 3D10 4P6 5秒2 4D10 5p6 6秒2 4f1.
以下のことも知ってください:周期表の起源は何ですか?
周期表のファミリーに関する演習を解決しました
質問1
(UFC — 適応) 元素の現代の周期的分類に関して、正しい記述にチェックを入れてください。
A) 周期表では、ファミリーまたはグループは水平線に対応します。
B) ファミリー内の元素は非常に異なる化学的性質を持っています。
C) 族では、通常、要素は最後のシェルに同じ数の電子を持ちます。
D) ある期間では、元素は同様の化学的性質を持ちます。
E) 代表的な要素はグループ 3 ~ 12 に分類されます。
解決:
オルタナティブC
項目 A は不正確です。族またはグループは周期表の列 (垂直線) です。
項目 B と D が不正解: ファミリーでは、元素は同様の化学的特性を持っています。 周期では、元素は価電子が占める同じ電子殻を持ちます。
項目 C 正解: 族では、要素は最後の殻に同じ数の電子を持っています。
項目 E 不正解: 代表的な元素はグループ 1、2、13、14、15、16、17、18 です。 遷移要素はグループ 3 ~ 12 に分散されています。
質問2
(EAM) 元素 A、B、および C は、価電子殻に次の電子配置を持っています。
答え: 3秒1
B: 4秒2 4P4
C: 3秒2
この情報に基づいて、正しいオプションを選択してください。
A) 元素 A はアルカリ金属です。
B) 元素 B はハロゲンです。
C) 元素 C はカルコゲンです。
D) 元素 A と B は周期表の第 3 周期に属します。
E) 3 つの元素は周期表の同じグループに属します。
解決:
代替案A
項目 A 正解: 元素 A は価電子を 1 つだけ含む電子分布を持っているため、周期表のグループ 1 に属します。
間違った項目 B: 元素 B は 4s 電子配置を持っています2 4P4、最後の殻には 6 つの電子があり、この元素が 16 族 (カルコゲン) に属していることを示しています。
誤った項目 C: 元素 C は、最後の殻に 2 つの電子を持つ電子配置を持っているため、表のグループ 2 の元素です。
誤項目 D: 要素 A は第 3 周期 (n = 3) に属し、要素 B は第 4 周期 (n = 4) に属します。
間違った項目 E: 3 つの元素は最後の殻に含まれる電子の量が異なるため、同じ族に属することはできません。
アナ・ルイザ・ロレンゼン・リマ
化学の先生
ここをクリックして、価電子層とは何かを学び、それを識別する方法を見つけてください。
電子配布がどのように行われるかを理解し、例を確認してください。
周期表の第 3 族の第 6 周期と第 7 周期を占める内部遷移元素 (アクチニドとランタニド) の特殊性について学びます。
既存の化学元素を知り、それらが何であるか、そしてそれらをどのように表現するかを理解します。
希ガスは、自然界に分離された形で存在する唯一の元素です。 詳細については、この記事をご覧ください。
ハロゲン、その性質、特性、日常生活における主な用途について学びます。
アルカリ土類金属について詳しく学び、特徴、性質、用途を学びましょう。
原子番号とは何かを理解し、そこからわかる原子の特徴を学びます。
ここで周期表が何であるかを確認し、それを構成するすべての化学元素を知るための対話型モデルを参照してください。