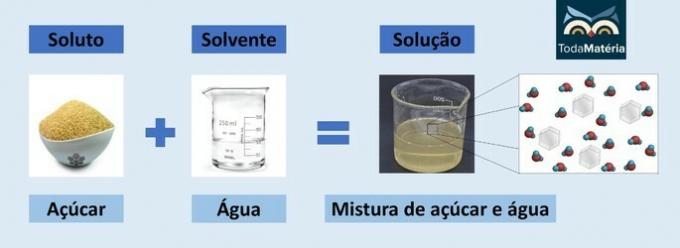
で 共有結合、 とも呼ばれている 分子結合または単極結合、の原子間で発生するものです 電気陰性要素、つまり、電子を受け取る傾向があり、 価電子殻からの電子を共有します。
共有結合は、次の要素間で発生する可能性があります。 水素、非金属および半金属。 金属はこのタイプの結合には決して関与しません。
共有結合の簡単な例を考えてみましょう:水素ガス形成結合(H2):
H + H→H2
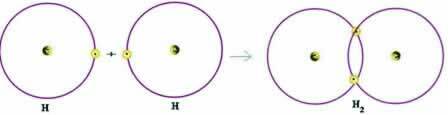
オクテット則に従って、両方の原子が価電子を受け取り、このようにして安定性を維持する必要があることに注意してください。 したがって、彼らは電子を共有し、このようにして、両方とも2つの電子を持ち、完全なKシェルを持ち、希ガスヘリウムの構成を取得しました。
この電子の共有は、このタイプの結合を、電子移動が行われるイオン結合と区別するものです。
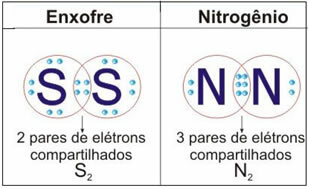
この場合のさらに2つの例については、次の図を参照してください。
今やめないで... 広告の後にもっとあります;)
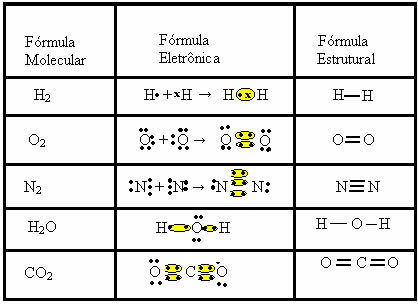
このタイプの結合では、分子の形成があり、それぞれの分子で表すことができます 分子式つまり、分子内に各元素の原子がいくつあるかを示す最も単純な表現です。 分子式のいくつかの例は次のとおりです。H2、S2、O2、 番号2、H2O、CO2、など。
共有結合は、他の2つの式で表すことができます。
- 電子式またはルイス式:この式には、各原子の価電子と電子対の形成も含まれています。 これらの電子は記号で表されます . またはx;
- フラット構造式またはクーパー構造式:要素のリンクを示します。各共有ペアはダッシュに対応します。 ダッシュの場合は、単一リンクと呼びます。 2つある場合は、二重結合。 ダッシュが3つある場合は、三重結合。
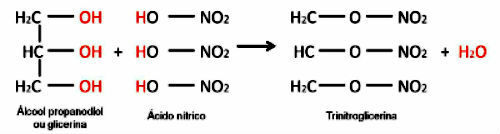
次の3つの化学式で表される共有結合の他の例に注意してください。
ジェニファー・フォガサ
化学を卒業
学校や学業でこのテキストを参照しますか? 見てください:
FOGAÇA、ジェニファー・ロシャ・バルガス。 "共有結合"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/ligacoes-covalentes.htm. 2021年6月27日にアクセス。