実験は、化学で研究された概念の知識を学び、テストするための実用的な方法です。
これらの化学実験を利用して、自宅で(大人の監督下で)行うか、教室で教師と一緒に作業して、研究を補完することができます。
初体験-色を解き明かす
関係する概念:クロマトグラフィーと混合物の分離
材料
- さまざまな色のペン(マークされたマーカー)
- アルコール
- コーヒーフィルターペーパー
- カップ(実験のモニタリングを容易にするためのガラス)
作り方
- はさみを使用し、ろ紙のストリップをカットします。 使用するペンごとに、長方形を作成します。
- 次に、ベースから約2 cmの距離で、選択したカラーペンで円を描き、内側をすべてペイントします。
- 描かれたビー玉から最も遠い紙の端をサポートに接着します。 これには、テープを使用して鉛筆に貼り付けることができます。
- ペンマークの近くの紙の端にちょうど触れるはずなので、あまり多くないで、カップにアルコールを追加します。
- 紙が垂直になるようにカップに入れます。 それを支える鉛筆は端に置いておく必要があります。
- アルコールがろ紙を通って上昇するまで10〜15分待ちます。 その後、紙を取り除き、乾かします。
結果
アルコールがペンマークを通過するとき、それは色成分と相互作用し、紙全体にそれらを駆動します。 したがって、異なる顔料はアルコールとの接触によって分離されます。
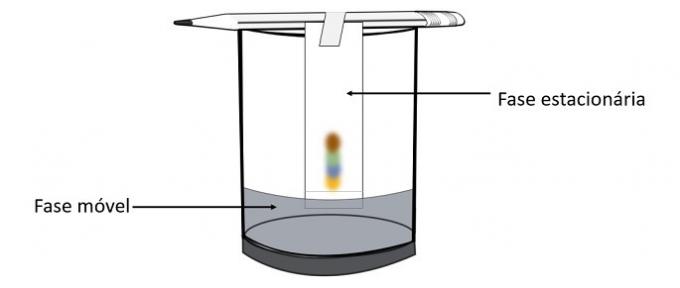
この実験を通して、ペンの色を作成するためにどの色が混合されたかを知ることができます。
説明
クロマトグラフィーは、混合物を分離するためのプロセスの一種です。 ろ紙は固定相であり、アルコールは混合物が固定相を通過するときに混合物の成分を引きずる移動相です。 このプロセスでは、アルコールとの相互作用が大きいほど、溶媒の通過に伴って顔料が速く移動します。
材料の構成要素は、異なる特性を持っているため、移動相と相互作用します さまざまな方法で、これは固定相のさまざまなドラッグ時間によって認識できます。
詳細については クロマトグラフィー.
2回目の体験-食品保存
関連する概念:有機化合物と化学反応
材料
- リンゴ、バナナまたはナシ
- レモンまたはオレンジジュース
- ビタミンC錠
作り方
- 3つの果物から1つを選び、3つの等しい部分に切ります。
- 最初の部分は他の部分との比較として役立ちます。 したがって、何も追加せず、空気にさらしたままにしてください。
- 片方にレモンかオレンジの中身を垂らします。 果物の内側全体がジュースで覆われるように広げます。
- 最後の部分では、ビタミンCを広げます。これは、果肉全体に砕いた錠剤にすることができます。
- 何が起こるかを見て、結果を比較します。
結果
空気にさらされた果物の果肉はすぐに暗くなるはずです。 レモンまたはオレンジジュースとアスコルビン酸と呼ばれる化学物質であるビタミンCは、果物の褐色化を遅らせるはずです。

説明
果物を切ると、その細胞が損傷を受け、ポリフェノールオキシダーゼなどの酵素が放出されます。 空気との接触は、食品に存在するフェノール化合物を酸化し、酵素による褐変を引き起こします。
アスコルビン酸などの防腐剤は、フェノール化合物の代わりに優先的に酸化されるため、酸素の作用を防ぐために使用されます。 ビタミンCタブレットに加えて、アスコルビン酸は、実験で示唆されている柑橘類、レモン、オレンジなどの天然資源にも存在します。
詳細については 酸化.
3番目の経験–誰がより速くフリーズしますか?
関連する概念:束一性と凝固点降下
材料
- 2本のチューブ(パーティーの記念品に使用)
- ガラスのボウル
- 食卓塩
- ろ過水
- 氷
- 温度計
作り方
- 両方のチューブに同量のろ過水を追加します。 たとえば、各チューブに5mL。
- チューブの1つに食卓塩を追加し、どちらが塩辛いのかを区別するために識別テープを貼ります。
- ガラス容器に砕いた氷を入れ、塩を加えます。
- 2本のチューブを同時に氷の中に置き、何が起こるかを観察します。
- 各状況の凍結温度を記録します。
結果
水に溶質を加えると、凍結温度が下がります。 したがって、同じ条件にさらされた場合、普通の水は塩と水溶液よりもはるかに速く凍結する傾向があります。
説明
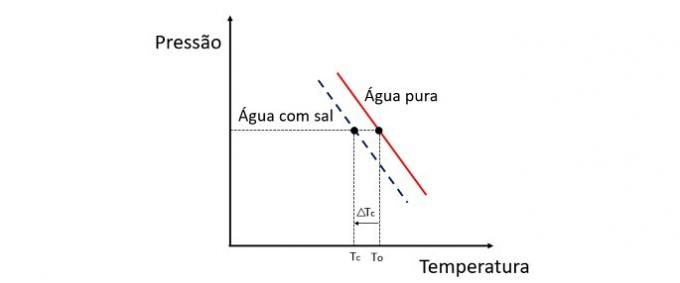
凝固点降下は、さまざまな量の溶質が溶媒に溶解したときの溶媒の温度の変化を研究する束一性です。
水の凍結温度の低下は、不揮発性の溶質によって引き起こされ、この現象には多くの実用的な用途があります。 したがって、溶液中の溶質の濃度が高いほど、凝固点降下効果に影響します。
たとえば、水が0°Cで凍結し、それに塩を加えると、相変化温度は負になります。つまり、はるかに低くなります。
そのため、気温が0℃以下の場所では海水が凍りません。 水に溶けた塩は、氷点下の温度をさらに下げる傾向があります。 雪が降る場所では、道路に塩をかけて氷を溶かし、事故を防ぐことも一般的です。
詳細については 束一性.
4番目の実験-過酸化水素の分解
関係する概念:化学反応と触媒
材料
- 生のジャガイモの半分と調理済みの半分
- 生のレバーと別の調理済みのピース
- 過酸化水素
- 2皿
作り方
- 各皿に食べ物、ジャガイモを一緒に、そして肝臓を一緒に追加します。
- 4つの材料のそれぞれに、過酸化水素を3滴加えます。
- 何が起こるかを見て、結果を比較します。
結果
過酸化水素水である過酸化水素は、生の食品と接触すると、ほぼ瞬時に発泡し始めます。
この実験は、過酸化水素の入った容器に食品を加えて反応をより目立たせることによっても行うことができます。
説明
生の食品と接触したときに過酸化水素によって提示される発泡性は、 過酸化水素の分解とガスの放出である化学反応の発生 酸素。
過酸化水素の分解は、動物や植物の細胞に存在するペルオキシソームオルガネラに見られるカタラーゼ酵素の作用によって起こります。
過酸化水素の分解は、太陽光の存在下で自発的に発生しますが、反応が非常に遅いことに注意することが重要です。 ただし、カタラーゼは触媒として機能し、化学反応の速度を上げます。
過酸化水素は細胞にとって有毒物質になる可能性があります。 したがって、カタラーゼは化合物を分解し、体に害を及ぼさない2つの物質である水と酸素を生成します。
食品が調理されると、その成分が変化します。 料理によって引き起こされる修飾はまた、タンパク質を変性させることによってカタラーゼの作用を損ないます。
食べ物で見られるのと同じ行動は、過酸化水素を傷口に置いたときに起こることです。 カタラーゼが作用し、酸素の放出からなる泡の形成があります。
詳細については 化学反応.
書誌参照
聖人、W。 L。 P。; MOL、G。 S。 (調整)。 市民化学。 1. ed。 サンパウロ:新世代、2011年。 v。 1, 2, 3.
BRAZILIAN CHEMICAL SOCIETY(org。)2010。 お近くの化学:幼稚園から高校までの教室での低コストの実験。 1. ed。 サンパウロ。