IL distillazione è un metodo per separare miscele omogenee, cioè quando i componenti sono in un'unica fase.
Esistono due tipi di distillazione. La distillazione semplice viene utilizzata nella separazione solido-liquido e nella distillazione frazionata in una miscela di liquidi miscibili tra loro.
Per poter isolare un particolare componente di una miscela è necessario modificare una variabile. Nel caso della distillazione, la separazione avviene modificando la temperatura in modo che il componente di interesse cambi il suo stato fisico.
La proprietà delle sostanze utilizzate in questo processo è la punto di ebollizione, cioè la temperatura alla quale avviene il passaggio da liquido a gas.
processo di distillazione
Il processo di distillazione consiste nel fornire calore ad una miscela fino al raggiungimento del punto di ebollizione del componente di interesse e questo passa allo stato gassoso, separandosi dagli altri.
Successivamente, il gas passa attraverso una colonna di raffreddamento, dove viene sottratto calore alla sostanza fino a raggiungere il punto di fusione e, quindi, tornare allo stato liquido. Questo materiale è diretto a un altro contenitore.
distillazione semplice
Per separare una miscela omogenea da solido disciolto in liquido viene utilizzata la distillazione semplice.
Nell'immagine sottostante possiamo vedere l'attrezzatura di base per il processo di separazione.

Sono loro:
- pallone da distillazione (1), che contiene la miscela;
- Coperta riscaldante (2), che fornisce calore alla miscela;
- Termometro (3), per monitorare la variazione di temperatura;
- Condensatore (4), per raffreddare il componente evaporato e
- Bicchiere (5), per raccogliere il componente separato allo stato liquido.
Questo processo può essere utilizzato, ad esempio, per separare il cloruro di sodio (NaCl), noto come sale da cucina, e l'acqua. Il sale ha un punto di ebollizione di 1465 °C e si scioglie in acqua per formare una miscela omogenea.
Poiché l'acqua ha un punto di ebollizione di 100 ºC, si trasforma facilmente in uno stato gassoso e si separa dalla miscela, mentre il sale cristallizza e rimane allo stato solido nel contenitore.
Il vapore acqueo esce dalla parte superiore del pallone di distillazione e passa attraverso un condensatore. L'acqua fredda o fredda circola sulle pareti di questa apparecchiatura. Lo scambio di calore tra i fluidi fa sì che il componente separato della miscela perda calore e ritorni allo stato liquido per essere raccolto in un altro contenitore. Questo liquido è chiamato distillato.
distillazione frazionata
Per separare una miscela omogenea da liquidi miscibili tra loro e con una grande differenza tra le temperature di ebollizione, viene utilizzata la distillazione frazionata.
Questo metodo è frazionato perché i componenti sono separati dalla miscela in ordine crescente del punto di ebollizione, cioè partendo dalla più bassa fino a quella che richiede la temperatura più alta per cambiare fase.
Nell'immagine qui sotto, c'è l'attrezzatura utilizzata per eseguire il metodo.
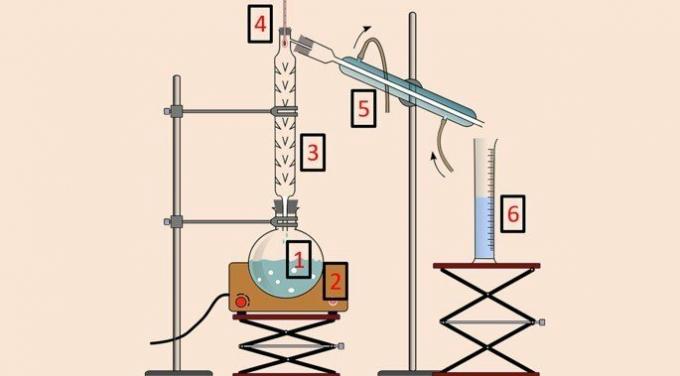
Come nella distillazione semplice, vengono utilizzati il pallone di distillazione (1), la coperta riscaldante (2), il termometro (4), il condensatore (5) e il bicchiere (6). in ogni caso, il colonna di distillazione o frazionamento (3) è l'apparecchiatura che consente la separazione in base alla temperatura.
La colonna di distillazione presenta al suo interno una serie di ostacoli per evitare che tutti i componenti della miscela si volatilizzino contemporaneamente.
Questo processo è ampiamente utilizzato per separare frazioni di petrolio, che è una miscela di idrocarburi. Alcuni dei componenti del petrolio e dei rispettivi punti di ebollizione (PE) sono: butano (PE 20 ºC), benzina (PE 150 ºC) e cherosene (PE 300 ºC).
Attraverso la distillazione frazionata, il butano è il primo componente separato, in quanto ha il punto di ebollizione più basso, poi la benzina, con punto di ebollizione intermedio, e infine il cherosene.
Applicazioni di distillazione
La distillazione è ampiamente utilizzata nelle industrie, poiché molte miscele subiscono questo processo. Gli alcolici come whisky, brandy e vodka sono realizzati con il metodo.
L'industria petrolchimica utilizza la distillazione frazionata per raffinare il petrolio. Le torri di distillazione sono grandi strutture realizzate per separare le frazioni di questo combustibile fossile.

Esercizi di distillazione
domanda 1
La distillazione è un metodo di separazione basato sulle proprietà.
la chimica
b) Fisica
c) Biologico
d) Generale della questione
Alternativa: b) Fisica.
Il punto di ebollizione è una proprietà fisica specifica della materia, in quanto inerente a una data sostanza. È la temperatura alla quale un materiale passa dallo stato liquido allo stato gassoso, cioè subisce l'evaporazione.
Domanda 2
Questi sono esempi di miscele separate per distillazione, TRANNE
a) acqua + acetone
b) salamoia
c) acqua + olio
d) acqua di mare
Alternativa corretta: c) acqua + olio.
Acqua e olio sono sostanze immiscibili. In questo caso si utilizza il metodo della decantazione per separare i componenti della miscela. Questo metodo si basa sulla differenza di densità.
La salamoia (acqua + sale) e l'acqua di mare, anch'essa con sali disciolti, vengono separate per semplice distillazione. Per acqua e acetone si usa la distillazione frazionata.
Domanda 3
(UFRGS) Un sistema bifasico eterogeneo è formato da tre diversi liquidi A, B e C. È risaputo che:
A e B sono miscibili tra loro;
C è immiscibile con A e con B;
A è più volatile di B.
Sulla base di queste informazioni, i metodi più adatti per separare i tre liquidi sono:
a) centrifugazione e decantazione.
b) decantazione e fusione frazionata.
c) filtrazione e centrifugazione.
d) filtrazione e distillazione frazionata.
e) decantazione e distillazione frazionata.
Alternativa corretta: e) decantazione e distillazione frazionata.
Il sistema eterogeneo della domanda ha due fasi:
Fase 1: liquidi A e B miscibili tra loro
Fase 2: liquido C, immiscibile con gli altri componenti
Pertanto, a causa della differenza di densità, la fase 1 viene separata dalla fase 2 mediante il metodo della decantazione. A causa della differenza della temperatura di ebollizione, poiché A è più volatile di B, cioè tende a passare facilmente allo stato gassoso, si utilizza la distillazione frazionata.
Acquisisci maggiore conoscenza con i contenuti:
- Distillazione semplice e frazionata
- Separazione di miscele
- Esercizi sulla separazione delle miscele