Come si legge nel testo"Equazione chimica”, per rappresentare le reazioni chimiche e comprendere il modo in cui vengono elaborate, i loro aspetti quantitativi e qualitativi, si è convenuto di utilizzare equazioni chimiche. Le equazioni chimiche contengono simboli e numeri che mostrano quali sostanze sono presenti e le proporzioni appropriate in cui reagiscono.
Attraverso l'interpretazione di queste equazioni, è possibile trovare dati importanti che ci aiutano a eseguire calcoli stechiometrici. Tuttavia, il primo passo dice che l'equazione deve essere bilanciata, cioè deve avere il numero totale di atomi dei reagenti uguale a quello dei prodotti. Puoi capire come eseguire questo bilanciamento attraverso il testo "Bilanciamento dell'equazione”.
Prima, però, comprendi alcuni concetti importanti in questo caso, come il significato dei termini: indice, coefficiente stechiometrico e mol. Questi termini verranno spiegati di seguito e ci daranno un'idea migliore della parte quantitativa della reazione:
- Indice: è il numero che indica il numero di atomi di ciascun elemento presenti nelle formule chimiche. Questo numero si trova a destra dell'elemento in questione e appare in pedice, cioè in una dimensione del carattere più piccola.
Esempio:
h2oh (formula chimica della sostanza acquosa)
Cosa significa:
- Gli elementi che compongono questa sostanza sono H (idrogeno) e O (ossigeno).
- L'indice di ciascun elemento indica quanti atomi di ciascuno sono presenti nella formula della molecola d'acqua:
h2O→ O-index: c'è solo 1 atomo di ossigeno.
↓
Indice H: indica che ci sono 2 atomi di idrogeno.
Nota che nel caso dell'ossigeno non c'è un numero scritto, il che significa che c'è solo 1 atomo di quell'elemento, come spiegato sopra.
Ora, ci sono alcuni casi in cui le parentesi appaiono nelle formule. Come dobbiamo interpretare questo? Vedi l'esempio qui sotto:
Qui3(POLVERE4)2(formula chimica della sostanza fosfato di calcio)
- Il contenuto di Ca indica che nella formula chimica sono presenti 3 atomi dell'elemento calcio;
- La P (fosforo) e la O (ossigeno) sono tra parentesi, quindi l'indice che è esterno, che in questo caso è 2, appartiene ad entrambi. Quindi, per scoprire quanti atomi di ciascuno ci sono nella formula, devi moltiplicare i loro indici separatamente per l'indice esterno. Nota come si fa:

Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
P → indice 1 O → indice 4
P = 1. 2O = 4. 2
P = 2 O = 8
Quindi ci sono 2 atomi di fosforo e 8 di ossigeno.
- Coefficiente stechiometrico: è il numero che precede la formula per indicare la quantità di ciascuna sostanza e la proporzione di molecole che partecipano alla reazione. Quindi, come nel caso dell'indice, quando il coefficiente è uguale a 1, non è necessario scriverlo, poiché è implicito.
Esempio:
2h2 + 1oh2 → 2 h2O (questa reazione di formazione dell'acqua è mostrata nella figura introduttiva)
↓ ↓ ↓
Coefficienti di reazione
In questa equazione, attraverso i coefficienti, si mostra che due molecole di gas idrogeno reagiscono con una di gas ossigeno, per formare come prodotto due molecole di acqua. Pertanto, il rapporto stechiometrico di questa reazione è 2:1:2.
Per conoscere il numero totale di atomi di ciascun elemento presenti nella reazione è necessario moltiplicare i coefficienti per gli indici di ciascun elemento:
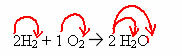
Reagenti:
H = 2. 2 = 4 atomi di idrogeno
O = 1. 2 = 2 atomi di ossigeno
Prodotto:
H = 2. 2 = 4 atomi di idrogeno
O = 1. 2 = 2 atomi di ossigeno
Nota che hai dato la stessa quantità ai reagenti e ai prodotti, il che significa che la reazione è bilanciata correttamente.
- Mol (quantità di materia):in un'equazione chimica, i coefficienti sono considerati per indicare la quantità di mole o la quantità di materia. Quindi, nel caso precedente abbiamo 2 moli di H2 reagendo con 1 mole di O2, generando come prodotti 2 moli di H2O.
di Jennifer Fogaça
Laureato in Chimica
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Aspetto:
FOGAÇA, Jennifer Rocha Vargas. "Termini quantitativi in un'equazione chimica"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/quimica/termos-quantitativos-uma-equacao-quimica.htm. Consultato il 27 luglio 2021.