ITU entalpi (H) itu dapat didefinisikan sebagai kandungan energi dari setiap bahan atau sebagai energi keseluruhan dari suatu sistem. Namun, dalam praktiknya, tidak mungkin menentukan entalpi suatu zat. Jadi, yang biasanya diukur adalah variasi entalpi 

Kami akan menganalisis di sini variasi entalpi dalam reaksi eksoterm (kata "exo" berasal dari bahasa Yunani dan berarti "keluar, dari, keluar"), yang merupakan reaksi di mana ada pelepasan panas. Dalam kehidupan sehari-hari, banyak contoh reaksi yang terjadi, seperti pembakaran dan pencampuran kapur tohor dengan air.
Dalam kasus ini, variasi entalpi 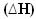 akan persis jumlah panas yang dilepaskan, diberikan oleh nilai entalpi akhir dikurangi entalpi awal (Hf - Hsaya) atau, karena merupakan reaksi, nilai entalpi produk dikurangi reaktan (HP - HR).
akan persis jumlah panas yang dilepaskan, diberikan oleh nilai entalpi akhir dikurangi entalpi awal (Hf - Hsaya) atau, karena merupakan reaksi, nilai entalpi produk dikurangi reaktan (HP - HR).
Saat panas dilepaskan, energi hilang. Dengan demikian, energi total sistem berkurang, sehingga entalpi produk akan selalu lebih rendah dari reagen, sehingga variasi entalpi dalam reaksi eksotermik akan selalu negatif, kurang dari nol 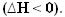
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
Mempertimbangkan reaksi eksotermik umum:
| A → B + panas |
Hal ini dapat dinyatakan dengan menggunakan diagram entalpi seperti di bawah ini:
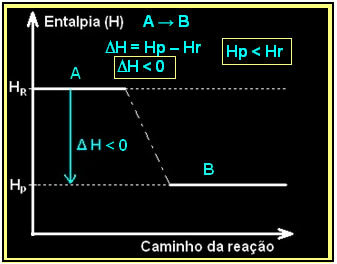
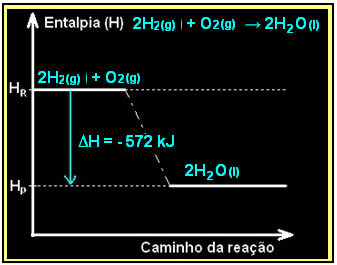
Pembakaran gas hidrogen, dengan pembentukan air cair, terjadi dengan pelepasan energi. Nilai variasi entalpi sistem dalam reaksi ini diberikan oleh:
2 jam2 (g) + O2 (g) → 2H2HAI(1)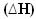 = - 572 kJ
= - 572 kJ
Diagram Anda akan direpresentasikan sebagai berikut:
Oleh Jennifer Fogaa
Lulus kimia
Apakah Anda ingin mereferensikan teks ini di sekolah atau karya akademis? Lihat:
FOGAÇA, Jennifer Rocha Vargas. "Variasi Entalpi pada Reaksi Eksotermik"; Sekolah Brasil. Tersedia di: https://brasilescola.uol.com.br/quimica/variacao-entalpia-reacoes-exotermicas.htm. Diakses pada 28 Juni 2021.
Kimia

Termokimia, Entalpi, Panas yang Dilepaskan, Reaksi Eksotermik, Reaksi Pembakaran, Lingkungan Eksternal, Reaksi Endotermik, Reaksi kimia, pertukaran energi, reagen, emisi cahaya, penyerapan cahaya, panas, listrik, komponen, keadaan fisik, produk.