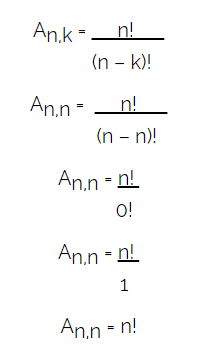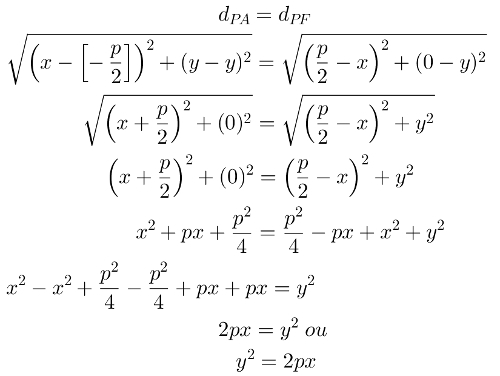geometriai izomer egyfajta űrizomerizmus amely értékeli és összehasonlítja egy lánc két szénatomjának ligandumának térbeli helyzetét. Ez az értékelés az érintett szénatomok közötti képzeletbeli síkból készül.
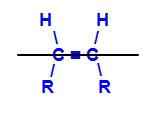
Képzelt sík osztja el a molekulát
A fenti szerkezet képzeletbeli síkja felosztja a molekulát egy felső és egy alsó síkra. Ezzel kiértékelhetjük és összehasonlíthatjuk az egyes síkokban részt vevő szén-ligandumokat. Tekintse meg a geometriai izomerek típusait:
→ Cisz-transz geometriai izomer
Egy vegyületnek van cisz-transz geometriai izomerizmus amikor a lánc megjelenik:
Nyitott lánc kettős kötéssel két szén között, amelyek azonos összekötőkkel rendelkeznek egymással. Lásd egy példát:
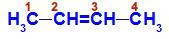
A But-2-én szerkezeti képlete
A felépítésben megfigyelhetjük, hogy mind a 2-es, mind a 3-as szénatomnak ugyanazok a ligandumai vannak, amelyek hidrogén (H) és metil (CH3).
Zárt lánc két szénnel, amelyek azonos ligandumokkal rendelkeznek egymással. Lásd egy példát:
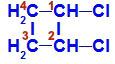
Az 1,2-diklór-ciklobután szerkezeti képlete
A felépítésben megfigyelhetjük, hogy az 1-es és a 2-es szén egyaránt azonos ligandumokkal rendelkezik, amelyek hidrogén (H) és klór (Cl).
A cisz-transz izomerizmus magyarázatához a but-2-ént fogjuk használni:
a) Cisz izomer: az a geometriai izomer, amelyben ugyanazok a ligandumok ugyanazt a síkot foglalják el. Az alábbi példában a hidrogének ugyanazon a síkon vannak, mint a metilcsoportok.

A cisz-but-2-én szerkezeti képlete
b) transz-izomer: az a geometriai izomer, amelyben a különböző ligandumok ugyanazt a síkot foglalják el. Az alábbi példában ugyanazon a síkon van hidrogén és metil (CH3).
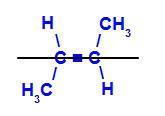
A transz-but-2-én szerkezeti képlete
Ne álljon meg most... A reklám után még több van;)
→ E-Z geometriai izomer
Egy vegyületnek E-Z geometriai izomerizmusa van, ha a lánc:
Nyitott lánc kettős kötéssel két szénatom között, amelyek mindegyike vagy néhány különböző összekötővel rendelkezik. Lásd egy példát:
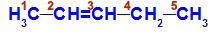
A pent-2-én szerkezeti képlete
A felépítésben láthatjuk, hogy a 2-es szénatomban van metil-ligandum (CH3) és hidrogén (H), és a 3 szénatom rendelkezik hidrogén (H) és etil (H) ligandummal3C-CH2).
Zárt lánc két szénatommal, amelyeknek az összes vagy néhány liganduma eltér egymástól. Lásd egy példát:
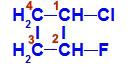
Az 1-klór-2-fluor-ciklobután szerkezeti képlete
A szerkezetben megfigyelhetjük, hogy az 1. szén fő liganduma hidrogén és klór, míg a 2. szén fő hidrogén és fluor.
JEGYZET: A különböző ligandumok közül a geometriai izomerizmusban értékeljük a ligandum komplexitását (atomok számát) vagy atomszámát.
Az E-Z izomer magyarázatához mind pent-2-ént, mind 1-klór-2-fluor-ciklobutánt használunk:
a) E-izomer
geometriai izomer ahol a bonyolultabb vagy a legnagyobb atomszámú ligandumok ellentétes síkokon helyezkednek el. A következő példában a 2-es szén legösszetettebb liganduma a metil, a 3-as szén legösszetettebb liganduma az etil, amelyek különböző síkokban helyezkednek el.
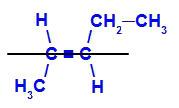
Az E-pent-2-én szerkezeti képlete
b) Z izomer
geometriai izomer ahol a bonyolultabb vagy a legmagasabb atomszámú ligandumok ugyanazon a síkon helyezkednek el. A következő példában az 1-es szén legmagasabb atomszámú liganduma a klór (Z = 17), a legmagasabb 2-es atomszámú ligandum pedig a fluor (Z = 9), amelyek ugyanabban a síkban helyezkednek el.
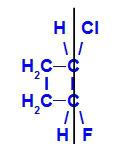
A Z-1-klór-2-fluor-ciklobután szerkezeti képlete
Általam. Diogo Lopes Dias
Hivatkozna erre a szövegre egy iskolai vagy tudományos munkában? Néz:
NAPOK, Diogo Lopes. "Mi a geometriai izomerizmus?"; Brazil iskola. Elérhető: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria-geometrica.htm. Hozzáférés: 2021. június 28.
Kémia
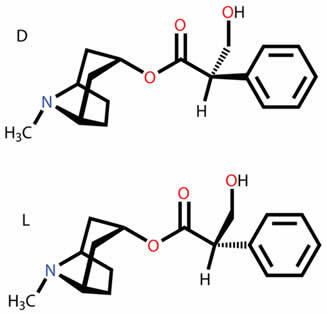
Tudja meg, mi a különböző síkbeli és térbeli izomerek, például a funkció, a helyzet, a lánc, a tautomerizmus, a metamerizmus, a cisz-transz geometriai és az optikai izomerizmus.