Organske reakcije su reakcije koje se odvijaju između organskih spojeva. Postoji nekoliko vrsta reakcija koje se događaju razbijanjem molekula što dovodi do novih veza.
Od njih se često mogu proizvoditi lijekovi i kozmetički proizvodi, plastika, između ostalog i u industriji.
glavni vrste organskih reakcija oni su:
- reakcija dodavanja
- reakcija zamjene
- reakcija eliminacije
- Reakcija oksidacije
Reakcija dodavanja
Reakcija dodavanja odvija se kada se veze organske molekule puknu i u nju se doda reagens.
To se uglavnom događa u spojevima čiji su lanci otvoreni i koji imaju nezasićenja, poput alkena () i alkini (
).
Primjeri reakcija zbrajanja
Primjer 1: hidrogeniranje (dodavanje vodika)
Hidrogeniranjem alkena nastaje alkan.
Primjer 2: halogeniranje (dodavanje halogena)
Halogeniranjem alkena nastaje halid.
Primjer 3: hidratacija (dodavanje vode)
Hidratacija alkena stvara alkohol.
Pročitajte i vi: Organski spojevi
Zamjena Reakcija
Reakcija supstitucije događa se kada postoje atomi veze (ili skupina) koji su zamijenjeni drugima.
To se uglavnom događa među alkanima, ciklanima i aromatima.
Primjeri reakcija zamjene
Primjer 1: halogeniranje (supstitucija s halogenom)
Halogeniranjem alkana nastaje halid.
Primjer 2: nitriranje (supstitucija nitro)
Nitriranjem alkana nastaje nitro spoj.
Primjer 3: sulfonacija (supstitucija sulfonikom)
Sulfoniranjem alkana nastaje kiselina.
Pročitajte i vi: Organske funkcije
Reakcija eliminacije
Reakcija eliminacije odvija se kada se ugljični ligand ukloni iz organske molekule.
Ova reakcija suprotna je reakciji adicije.
Primjeri reakcija eliminacije
Primjer 1: uklanjanje vodika (dehidrogenacija)
Uklanjanjem vodika iz alkana nastaje alken.
Primjer 2: uklanjanje halogena (dehalogeniranje)
Eliminacijom halogena iz dihalida stvara se alken.
Primjer 3: eliminacija halogenida
Uklanjanjem halogenida iz halogenida nastaje alken.
Primjer 4: uklanjanje vode (dehidracija alkohola)
Uklanjanjem vode iz alkohola nastaje alken.
Vidi i ti: esterifikacija
Reakcija oksidacije
Reakcija oksidacije, koja se naziva i redoks, odvija se kada postoji dobitak ili gubitak elektrona.
Primjeri reakcija oksidacije
Primjer 1: energetska oksidacija alkena
Energetskom oksidacijom alkena nastaju karboksilne kiseline.
Primjer 2: primarna oksidacija alkohola
Energetskom oksidacijom primarnog alkohola nastaju karboksilna kiselina i voda.
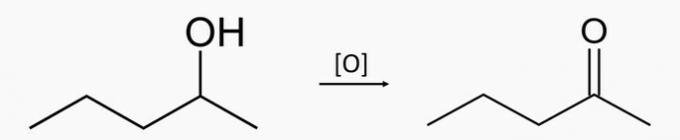
Primjer 3: sekundarna oksidacija alkohola
Oksidacijom sekundarnog alkohola nastaju keton i voda.
Pročitajte i vi: Karboksilne kiseline
Vježbe na organskim reakcijama
Pitanje 1
(Unifesp / 2002) Mnogi alkoholi mogu se dobiti hidratacijom alkena kataliziranom kiselinom.
U ovoj reakciji dodavanja, H u vodi se dodaje ugljiku koji ima više vodika, a hidroksilna skupina se veže na manje hidrogenirani ugljik (Markovnikovo pravilo).
Znajući da su alkoholi koji nastaju hidratacijom dva alkena, odnosno 2-metil-2-pentanol i 1-etilciklopentanol, koja su imena odgovarajućih alkena koji su ih stvorili?
a) 2-metil-2-penten i 2-etilciklopenten.
b) 2-metil-2-penten i 1-etilciklopenten.
c) 2-metil-3-penten i 1-etilciklopenten.
d) 2-metil-1-penten i 2-etilciklopenten.
e) 3-metil-2-penten i 2-etilciklopenten.
Točna alternativa: b) 2-metil-2-penten i 1-etilciklopenten.
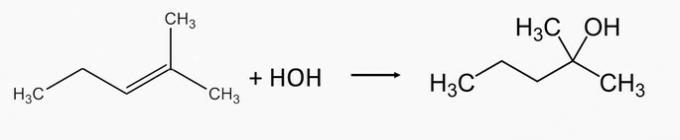
2-metil-2-pentanol alkohol nastaje hidratacijom 2-metil-2-pentena alkena.
1-etilciklopentanol alkohol nastaje hidratacijom 1-etilciklopentena alkena.
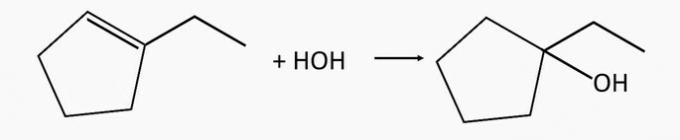
pitanje 2
(Ufal / 2000) U proučavanju kemije ugljikovih spojeva doznaje se da BENZEN:
() To je ugljikovodik.
() Može se dobiti iz acetilena.
() U ulju je komponenta većeg masenog udjela.
() Može proći reakciju supstitucije.
() To je primjer molekularne strukture koja predstavlja rezonanciju.
(TOČNO) Benzen je aromatski ugljikovodik. Ovaj spoj tvore samo atomi ugljika i vodika čija je formula C6H6.
(TOČNO) Benzen se može dobiti iz acetilena slijedećom reakcijom:
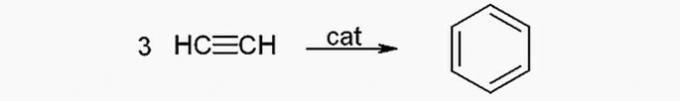
(NETOČNO) Nafta je smjesa ugljikovodika i masa komponenata povezana je s veličinom lanca. Stoga veći ugljikovi lanci imaju veću masu. Teže frakcije nafte, poput asfalta, imaju lance s više od 36 atoma ugljika.
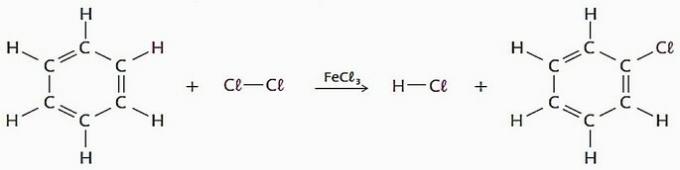
(TOČNO) Reakcije supstitucije upotrebom benzena kao reagensa imaju brojne industrijske primjene, uglavnom za proizvodnju lijekova i otapala.
U tom se procesu atom vodika može zamijeniti halogenima, nitro skupinom (-NO2), sulfonska skupina (—SO3H), između ostalih.
Pogledajte primjer ove vrste reakcije.
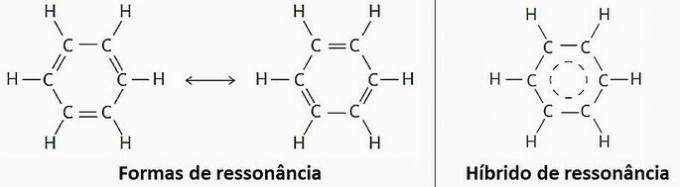
(ISTINITO) Zbog rezonancije benzen se može predstaviti s dvije strukturne formule.
Međutim, u praksi je uočeno da su duljina i energija veza uspostavljenih između atoma ugljika jednake. Stoga je rezonancijski hibrid najbliži stvarnoj strukturi.
pitanje 3
(UFV / 2002) Reakcija oksidacije alkohola s molekularnom formulom C5H12O ‚s KMnO4 daje spoj molekulske formule C5H10O.
Označite opciju koja prikazuje PRAVILNU korelaciju između naziva alkohola i naziva nastalog proizvoda.
a) 3-metilbutan-2-ol, 3-metilbutanal
b) pentan-3-ol, pentan-3-on
c) pentan-1-ol, pentan-1-on
d) pentan-2-ol, pentanal
e) 2-metilbutan-1-ol, 2-metilbutan-1-on
Ispravna alternativa: b) pentan-3-ol, pentan-3-on.
a) POGREŠNO. Oksidacijom sekundarnog alkohola nastaje keton. Stoga je ispravan proizvod za oksidaciju 3-metilbutan-2-ola 3-metilbutan-2-on.
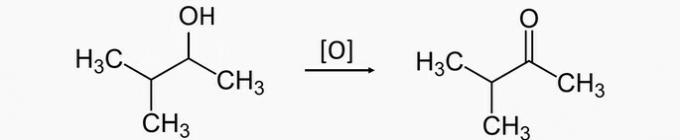
b) TOČNO. Oksidacijom sekundarnog alkohola pentan-3-ol nastaje keton pentan-3-ona.

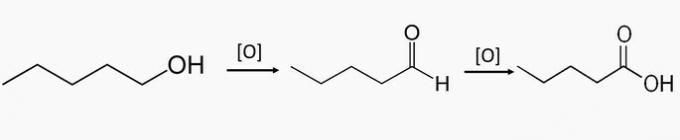
c) POGREŠNO. Ti su spojevi dio oksidacije primarnih alkohola, koji proizvode aldehid ili karboksilnu kiselinu.
Pentan-1-ol je primarni alkohol i djelomičnom oksidacijom spoja pentanal može nastati, a ukupnom oksidacijom nastaje pentanska kiselina.
d) POGREŠNO. Oksidacijom pentan-2-ol sekundarnog alkohola nastaje pentan-2-on keton.
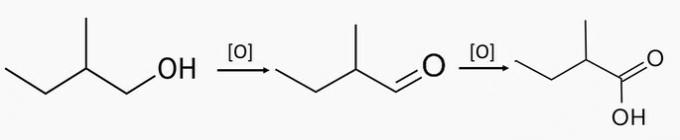
e) POGREŠNO. Primarni alkohol 2-metilbutan-1-ol stvara aldehid 2-metilbutanal u djelomičnoj oksidaciji, a 2-metilbutanska kiselina u ukupnoj oksidaciji.
pitanje 4
(Mackenzie / 97) U reakciji eliminacije koja se događa u 2-bromobutanu s kalijevim hidroksidom u alkoholnom mediju, dobiva se smjesa dva organska spoja koji su položajni izomeri.
Jedan od njih, koji nastaje u manjoj količini, je 1-buten. Drugi je:
a) metilpropen.
b) 1-butanol.
c) butan.
d) ciklobutan.
e) 2-buten.
Ispravna alternativa: e) 2-buten.
Alkeni nastaju reakcijom organskog halogenida HBr s kalijevim hidroksidom KOH, u prisutnosti etilnog alkohola kao otapala.

Različiti spojevi nastali su zbog atoma halogena koji se nalazi u sredini ugljikovog lanca, stvarajući više od jedne mogućnosti eliminacije.
Međutim, iako postoje dvije mogućnosti proizvoda, oni neće imati iste količine.
Za ovu reakciju 2-buten stvorit će se u većoj količini, jer dolazi od uklanjanja tercijarnog ugljika. 1-buten je nastao eliminacijom primarnog ugljika i, prema tome, nastala je manja količina.