Djelovanje katalizatora u osnovi je ubrzavanje razvoja određene reakcije. To je moguće jer katalizator mijenja mehanizam kojim se reakcija odvija, što dovodi do "alternativnog puta" koji zahtijeva manje energije za aktiviranje da bi reakcija započela i došla do aktiviranog kompleksa.
Postoji nekoliko vrsta katalize, od kojih je jedna heterogena kataliza, koji se može definirati kao ono što se događa kada sustav ima više od jedne faze, odnosno reaktanti i proizvodi su u fizikalnom stanju različitom od fizikalnog stanja katalizatora.
Primjer koji možemo spomenuti je srednji stupanj stvaranja sumporne kiseline (H2SAMO4 (vod.)). Ovaj se korak sastoji od stvaranja sumpornog trioksida (SO3 (g)) reakcijom izgaranja sumpornog dioksida (SO2 (g)):
2 PA2 (g) + O2 (g) → 2 OS3 (g)
Kako se ova reakcija odvija tako sporo, za njezino ubrzanje koristi se katalizator. Katalizator koji se može upotrijebiti u ovom slučaju je divanadij pentoksid (V2O5 (S)), što je solidno. Budući da su reaktanti i produkti reakcije plinoviti, imat ćemo heterogeni sustav.
Ali kako divanadij pentoksid može ubrzati reakciju?
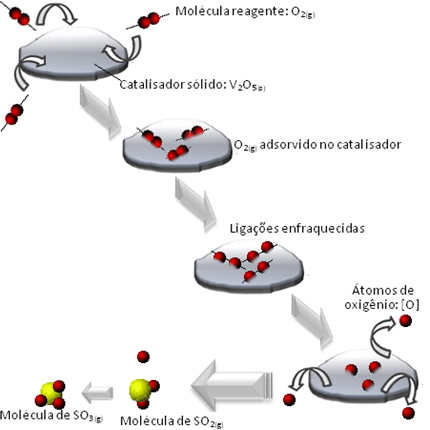
Ono što se događa jest da se molekule kisikovog reagensa adsorbiraju, odnosno zadrže na površini divanadij pentoksida. To uzrokuje da veze molekula ovog plina vremenom slabe, što olakšava stvaranje kompleksa aktivira se i, posljedično, smanjuje energiju aktivacije reakcije, povećavajući njezin stupanj razvoja, odnosno brzina.
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Pogledajte kako se to događa na donjem dijagramu:
Ostali primjeri heterogene katalize prikazani su u nastavku. Imajte na umu da su u oba slučaja reaktanti i proizvodi u plinovitom, vodenom ili tekućem stanju, dok su katalizatori u krutom stanju:
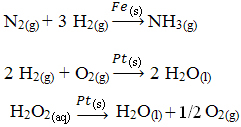
Primjer heterogene katalize koja se događa u našem svakodnevnom životu je pretvarača automobil katalitički, poznatiji kao katalizatori. Ovi uređaji protiv onečišćenja pokriveni su tvarima koje djeluju kao katalizatori obično legura paladija i rodija (za benzinske motore) i paladija i molibdena (za benzinske motore). alkohol).
Unutar ovog katalizatora događaju se kemijske reakcije u kojima se plinovi od nepotpunog izgaranja, koji su štetniji za ljude, pretvaraju u netoksične plinove. Reagensi i proizvodi su svi plinovi, dok su katalizatori krute tvari.
Da biste razumjeli više o operativnom sustavu ove opreme, pročitajte tekst: "Katalizator”.
Napisala Jennifer Fogaça
Diplomirao kemiju
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
FOGAÇA, Jennifer Rocha Vargas. "Heterogena kataliza"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/catalise-heterogenea.htm. Pristupljeno 27. lipnja 2021.