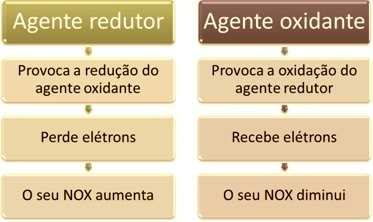
Jedno od glavnih obilježja koje razlikuju reakciju redukcije oksidacije (ili redoks) ostalih je prisutnost oksidirajućeg i redukcijskog sredstva, što se može definirati kako slijedi:
Na primjer, pogledajte donju kemijsku reakciju gdje aluminij (Al) nagriza u vodenoj otopini klorovodične kiseline (HCl). Atomi aluminija prenose elektrone u H katione+(ovdje) i proizvode Al kation3+(ovdje):
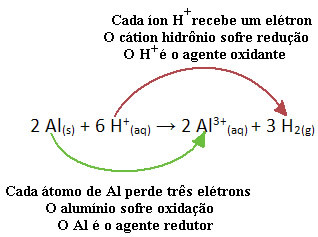
Imajte na umu da, budući da je Al prenio elektrone, to znači da on je izazvao smanjenje kationa H+(ovdje); zato je i pozvan redukcijsko sredstvo. Već je kation H+(ovdje) uklonili elektrone iz aluminija, uzrokujući oksidaciju od tog metala; stoga djeluje kao a oksidirajuće sredstvo.
U svakodnevnom životu postoji mnogo primjera djelovanja oksidirajućih i redukcijskih sredstava. Pogledajte neke od njih i sjetite se, međutim, da se u svim slučajevima redukcija događa istodobno s oksidacijom; dakle, ako postoji redukcijsko sredstvo, postoji i oksidacijsko sredstvo.
- Primjeri redukcijskih sredstava:
- U fotografskim filmovima: fotografski filmovi sadrže srebrne soli osjetljive na svjetlost. U mjestima gdje postoji pojava svjetlosti dolazi do smanjenja iona Ag+, što rezultira kontrastom uočenim u negativima.

- Vitamin C: Vitamin C (L-askorbinska kiselina) snažno je reducirajuće sredstvo u vodenoj otopini. Ima izuzetnu sposobnost oksidacije i zato se široko koristi, posebno u hrani poput antioksidans, odnosno dodaje se drugim namirnicama i štiti ih od moguće oksidacije, zbog vlastite žrtva. Primjer je voće poput jabuka i krušaka koje potamne u dodiru s kisikom u zraku, jer oksidiraju. Ali kad voću dodate malu količinu soka od naranče ili limuna (koji sadrže vitamin C) rezati, ovo sprječava pojavu ove reakcije, jer vitamin C djeluje kao redukcijsko sredstvo i oksidira prije voća.

- Vodikov plin: plin vodik (H2) koristi se u raketnom pogonu i smatra se jednom od najvažnijih energetskih alternativa, jer njegovo izgaranje oslobađa veliku količinu energije i nema zagađivača. U ovoj reakciji vodik djeluje kao redukcijsko sredstvo i oksidira se kisikom.
- Primjeri oksidacijskih sredstava:
- U proizvodnji octa: kada je vino izloženo zraku, ono se pretvara u ocat čija je glavna komponenta octena kiselina. To je zato što etilni alkohol ili etanol prisutni u vinu oksidiraju u dodiru s atmosferskim kisikom, što rezultira octenom kiselinom. Dakle, kisik je oksidirajuće sredstvo. Čak je i podrijetlo izraza "oksidacija" povezano s reakcijom s kisikom.

Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
- U hrđi: kao što je navedeno u prethodnom primjeru, kisik djeluje kao oksidacijsko sredstvo za alkohol; a to čini i u dodiru s raznim metalima, poput željeza, uzrokujući proces hrđanja. Osim kisika u zraku, druga oksidacijska sredstva u ovom su slučaju voda ili kisela otopina.
- U izbjeljivačima: učinak izbjeljivanja izbjeljivača posljedica je prisutnosti sljedeća dva redukcijska sredstva: o hipoklorit anion (općenito u obliku natrijeve soli - NaOCl), prisutan, na primjer, u bjelilu; i vodikov peroksid (H2O2), koji se prodaje kao vodikov peroksid. Ova dva spoja imaju vrlo jaku tendenciju oksidacije i uzrokuju smanjenje ostalih kemijskih vrsta. Stoga su odgovorni za oksidacijske tvari koje proizvodima daju tamnu boju. Primjerice, u celulozi se lignin razgrađuje i postaje lakši i podatniji. U slučaju uklanjanja mrlja i izbjeljivanja tkanine, ovi oksidanti uzrokuju oksidaciju organskih molekula kao što su masti i boje.

- U alkotestima: jednostavan alkotest za jednokratnu upotrebu sastoji se od prozirne cijevi koja sadrži vodenu otopinu dikromatske soli kalija i silicijevog dioksida, navlaženu sumpornom kiselinom; pomiješana s narančastom bojom. Ova sol u dodiru s alkoholnom parom koja se nalazi u dahu pijanog vozača reagira, mijenjajući boju u zelenu. To znači da je uzrokovana oksidacija etanola (alkohola) u etanal.

Napisala Jennifer Fogaça
Diplomirao kemiju
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
FOGAÇA, Jennifer Rocha Vargas. "Pojam i primjeri redukcijskog i oksidacijskog agensa"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/conceito-exemplos-agente-redutor-agente-oxidante.htm. Pristupljeno 28. lipnja 2021.
Kemija

Atmosferski čelik otporan na koroziju, krom, nikal, proizveden od sirovog željeza u visokim pećima, otporan na visokotemperaturna oksidacija, Nerđajući čelik, grupa legura željeza otporna na oksidaciju i koroziju, proizvodnja dijelova za vozilo
Kemija

Kako alkotest djeluje, koncentracija alkohola, alkotest, reakcije koje uključuju etilni alkohol, vrste alkotesti, kalijev dikromat, gorivna ćelija, katalizator, otpuštanje elektrona, octena kiselina, vodik, konce
Kemija

Fotoosjetljive leće, reakcije redukcije oksidacije, gubitak ili dobitak elektrona, fotosintetske leće u sunčanim naočalama, sastav fotokromatskog stakla, tetraedrični atomi kisika, kristalna struktura srebrnog klorida, ultraljubičasto svjetlo, srebrni metal


