L'hydrogénation se produit avec des hydrocarbures acycliques insaturés, c'est-à-dire qui ont des chaînes ouvertes avec des liaisons doubles ou triples, tels que les alcènes, les alcynes et les diènes. Il peut également se produire dans les hydrocarbures aromatiques, car ils ont des doubles liaisons dans le cycle, et avec des cyclanes (cycloalcanes) jusqu'à cinq carbones.
Ces composés réagissent comme de l'hydrogène gazeux en présence de certains catalyseurs, tels que le nickel, le platine et le palladium, sous chauffage. Ainsi, une réaction d'addition se produit, dans laquelle la liaison pi (π) est rompue, formant deux nouvelles liaisons simples et de l'hydrogène est introduit dans la molécule.
De manière générique, nous avons :
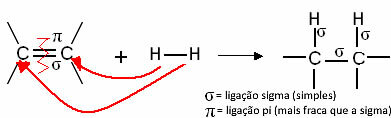
Réaction d'hydrogénation générique
Voyons maintenant quelques exemples :
- Hydrogénation en alcènes: Le produit obtenu est un alcane.
Ci-dessous nous avons une réaction d'hydrogénation de l'éthylène (ou de l'éthylène) pour obtenir de l'éthane :
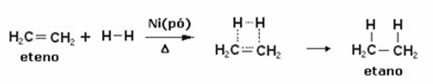
Exemple de réaction d'hydrogénation de l'éthylène
Ce type d'hydrogénation catalytique est utilisé par l'industrie alimentaire pour fabriquer des graisses semi-solides telles que margarine. Les huiles et graisses végétales ne diffèrent que par le fait que les huiles ont de longues molécules avec des doubles liaisons entre les carbones, tandis que les graisses n'ont que des liaisons simples entre leurs carbones.
Ainsi, pour transformer une huile en graisse, il suffit d'hydrogéner l'huile. De cette façon, vos doubles liaisons seront rompues et converties en simples liaisons. Le résultat est la production d'appels graisses végétales hydrogénées.
- Hydrogénation des alcynes: Comme les alcynes ont deux liaisons pi, leur hydrogénation complète se déroule en deux étapes, dans la première un alcène est formé et dans la seconde, un alcane.
Dans la réaction ci-dessous, on a l'hydrogénation du propyne avec formation finale du propane :
1ère étape : H3C C ≡ CH+ H2 → H3C CH═ ÇH2
2ème étape : H3C CH═ ÇH2 + 2 heures2 → H3C CH2─ ÇH3
Si nous voulons que cette réaction s'arrête dans la 1ère étape, nous devons utiliser une substance qui interrompt l'action du catalyseur.
- Hydrogénation des diènes: Il existe trois types de diènes: accumulé (les doubles liaisons apparaissent ci-dessous), isolé (les doubles liaisons sont séparées par au moins deux simples liaisons) et conjugués (des doubles liaisons apparaissent en alternance).
L'hydrogénation des diènes accumulés et isolés se produit de la même manière que nous l'avons vu pour les alcènes, mais en double, car les diènes ont plus d'insaturation. Voir deux exemples :
* Exemple d'hydrogénation en diène accumulé :
H H H
│ │ │
H3C CH ═ Ç ═ CH CH3 + 2 heures2 → H3C CH ─ Ç ─ CH CH3
│ │ │
H H H
* Exemple d'hydrogénation en diène isolé :
H H H H
│ │ │ │
H3C CH ═ CH─CH2 CH ═ CH CH3 +2H2 → H3C CH ─ CH─CH2 CH ─ CH CH3
D'autre part, l'hydrogénation des diènes conjugués peut se faire de deux manières: avec 1,2 addition et 1,4 addition. La plus courante est l'addition 1,2, dans laquelle des hydrogènes sont ajoutés aux carbones qui forment la double liaison et à basse température. L'addition 1,4, en revanche, se produit à des températures élevées et se produit lorsqu'il y a résonance et apparition de valences libres dans les carbones 1 et 4. Voir des exemples de chaque cas :
* Exemple d'addition 1.2 dans les diènes conjugués :
H2C CH CH ═ CH2 + H2 → H2C CH C ─ CH CH2
│ │
H H
* Exemple d'addition 1.4 dans les diènes conjugués :
H2C CH CH ═ CH2 + H2 → H2C CH ═ CH CH2
│ │
H H
- Hydrogénation des aromatiques: Les liaisons pi du cycle benzénique sont rompues et les atomes d'hydrogène sont ajoutés aux carbones qui forment ces liaisons.
Ce type d'hydrogénation totale est illustré ci-dessous :

Réaction d'hydrogénation du benzène total
- Hydrogénation des cyclanes: La formation d'un alcane se produit.
Exemple: Hydrogénation du cyclopropane :
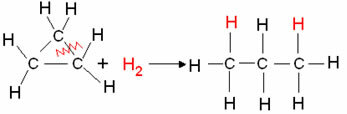
Réaction d'hydrogénation du cyclopropane
Par Jennifer Fogaça
Diplômé en Chimie
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/reacao-organica-hidrogenacao.htm
