Le pH correspond au potentiel hydrogéné d'une solution. Elle est déterminée par la concentration en ions hydrogène (H+) et sert à mesurer le degré d'acidité, de neutralité ou d'alcalinité d'une solution donnée.
En plus du pH, il existe également une autre quantité qui détermine l'acidité et la basicité d'un système aqueux: le pOH (potentiel hydroxylionique). Cette échelle a la même fonction que le pH, bien qu'elle soit moins utilisée.
échelle de pH
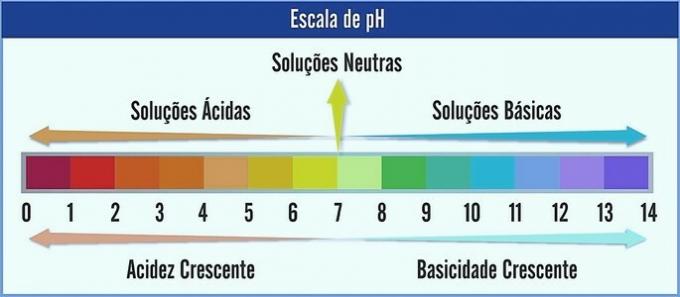
Le pH est représenté sur une échelle allant de 0 à 14. Il mesure l'acidité et la basicité d'une solution.
Par conséquent, pH 7 représente une solution neutre (par exemple de l'eau pure). Ceux qui le précèdent sont considérés comme des solutions acides (pH acide) et ceux après 7 sont des solutions basiques (pH alcalin).
Avec cette observation faite, le caractère acide augmente de droite à gauche. Le personnage de base, de gauche à droite. Notez que plus le pH est bas, plus la solution sera acide.
En savoir plus sur:
- Solution tampon
- Titrage
- Réaction de neutralisation
Exemples
Solutions acides
| Solution | pH |
|---|---|
| Suc gastrique | 2,0 |
| Jus de citron | 2,2 |
| Le vinaigre | 3,0 |
| Café | 5,0 |
| Lait de vache | 6,4 |
Solutions de base
| Solution | pH |
|---|---|
| sang humain | 7,35 |
| Eau de mer | 7,4 |
| Bicarbonate de sodium | 8,4 |
| Lait de magnésie | 10,5 |
| Eau de Javel | 12,5 |
Comment calculer le pH ?
En 1909, le chimiste danois Soren Sörensen (1868-1939) a proposé que l'acidité des solutions, mesurée en termes de concentrations d'ions H+, a vu ses valeurs transformées à l'aide de logarithmes pour faciliter la compréhension.
A une température de 25 °C le produit ionique de l'eau est égal à 10–14 mole2/L2.
En appliquant le cologarithme dans l'expression, nous devons :
Grâce à cette expression, nous pouvons obtenir la valeur correspondante d'une échelle à l'autre par soustraction.
Comment mesurer le pH ?
Le contrôle du pH est important non seulement à des fins scientifiques, mais aussi dans la vie de tous les jours.
Le pH de la piscine doit être vérifié, ainsi que le pH de l'aquarium et même le pH du sol pour permettre certains types de cultures.
Vous trouverez ci-dessous les principales façons de mesurer le pH.
indicateur acido-basique
Les indicateurs dits acido-basiques sont utilisés pour mesurer le pH d'une solution. Ce sont des substances qui changent de couleur indiquant le caractère de la solution. Les indicateurs les plus utilisés sont: le tournesol et la phénolphtaléine.

Pédomètre
En plus des indicateurs, le pH d'une solution peut être mesuré à l'aide d'un instrument appelé peagomètre. Cet appareil électronique mesure la conductivité électrique de la solution et la convertit à l'échelle des valeurs de pH.

Exercices d'examen d'entrée avec rétroaction
1. (Enem/2014) Un chercheur se rend compte que l'étiquette d'un des verres dans lequel il conserve un concentré d'enzymes digestives est illisible. Il ne sait pas quelle enzyme le verre contient, mais soupçonne qu'il s'agit d'une protéase gastrique, qui agit dans l'estomac en digérant les protéines.
Sachant que la digestion dans l'estomac est acide et que l'intestin est basique, il assemble cinq tubes à essai avec de la nourriture différent, ajoutez le concentré d'enzyme à des solutions avec un pH déterminé et attendez de voir si l'enzyme agit dans n'importe quel leur.
L'éprouvette dans laquelle l'enzyme doit agir pour indiquer que l'hypothèse du chercheur est correcte est celle qui contient :
a) cube de pomme de terre en solution avec pH = 9
b) morceau de viande en solution avec pH = 5
c) blanc d'oeuf bouilli en solution avec pH = 9
d) portion de nouilles en solution avec pH = 5
e) boule de beurre en solution avec pH = 9
Alternative correcte: b) morceau de viande en solution avec pH = 5.
La protéase est une enzyme qui digère les protéines et parce qu'elle est gastrique elle agit dans l'estomac, dont le pH est acide.
En analysant les alternatives, nous devons :
Un tort. Les pommes de terre sont riches en glucides et le pH du concentré est basique.
b) CORRECT. La viande contient des protéines et des enzymes peuvent agir dessus, et le pH du concentré est acide, comme l'estomac.
c) FAUX. Le pH du concentré est basique.
d) FAUX. Les pâtes sont riches en glucides.
e) FAUX. Le pH du concentré est basique.
2. (Udesc/2009) « Pluie acide » est un terme faisant référence aux précipitations de l'atmosphère de pluie avec des quantités supérieures à la normale d'acides nitrique et sulfurique.
Les précurseurs des pluies acides proviennent à la fois de sources naturelles, telles que les volcans et la végétation en décomposition, et de processus émissions industrielles, principalement de dioxyde de soufre et d'oxydes d'azote provenant de la combustion de combustibles fossiles.
Le pH de l'eau de pluie considéré comme normal est de 5,5 (en raison de la présence d'acide carbonique issu de la solubilisation du dioxyde de carbone). Un chimiste surveillant une région hautement industrialisée a noté que le pH de l'eau de pluie était de 4,5.
Considérant que l'acidité est liée à la concentration de H3O+, il est exact de dire que l'eau avec un pH de 4,5 était :
a) deux fois plus basique que la normale.
b) deux fois plus acide que la normale.
c) dix fois plus basique que la normale.
d) dix fois plus acide que la normale.
e) cent fois plus acide que la normale.
Alternative correcte: d) dix fois plus acide que la normale.
D'après les expressions pH = - log [H+] et [H+] = 10-pH, Nous devons:
pH = 5,5
[H+] = 10-5,5
pH = 4,5
[H+] = 10-4,5
La différence entre les valeurs est: 10- 5,5 - ( - 4,5) = 10 -1
L'échelle de pH étant une échelle logarithmique, un changement d'une unité équivaut à une solution 10 fois plus acide.
3. (UFMG/2009) Considérons une certaine quantité d'eau et de jus de citron, mélangés, contenus dans un verre. Passez en revue ces trois déclarations concernant ce système :
JE. Le système est acide.
II. Le pH du système est supérieur à 7.
III. Dans le système, la concentration des ions H+ est plus grand que le OH–.
Sur la base de cette analyse, il est CORRECT de déclarer que :
a) seuls les énoncés I et II sont corrects.
b) seuls les énoncés I et III sont corrects.
c) seuls les énoncés II et III sont corrects.
d) les trois affirmations sont correctes.
Alternative correcte: b) seules les affirmations I et III sont correctes.
JE. CORRIGER Le citron contient de l'acide citrique qui, en solution, libère des ions H+ et donc le système est acide.
II. TORT. Le pH est inférieur à 7, caractérisant un système acide: plus le pH de la solution est proche de 0, plus il est acide.
III. CORRIGER Le pH acide est le résultat de la forte concentration d'ions H+ en solution, puisque pH = - log [H+].
Pour plus de questions, avec une résolution commentée, assurez-vous de vérifier :Exercices sur le pH et le pOH.