LES pression osmotique c'est une propriété colligative qui correspond à la pression qui doit être exercée sur un système pour empêcher l'osmose de se produire spontanément.
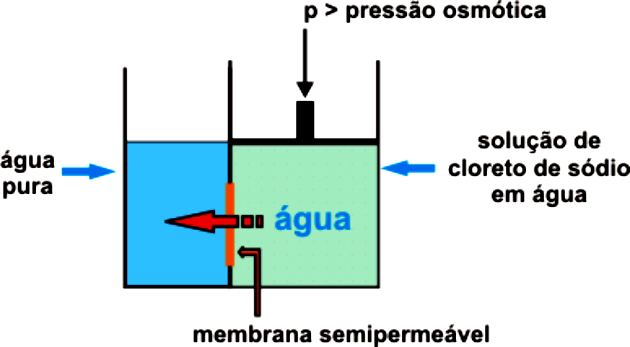
L'osmose est le passage de l'eau d'un milieu moins concentré (hypotonique) à un milieu plus concentré (hypertonique) à travers une membrane semi-perméable jusqu'à ce que l'équilibre soit atteint.
Pour éviter que l'osmose ne démarre et se produise naturellement, il est nécessaire d'appliquer une pression externe sur la solution la plus concentrée, empêchant le passage du solvant vers le milieu plus concentré. C'est la pression osmotique.
Plus la solution est concentrée, plus la pression osmotique doit être élevée. Par conséquent, la pression osmotique est proportionnelle à la concentration en soluté.
Comment calculer la pression osmotique ?
Chaque solution a une valeur de pression osmotique différente. La pression osmotique peut être calculée à partir de la formule suivante :
= M. UNE. T. je
Où, on a les variables suivantes :
= pression osmotique ;
M = concentration en mol/L ;
R = constante universelle des gaz, dont la valeur correspond à 0,082 atm. L. mole-1. K-1 ou 62,3 mm Hg L. mole-1. K-1;
T = température sur l'échelle absolue (Kelvin) ;
i = facteur de Van't Hoff, qui comprend la relation entre le nombre total de particules finales et initiales dans les solutions ioniques.
Exercice résolu
1. (Puccamp-SP) Occasionnellement, la solution de glucose 0,30 M est utilisée en injection intraveineuse, car elle a une pression osmotique proche de celle du sang. Quelle est la pression osmotique, en atmosphères, de ladite solution à 37°C ?
a) 1,00.
b) 1,50.
c) 1,76.
d) 7.63.
e) 9.83.
Compte tenu des données fournies par la question, nous avons :
M = 0,30 mol/L ;
R = 0,082 atm. L. mol-1. K-1
T = 37° + 273 = 310 K
Vous devez maintenant appliquer ces valeurs à la formule de calcul de la pression osmotique :
= M. UNE. T. je
π = 0,30. 0,082. 310
= 7,63 atm (Alternative)
Classement des solutions
Les solutions peuvent être classées en trois types, selon la pression osmotique :
- solution hypertonique: A une pression osmotique et une concentration de soluté plus élevées.
- solution isotonique: Lorsque les solutions ont la même pression osmotique.
- solution hypotonique: A une pression osmotique et une concentration de soluté plus faibles.

L'importance de la pression osmotique pour les êtres vivants
La solution saline est une substance préparée sur la base des principes de la pression osmotique. Il doit être appliqué à une pression osmotique égale à celle trouvée dans le corps, cela empêche la Globules rouges ne souffrent pas d'hémolyse et ne se ratatinent pas.
La pression osmotique du sang est d'environ 7,8 atm. Par conséquent, pour le bon fonctionnement de l'organisme, les globules rouges doivent avoir la même pression osmotique, assurant l'écoulement normal de l'eau dans et hors des cellules.
En cas de déshydratation, par exemple, l'utilisation d'une solution saline est indiquée, qui doit être isotonique par rapport aux cellules sanguines et autres fluides corporels.
La solution saline a pour fonction de rétablir l'équilibre osmotique à l'intérieur du corps. C'est parce que pendant la déshydratation, le sang devient plus concentré qu'à l'intérieur des cellules, ce qui les fait flétrir.
Osmose et Osmose Inverse
Comme nous l'avons vu, le osmose c'est le processus de passage de l'eau de l'environnement hypotonique à l'environnement hypertonique, à travers une membrane semi-perméable, jusqu'à ce que l'équilibre entre les concentrations soit atteint.
Pendant ce temps, le osmose inverse c'est un processus de séparation des substances à travers une membrane qui retient le soluté. Le solvant s'écoule du milieu le plus concentré vers le moins concentré et est isolé du soluté par une membrane qui permet son passage.
Cela ne se produit qu'en raison de la pression exercée, ce qui fait que la membrane semi-perméable ne laisse passer que l'eau, retenant le soluté. Cette pression doit être supérieure à la pression osmotique naturelle.
Par exemple, si la pression osmotique appliquée est supérieure à ce qui est nécessaire, une osmose inverse se produira. Ainsi, le flux passera du milieu ayant la plus forte concentration à celui ayant la plus faible concentration.