Dans le texte "Titre ou pourcentage de masse” nous avons vu comment calculer le rapport entre la masse du soluté et la masse de la solution, pour les solutions solides, liquides et gazeuses. Dans ce texte, cependant, nous verrons qu'il est également possible de calculer le titre en termes de volume, pour des solutions avec des composants liquides ou gazeux.

Le titre en volume peut être calculé par l'expression :
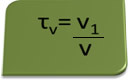
Prenons comme exemple une solution aqueuse d'alcool éthylique utilisée comme antiseptique et désinfectant, qui a été préparé en ajoutant 70 ml d'alcool pur à suffisamment d'eau pour obtenir un volume de 100 ml de solution. Donc nous avons:
τ = 70 ml = 0,7
100 ml
Nous pouvons également exprimer le titre en pourcentage, en multipliant simplement le résultat par 100 %. Donc, dans ce cas, nous avons une solution d'alcool éthylique à 70%, ce qui signifie que sur 100 unités de volume de la solution, 70 unités de volume sont de l'alcool.
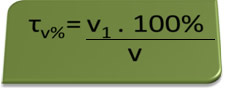
Dans le cas ci-dessous, nous avons une solution d'alcool éthylique à 70 % dans un volume de solution de 250 mL; ce qui signifie que 175 ml sont de l'alcool, selon les calculs :
100 ml 70 ml d'alcool
250 ml x
x = 70. 250
100
X = 175 ml d'alcool

Cependant, nous ne pouvons pas dire que dans ce cas, nous avons 75 ml (250-175) d'eau. Contrairement au titre massique, dans lequel on peut ajouter la masse du solvant à la masse du soluté pour trouver la masse de la solution, cela ne peut pas se faire par rapport au titre volumique.

Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
Cela signifie que le volume de solution n'est pas égal à la somme du volume de solvant et du volume de soluté (bien que souvent la différence puisse être considérée comme négligeable). En effet, les forces intermoléculaires qui existent dans ces liquides influencent le volume final.
Dans le cas de la solution précitée, d'alcool éthylique par exemple, lorsque l'on mélange de l'alcool à de l'eau, il se produit une contraction du volume total de la solution; c'est-à-dire que le volume final sera plus petit que si nous ajoutions le volume d'alcool et d'eau seuls. En effet, les molécules d'alcool établissent des liaisons ou des liaisons hydrogène avec les molécules d'eau, réduisant les espaces entre elles.
Par conséquent, dans ce cas et dans d'autres, le volume de la solution doit être mesuré expérimentalement lorsqu'il n'est pas fourni dans l'exercice.
Le pourcentage en volume est largement utilisé dans le cas des boissons alcoolisées et des alcools commerciaux, comme mentionné ci-dessus. Voir deux applications importantes de ce calcul :
- Alcootest : l'alcootest mesure la concentration d'alcool éthylique dans le sang, et au Brésil, il est interdit à quiconque de conduire tout type de véhicule avec un taux d'alcoolémie égal ou supérieur à 0,1% en volume. Une personne avec cette teneur en alcool a, pour chaque litre de sang, 1 ml d'alcool, comme le montrent les calculs suivants :
τv%=V1. 100%
v
0,1 % = V1. 100%
1L
V1 = 0,1% → V1 = 0,001 L = 1 ml
100%

- Teneur en éthanol dans l'essence: au Brésil, l'essence est réglementée par l'ajout d'éthanol. Mais la teneur en éthanol dans l'essence doit être d'au plus 24% en volume d'alcool anhydre (puisque l'essence doit être sans eau). Plus on ajoute d'éthanol à l'essence, plus la couleur du carburant s'éclaircit et sa densité augmente.
Par Jennifer Fogaça
Diplômé en Chimie
Souhaitez-vous référencer ce texte dans un travail scolaire ou académique? Voir:
FOGAÇA, Jennifer Rocha Vargas. « Titre du volume d'une solution chimique »; École du Brésil. Disponible en: https://brasilescola.uol.com.br/quimica/titulo-volume-uma-solucao-quimica.htm. Consulté le 28 juin 2021.
Chimie

Fonctionnement de l'éthylotest, concentration d'alcool, éthylotest, réactions impliquant l'alcool éthylique, types de alcootests, dichromate de potassium, pile à combustible, catalyseur, libération d'électrons, acide acétique, hydrogène, conce