O võrrandi tasakaalustamine võimaldab meil sobitada keemilises võrrandis olevate aatomite arv nii, et see saaks tõeks ja esindaks keemilist reaktsiooni.
Kasutage oma teadmiste kontrollimiseks allolevaid küsimusi ja kontrollige pärast tagasisidet kommenteeritud vastuseid küsimustele vastamiseks.
küsimus 1
(Mackenzie-SP)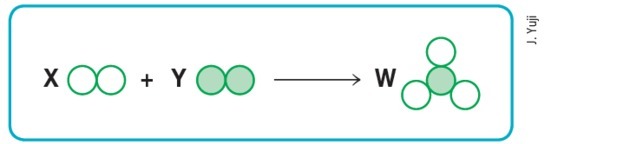
Eeldades, et tühjad ja täidetud ringid tähendavad vastavalt erinevaid aatomeid, siis skeem ülaltoodud kujutab tasakaalustatud keemilist reaktsiooni, kui asendame tähed X, Y ja W vastavalt tähtedega väärtused:
a) 1, 2 ja 3.
b) 1, 2 ja 2.
c) 2, 1 ja 3.
d) 3, 1 ja 2.
e) 3, 2 ja 2.
Alternatiiv d) 3, 1 ja 2.
1. samm: Määrame tähed, et võrrandit oleks hõlpsam mõista.
2. samm: liidame indeksid, et teada saada, kellel on võrrandis kõige rohkem aatomeid.
| THE | |
| B |
A ja B esinevad võrrandi igas liikmes ainult ühe korra. Kui aga liita indeksid, näeme, et A-l on kõige suurem väärtus. Seetõttu alustasime tema jaoks tasakaalustamist.
3. samm: Tasakaalustame elemendi A, viies indeksid üle ja muutes need koefitsientideks.
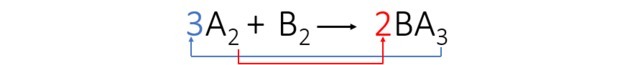
Täheldasime, et element B oli automaatselt tasakaalus ja võrrandi koefitsiendid on: 3, 1 ja 2.
2. küsimus
(Unicamp-SP) Lugege järgmine lause ja teisendage see (tasakaalustatud) keemiliseks võrrandiks, kasutades sümboleid ja valemeid: „gaasilise lämmastiku molekul, mis sisaldab kahte lämmastik molekuli kohta, reageerib kolme diatoomse, gaasilise vesiniku molekuliga, saades kaks molekulaarset gaasilist ammoniaaki, mis koosneb kolmest vesiniku aatomist ja ühest lämmastik ".
Vastus:
Esitades küsimuses kirjeldatud aatomeid, saame aru, et reaktsioon toimub järgmiselt:
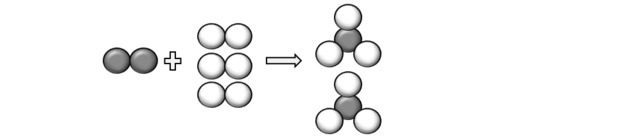
Niisiis jõuame võrrandini:
3. küsimus
Vesinikperoksiid on keemiline ühend, mis võib laguneda, moodustades vee ja hapniku vastavalt allpool toodud keemilisele võrrandile.
Selle reaktsiooni korral on õigesti tasakaalustatud võrrand:
a) H2O2 →2 + H2O
b) 2 tundi2O2 →2 + 2H2O
c) H2O2 → 2O2 + H2O
d) 2 tundi2O2 → 2O2 + 2H2O
Õige alternatiiv: b) 2H2O2 →2 + 2H2O
Pange tähele, et vesinikperoksiid on kemikaal, mis koosneb kahe keemilise elemendi aatomitest: vesinikust ja hapnikust.
Pärast lagunemisreaktsiooni peab teil nii reaktantides kui ka produktides olema sama arv kahe elemendi aatomeid. Selleks peame võrrandi tasakaalustama.
Pange tähele, et reagendis on 2 vesiniku aatomit (H2O2) ja kaks aatomit tootes (H2O). Hapnikul on aga reagendis kaks aatomit (H2O2) ja produktides kolm aatomit (H2O ja O2).
Kui panna koefitsient 2 vesinikperoksiidi ette, kahekordistame elementide aatomite arvu.
Pange tähele, et kui panna sama koefitsient koos vee valemiga, on meil mõlemal küljel sama kogus aatomeid.
Seetõttu on õigesti tasakaalustatud keemiline võrrand 2H2O2 →2 + 2H2O.
4. küsimus
(UFPE) Mõelge allpool toodud keemilistele reaktsioonidele.
Võime öelda, et:
a) kõik on tasakaalus.
b) 2, 3 ja 4 on tasakaalus.
c) ainult 2 ja 4 on tasakaalus.
d) ainult 1 on tasakaalustamata.
e) ükski neist pole õigesti tasakaalus, kuna reagentide ja saaduste füüsikalised olekud on erinevad.
Alternatiiv b) 2, 3 ja 4 on tasakaalustatud.
1. ja 5. alternatiiv on valed, kuna:
- 1. võrrand on tasakaalustamata, õige tasakaal oleks:
- 5. võrrand on vale, kuna reaktsioonis moodustunud ühend oleks H2AINULT3.
H moodustamiseks2AINULT4 tuleks võrrandisse lisada SO oksüdeerumine2.
5. küsimus
(Mackenzie-SP) 800 ° C-ni kuumutatud kaltsiumkarbonaat laguneb kaltsiumoksiidiks (neitsi lubi) ja süsinikdioksiidiks. Korrektselt tasakaalustatud võrrand, mis vastab kirjeldatud nähtusele, on:
(Arvestatud: Ca - leelismuldmetall.)
Alternatiiv c)
Kaltsium on leelismuldmetall ja stabiilsuse tagamiseks vajab kaltsium 2 elektroni (Ca2+), mis on hapniku laeng (O2-).
Seega seondub kaltsiumiaatom hapniku aatomiga ja moodustunud ühend on CaO, mis on kustutamata lubi.
Teine toode on süsinikdioksiid (CO2). Mõlemad moodustuvad kaltsiumkarbonaadist (CaCO3).
Pange see võrrandisse:
Märgime, et aatomite kogused on juba õiged ega vaja tasakaalustamist.
küsimus 6
(UFMG) Võrrand ei ole tasakaalus. Kui seda tasakaalustada võimalikult väikeste arvudega, on stöhhiomeetriliste koefitsientide summa järgmine:
a) 4
b) 7
c) 10
d) 11
e) 12
Alternatiiv e) 12
Proovimeetodit kasutades on tasakaalustamiskord järgmine:
1. samm: Kuna element, mis ilmub igas liikmes ainult üks kord ja millel on kõrgeim indeks, on kaltsium, hakkasime selle jaoks tasakaalu hoidma.
2. samm: Jälgime radikaalse PO tasakaalustamist43-, mis ilmub samuti ainult üks kord.
3. samm: tasakaalustame vesinikku.
Sellega täheldame, et automaatselt reguleeriti hapniku hulka ja võrrandi tasakaal on:
Pidades meeles, et kui koefitsient on 1, ei pea te seda võrrandisse kirjutama.
Meie koefitsientide lisamine:
7. küsimus
Põlemine on keemilise reaktsiooni tüüp, mille käigus energia eraldub soojuse kujul.
Süsiniku ja vesiniku moodustunud aine täielikul põlemisel moodustuvad süsinikdioksiid ja vesi.
Jälgige süsivesinike põlemisreaktsioone ja vastake, milline alltoodud võrranditest on valesti tasakaalustatud:
a) CH4 + 2O2 → CO2 + 2H2O
b) C3H8 +502 → 3CO2 + 4H2O
c) C4H10 + 13 / 3O2 → 4CO2 + 5h2O
d) C2H6 + 7 / 2O2 → 2CO2 + 3H2O
Vale vastus: c) C4H10 + 13 / 3O2 → 4CO2 + 5h2O
Keemiliste võrrandite tasakaalustamiseks vaatame kõigepealt, milline element ilmub võrrandi igas liikmes ainult ühe korra.
Pange tähele, et süsinik ja vesinik moodustavad igas esitatud võrrandis ainult ühe reaktiivi ja ühe toote.
Alustame siis vesinikuga tasakaalus hoidmist, kuna sellel on suurem aatomite arv.
Seetõttu on tasakaalustamise järjekord järgmine:
- Vesinik
- Süsinik
- Hapnik
Vesinik
Kuna tootel on 2 vesinikuaatomit, sisestame koefitsiendina arvu, mis korrutatakse 2-ga, tulemuseks on reagendi vesinikuaatomite arv.
a) CH4 + O2 → CO2 + 2H2O
b) C3H8 + O2 → CO2 + 4H2O
c) C4H10 + O2 → CO2 + 5H2O
d) C2H6 + O2 → CO2 + 3H2O
Süsinik
Tasakaalustamine toimub reagendi süsinikuindeksi ülekandmisega ja selle elemendi aatomeid sisaldava toote koefitsiendina kasutamisega.
a) CH4 + O2 → 1CO2 + 2H2O
b) C3H8 + O2 → 3CO2 + 4H2O
c) C4H10 + O2 → 4CO2 + 5h2O
d) C2H6 + O2 → 2CO2 + 3H2O
Hapnik
Lisades moodustunud produktides hapniku aatomite arvu, leiame reageeriva elemendi aatomite arvu.
Selleks peame koefitsiendina panema arvu, mis korrutatakse 2-ga, mille tulemuseks on toodetes hapniku aatomite arv.
a) CH4 + O2 → 1CO2 + 2H2O
2x = 2 + 2
2x = 4
x = 2
Nii et õige võrrand on: CH4 + 2O2 → 1CO2 + 2H2O.
b) C3H8 + O2 → 3CO2 + 4H2O
2x = 6 + 4
2x = 10
x = 5
Nii et õige võrrand on: C3H8 + 5O2 → 3CO2 + 4H2O
c) C4H10 + O2 → 4CO2 + 5h2O
2x = 8 + 5
2x = 13
x = 13/2
Nii et õige võrrand on: C4H10 + 13/2O2 → 4CO2+ 5h2O
d) C2H6 + O2 → 2CO2 + 3H2O
2x = 4 + 3
2x = 7
x = 7/2
Nii et õige võrrand on: C2H6 + 7/2O2 → 2CO2 + 3H2O
Õigesti tasakaalustatud võrrandid on:
a) CH4 + 2O2 → CO2 + 2H2O
b) C3H8 +502 → 3CO2 + 4H2O
c) C4H10 + 13 / 2O2 → 4CO2 + 5h2O
d) C2H6 + 7 / 2O2 → 2CO2 + 3H2O
Seega alternatiiv c) C4H10 + 13 / 3O2 → 4CO2 + 5h2Põhjus on selles, et sellel pole õiget tasakaalu.
8. küsimus
(Enem 2015) Lubjakivid on kaltsiumkarbonaadist koosnevad materjalid, mis võivad toimida vääveldioksiidi (SO2), oluline õhusaasteaine. Protsessis osalevad reaktsioonid on lubjakivi aktiveerimine kaltsineerimise teel ja SO fikseerimine2 kaltsiumisoola moodustumisega, mida illustreerivad lihtsustatud keemilised võrrandid.
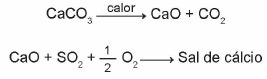
Võttes arvesse selle väävlitustamisprotsessi reaktsioone, vastab kaltsiumisoola keemiline valem järgmisele:
Alternatiiv b)
Kuna reaktsioon on tasakaalus, peavad reaktiivides sisalduvad aatomid olema produktides samas koguses. Seega
Moodustunud sool koosneb:
1 kaltsiumi aatom = Ca
1 väävliaatom = S
4 hapniku aatomit = O4
Seetõttu vastab kaltsiumisoola keemiline valem CaSO-le4.
küsimus 9
(UFPI) X reaktsioon Y-ga on näidatud allpool. Tehke kindlaks, milline võrrand esindab kõige paremini tasakaalustatud keemilist võrrandit.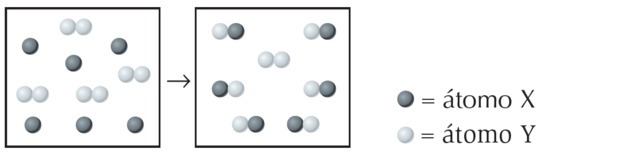
Alternatiiv a)
Joonisel täheldame, et liik X on üks aatom, samal ajal kui Y on diatoomiline, see tähendab, et see moodustub 2 aatomi liitumisel. Nii reageerib X Y-ga2.
Moodustunud toodet tähistab XY, kusjuures võrrand on tasakaalustamata:
Tasakaalustame võrrandi järgmiselt:
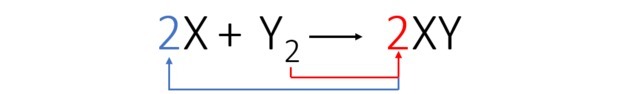
Tasakaalustatud võrrandi järgi näitab järgmine joonis meile, kuidas reaktsioon toimub ja selle osakaal.
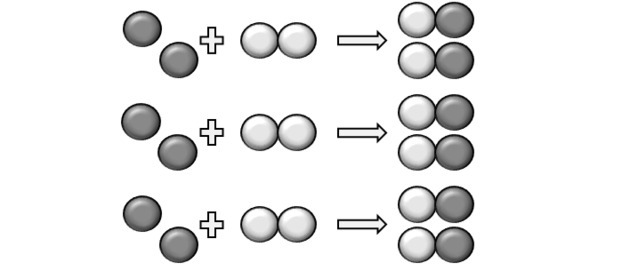
Reaktsiooni tekkimiseks peab olema kindel suhe ja seetõttu ei pruugi mõni ühend reageerida. Seda näitab joonis, sest tootes näeme, et Y2 ei reageerinud.
10. küsimus
(Enem 2010) Mobilisatsioone parema planeedi reklaamimiseks tulevastele põlvedele tehakse üha sagedamini. Enamik massitranspordivahendeid töötab praegu fossiilkütuse põletamise teel. Selle praktika põhjustatud koormuse näitena piisab teadmisest, et auto toodab keskmiselt umbes 200g süsinikdioksiidi läbitud kilomeetri kohta.
Ülemaailmse soojenemise ajakiri. 2., 8. aasta. Instituto Brasileiro de Cultura Ltda väljaanne
Bensiini üks peamisi koostisosi on oktaan (C8H18). Oktaanarvu põlemise kaudu on auto võimalik liikuma hakata. Selle protsessi keemilist reaktsiooni tähistav võrrand näitab, et:
a) protsessis eraldub hapnik O kujul2.
b) vee stöhhiomeetriline koefitsient on 8–1 oktaanarv.
c) selle käigus kulub vett, nii et energia vabaneb.
d) hapniku stöhhiomeetriline koefitsient on 12,5–1 oktaanarv.
e) süsinikdioksiidi stöhhiomeetriline koefitsient on 9–1 oktaan
Alternatiiv d) hapniku stöhhiomeetriline koefitsient on 12,5 kuni 1 oktaan.
Võrrandi tasakaalustamisel leiame järgmised koefitsiendid:
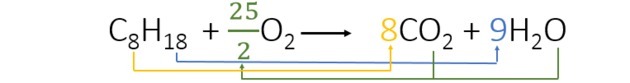
- Alustasime tasakaalustamist vesiniku abil, mis ilmub igas liikmes ainult üks kord ja mille indeks on kõrgem. Kuna reageerivaid vesiniku aatomeid on 18, on produktis 2, seega peame lisama arvu, mis korrutatakse 2-ga, saades 18. Seega on koefitsient 9.
- Seejärel lisame koefitsiendi 8 CO ette2 et igas võrrandi liikmes oleks 8 süsinikku.
- Lõpuks lisage lihtsalt toote hapniku kogus ja leidke väärtus, mis korrutatakse 2-ga, meile 25 hapnikuaatomit. Seega valisime 25/2 või 12.5.
Seega kulub ühe oktaanarvu põlemiseks hapnikku 12,5.
11. küsimus
(Fatec-SP) Väetiste oluline omadus on nende lahustuvus vees. Seetõttu muudab väetisetööstus kaltsiumfosfaadi, mille lahustuvus vees on väga madal, palju lahustuvamaks ühendiks, milleks on kaltsiumi superfosfaat. Seda protsessi esindab võrrand:
kus x, y ja z väärtused on vastavalt:
a) 4, 2 ja 2.
b) 3, 6 ja 3.
c) 2, 2 ja 2.
d) 5, 2 ja 3.
e) 3, 2 ja 2.
Alternatiiv e) 3, 2 ja 2.
Algebralise meetodi abil moodustame iga elemendi jaoks võrrandid ja võrdsustame reaktiivis olevate aatomite arvu toote aatomite arvuga. Seetõttu:
Tasakaalustatud võrrand:
küsimus 12
Tasakaalustage allpool toodud võrrandid katsemeetodi abil.
Vastus:
Võrrand koosneb vesiniku ja kloori elementidest. Tasakaalustame elemendid, lisades koefitsiendi 2 toote ette.
Võrrandit ei olnud vaja tasakaalustada, kuna aatomite kogused on juba kohandatud.
Fosforil on reagentides kaks aatomit, nii et selle elemendi tasakaalustamiseks reguleerime fosforhappe koguse tootes väärtusele 2H3TOLM4.
Pärast seda täheldasime, et vesinikul oli tootes 6 aatomit, tasakaalustasime selle elemendi koguse, lisades koefitsiendi 3 seda sisaldavale reaktandile.
Eelmiste sammudega fikseeriti hapniku kogus.
Võrrandit vaadates näeme, et vesiniku ja broomi kogused toodetes on kaks korda suuremad kui reagentides on, lisame nende kahe tasakaalustamiseks HBr-le koefitsiendi 2 elemendid.
Klooril on produktides 3 aatomit ja reagentides ainult 1 aatom, seega tasakaalustame koefitsiendi 3 panemist HCl-i ette.
Vesinikul oli reagentides 3 aatomit ja produktides 2 aatomit. Suuruste korrigeerimiseks teisendame H-indeksi2 koefitsiendina korrutame 3-ga, mis oli juba HCl-s, ja saame tulemuse 6HCl.
Korrigeerime toodetes sisalduvaid kloori koguseid, et neil oleks ka 6 aatomit, ja saame 2AlCl3.
Alumiiniumil oli toodetes 2 aatomit, reguleerisime reagentide koguse väärtuseks 2Al.
Tasakaalustame vesiniku koguse tootes 3H-ni2 ja me sobitame selle elemendi 6 aatomi hulga võrrandi igasse termini.
Valemis on nitraadiradikaal (NO3-) on tootes indeks 2, teisendame indeksi reaktiivis koefitsiendiks 2AgNO jaoks3.
Hõbeda kogust oli vaja reguleerida, kuna sellel on nüüd 2 aatomit reagentides, seega on meil tootes 2Ag.
Reagentides on meil 4 vesiniku aatomit ja selle elemendi tasakaalustamiseks lisame HCl-produktile koefitsiendi 2.
Klooril on nüüd produktides 4 aatomit, seega reguleerime reagendi koguse 2Cl-ni2.
Reagentides on 6 vesiniku aatomit ja selle elemendi tasakaalustamiseks reguleerime veekoguse 3H-ni2O.
Reagentides on 2 süsinikuaatomit ja selle elemendi tasakaalustamiseks reguleerime süsinikdioksiidi koguse 2CO-ni2.
Hapnik peab reageerivates ainetes sisaldama 7 aatomit ja selle elemendi tasakaalustamiseks reguleerime molekulaarse hapniku koguse väärtuseks 3O2.
Vaadates võrrandit, on nitraadiradikaal (NO3-) on tootes indeks 2. Indeksi teisendame koefitsiendiks 2 AgNO reaktiivis3.
Reagentides on 2 hõbeda aatomit ja selle elemendi tasakaalustamiseks reguleerime toote hõbekloriidi koguseks 2AgCl.
Meil on tootes 3 kaltsiumi aatomit ja selle elemendi tasakaalustamiseks reguleerime reaktiivis oleva kaltsiumnitraadi koguseks 3Ca (NO3)2.
Seejärel jääb meile 6 NO radikaali3- reaktantides ja selle radikaali tasakaalustamiseks reguleerime toodetes lämmastikhappe koguse 6HNO-le3.
Nüüd on produktides 6 vesinikuaatomit ja selle elemendi tasakaalustamiseks reguleerime fosforhappe koguse reaktiivis väärtuseks 2H3TOLM4.
Lisateavet keemiliste võrranditega arvutuste kohta leiate aadressilt:
- Keemiliste võrrandite tasakaalustamine
- Stöhhiomeetria
- Stöhhiomeetrilised arvutused
- Stöhhiomeetria harjutused
- Perioodiliste tabelite harjutused

