O radio atómico (r) generalmente se define como la mitad de la distancia entre dos núcleos de átomos vecinos, como representa la figura siguiente:

radio atómico
El radio atómico difiere de un átomo a otro según su familia y período en la tabla periódica. Con respecto a los elementos pertenecientes a un misma familia, su radio atómico aumenta a medida que aumenta el número atómico., es decir, de arriba a abajo. Porque, en este sentido, significa que de un átomo a otro se ha incrementado un nivel de energía o capa electrónica, por lo que su radio aumenta proporcionalmente.
Con respecto al elemento en el mismo período, es decir, horizontalmente, el radio aumenta de derecha a izquierda, o cuando el número atómico disminuye. Esto se debe a que todos tienen el mismo número de capas, lo que marca la diferencia es la cantidad de electrones en estas capas, y cuantos más electrones, mayor será la atracción hacia el núcleo, disminuyendo así el radio de la átomo.

Dirección de crecimiento del radio atómico según familia y período en la tabla periódica
Sin embargo, el radio atómico puede variar según la conexión que se realice. Veamos cómo sucede esto:
*Enlace iónico: Si el átomo forma un catión, el radio atómico disminuirá, dado que al perder uno o más electrones, el núcleo atraerá los electrones con mayor intensidad. Ahora si formar un anión, es decir, ganar electrones, el radio del átomo aumentará, ya que la carga total de la electrosfera será mayor que la carga total del núcleo, disminuyendo su atracción. Cuantos más electrones gane o pierda, mayor será la variación en el tamaño del haz.
No pares ahora... Hay más después de la publicidad;)
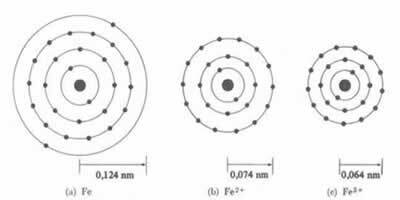
El diámetro o radio del catión es siempre menor que el diámetro o radio del átomo.
Además, en una serie de iones isoelectrónicos, que tienen la misma cantidad de electrones y niveles de energía, el ion con el menor número atómico tendrá un radio mayor. Por ejemplo, los iones 13Alabama3+, 12mg2+, 11A1+, 9F-1, 8O2- y 7norte-3, todos tienen 10 electrones y 2 niveles electrónicos. Pero lo que tiene el radio más grande es el 7norte-3, porque tiene el número atómico más pequeño (Z = 7).
*Enlace covalente: Cuando dos átomos forman un enlace covalente, si los dos átomos son iguales, como en el caso del gas hidrógeno (H2), se puede hablar de un radio covalente (r), que es la mitad de la longitud del enlace (d), es decir, la mitad de la distancia que separa los dos núcleos. Aunque, si el enlace está formado por diferentes átomos, como en el caso del cloruro de hidrógeno (HCl), la longitud o distancia (d) será la suma de los radios covalentes (r1 + r2) de los átomos involucrados en la covalencia.
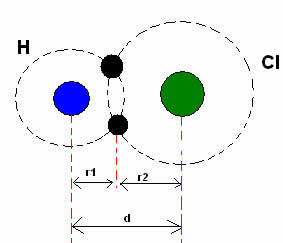
Suma de radios atómicos en un enlace covalente.
Por supuesto, debemos recordar que este tema es mucho más complicado, ya que el radio covalente de un átomo puede variar al unirse con otros átomos diferentes.
Por Jennifer Fogaça
Licenciada en Química
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
FOGAÇA, Jennifer Rocha Vargas. "Variación del radio atómico en enlaces químicos"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/quimica/variacao-raio-atomico-ligacoes-quimicas.htm. Consultado el 28 de junio de 2021.