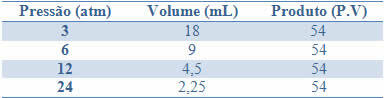
Αν ήταν δυνατόν να απεικονίσουμε τη δομή ενός μετάλλου πολύ καθαρά, θα το δούμε όπως στην παραπάνω εικόνα. Η ατομική δομή των μετάλλων είναι Κρυσταλλική, η οποία αποτελείται από μεταλλικά κατιόντα που περιβάλλονται από ηλεκτρόνια.
Τα κρυσταλλικά πλέγματα που υπάρχουν στα μέταλλα μπορούν να αναπαρασταθούν ως εξής: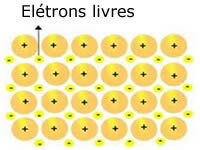
Αναπαράσταση μεταλλικού νατρίου (Na)
Τα κρυσταλλικά πλέγματα μετάλλων σχηματίζονται από μια ομάδα σταθερών κατιόντων.
Κάθε κατιόν Na + περιβάλλεται από ηλεκτρόνια, αλλά αυτά έχουν μετατοπιστεί, δηλαδή δεν προσελκύονται σε κανένα πυρήνα.
Καθώς δεν υπάρχει έλξη μεταξύ των αρνητικών φορτίων (ηλεκτρονίων) και του θετικού πυρήνα (κατιόν), τα ελεύθερα ηλεκτρόνια καταλήγουν να καταλαμβάνουν ολόκληρο το κρυσταλλικό πλέγμα του μετάλλου. Η ελευθερία που πρέπει να κινούνται τα ηλεκτρόνια τους προκαλεί να σχηματίσουν ένα ηλεκτρονικό νέφος.
Η ικανότητα των μετάλλων να μεταφέρουν ηλεκτρισμό εξηγείται από την παρουσία αυτού του νέφους. Το ηλεκτρικό ρεύμα προκύπτει από την επαφή ελεύθερων ηλεκτρονίων με άλλα μέταλλα.
Στη σύνθεση οποιουδήποτε ατόμου, συμπεριλαμβανομένων των μετάλλων όπως Νάτριο (Na), Gold Au, Copper (Cu), υπάρχει ένα στρώμα σθένους. Τα ηλεκτρόνια κινούνται ελεύθερα μέσω αυτού του στρώματος διατηρώντας την ηλεκτρομαγνητική έλξη κατιόντων. Αυτή η δομική ιδιότητα επιτρέπει το σχηματισμό μεταλλικών μορίων και, κατά συνέπεια, των ίδιων των μετάλλων.
Από τη Lria Alves
Αποφοίτησε στη Χημεία
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/quimica/como-se-forma-ligacao-metalica.htm