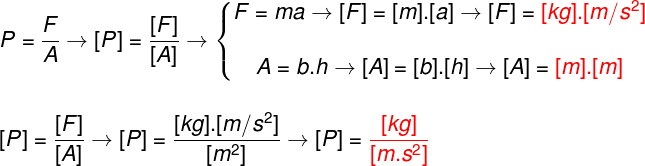Beim Hydratationsreaktionen in Alkadiene Sie sind Additionsreaktionend.h. die Komponenten (Hydronium und Hydroxid) des Wassermoleküls werden an ein Alkadien angelagert.
Sie Alkadiene sind Kohlenwasserstoffe, die eine offene Kette und zwei Doppelbindungen (gebildet durch ein Sigma und ein Pi) zwischen den Kohlenstoffen haben, wie wir in der folgenden Struktur sehen können:

Strukturformel eines Alkadiens
für die Hydratationsreaktion in Alkadienen durchgeführt wird, ist es unbedingt erforderlich, dass die in der Doppelbindung vorhandene pi-Bindung durch den Einfluss von Wärme und Schwefelsäure (H2NUR4). Beim Aufbrechen der pi-Bindung erscheinen zwei Bindungsstellen, jeweils an einem der an der Doppelbindung beteiligten Kohlenstoffe.

Entstehung von Bindungsstellen mit Unterbrechung der pi-Bindung
Das Auftreten von Bindungsstellen am Alkadienmolekül ist für die Ionen (H+ und oh-) aus dem Wasser werden dem Alkadien zugesetzt, wobei beispielsweise ein Dialkohol (Alkohol mit zwei Hydroxylen).
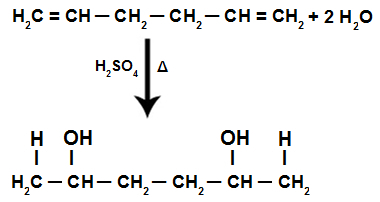
Zugabe von H+ und oh- in der Struktur eines Alkadiens
HINWEIS: Die Zugabe des H+ und oh- in der Alkadienstruktur folgt der Markownikows Regel, dh das H+ bindet an den am stärksten hydrierten Kohlenstoff, und das OH- bindet an den weniger hydrierten Kohlenstoff.

Beispiel für die Anwendung der Markownikow-Regel bei der Hydratation von Alkadienen
Da es hinsichtlich der Position der Doppelbindungen unterschiedliche Arten von Alkadienen gibt, kann es sein, dass die Hydratation eines Alkadiens unterschiedliche Verbindungen bildet. Siehe die folgenden Fälle:
→ Akkumuliertes oder kondensiertes Alkadien
Es ist ein Alkadien mit zwei Doppelbindungen, an denen gleichzeitig drei Atome von Kohlenstoff, d. h. es gibt keine Einfachbindung, die die an den Bindungen beteiligten Kohlenstoffe trennt Doppel.

Strukturformel eines akkumulierten Alkadiens
Während der Hydratationsreaktion eines alternierenden Alkadiens werden die pi-Bindungen aufgebrochen, da das H+ zu den stärker hydrierten Kohlenstoffen und dem OH. hinzugefügt- zu weniger hydrierten Kohlenstoffen hinzugefügt:
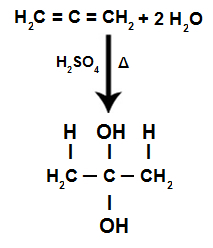
Reaktionsgleichung der akkumulierten Alkadienhydratation
Wir haben, dass bei der Hydratation eines angesammelten Alkadiens dasselbe Kohlenstoffatom die beiden Hydroxyle aufnimmt, wodurch ein Zwillingsalkohol entsteht, der eine instabile Struktur ist.

Struktur des Zwillingsalkohols
Da der Zwillingsalkohol instabil ist, kommt es zur Bildung eines Wassermoleküls mit den Komponenten der beiden Hydroxyle und zur Bildung einer Pi-Bindung zwischen Kohlenstoff und Sauerstoff.

Bildung eines Ketons aus einem Zwillingsalkohol
Daher führt die Hydratationsreaktion akkumulierter Alkadiene zur Bildung von a Keton.
→ Konjugiertes oder alternatives Alkadien
Es ist ein Alkadien mit zwei Doppelbindungen gleichzeitig mit vier Kohlenstoffatome, d. h. es gibt eine Einfachbindung, die die an den Bindungen beteiligten Kohlenstoffe trennt Doppel.
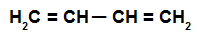
Strukturformel eines alternierenden Alkadiens
Bei alternierenden Alkadienen tritt die Resonanz ihrer Doppelbindungen auf. Somit ändern die Elektronen der Pi-Bindung ihre Position (rote Pfeile), wie im folgenden Diagramm:
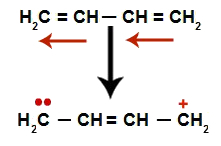
Schematische Darstellung der Resonanz in einem alternierenden Alkadien
Wir haben im Allgemeinen das Auftreten einer Doppelbindung genau zwischen den Kohlenstoffen, wo die beiden Doppelbindungen vorher waren und die Schaffung von zwei Bindungsstellen, eine an jedem Kohlenstoff, der keine Doppelbindung mehr bildet (im Beispiel Kohlenstoff 1 und 4). Kohlenstoff 1 und 4 der Kette erhalten das H the+ und das oh- aus dem Wasser.

Partielle Hydratation in alternierendem Alkadien
Nach der Resonanz wird die pi-Bindung der neuen Doppelbindung gebrochen und ein H+ und ein oh- werden an das Alkadienmolekül angelagert. Das OH wird an den Kohlenstoff addiert, der der ersten hinzugefügten OH-Gruppe am nächsten ist, weil es der elektronischen Anziehung der Gruppe unterliegt, die elektronegativer ist.

Beendigung der Hydratation in einem alternierenden Alkadien
Aufgrund der Resonanz sagen wir, dass das alternierende Alkadien eine 1.4-Hydratation durchlief, wodurch ein Dialkohol gebildet wurde.
→ Alkadien isoliert
Es ist ein Alkadien mit zwei Doppelbindungen, an denen mindestens fünf Atome gleichzeitig beteiligt sind. von Kohlenstoff, d. h. es gibt mindestens zwei Einfachbindungen, die die an den Bindungen beteiligten Kohlenstoffe trennen Doppel.

Strukturformel eines isolierten Alkadiens
Bei der Hydratationsreaktion eines isolierten Alkadiens werden die pi-Bindungen aufgebrochen, die H+ zu den stärker hydrierten Kohlenstoffen und dem OH. hinzugefügt- zu den weniger hydrierten Kohlenstoffen hinzugefügt.

Reaktionsgleichung der isolierten Alkadienhydratation
Daher haben wir bei der Zugabe eines isolierten Alkadiens nur die Bildung eines Diaalkohols.
Von mir. Diogo Lopes Dias
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/reacoes-hidratacao-alcadienos.htm