О балансиране на окислително-редукционно уравнение тя се основава на равенството на броя на подарените електрони и броя на получените електрони. Един прост метод за извършване на това балансиране се дава от следните стъпки:
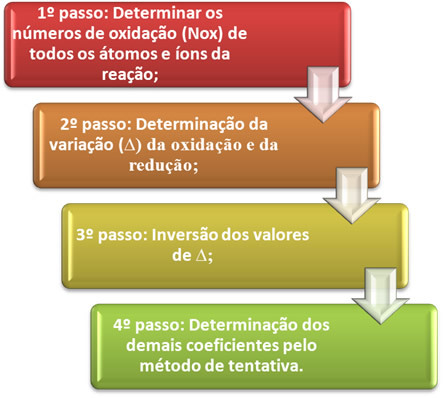
Нека да видим на практика как да приложим тези стъпки, чрез следния пример:
Реакция между воден разтвор на калиев перманганат и солна киселина:
kmnO4 + HCl → KCl + MnCl2 + Cl2 + Н2О
*1-ва стъпка:Определете окислителните числа:
Тази стъпка е важна, тъй като обикновено не можем бързо да си представим кои видове се подлагат на окисление и редукция.
+1 +7 -2 +1 -1 +1 -1 +2 -1 0 +1 -2
kmnO4 + HCl → KCl + MnCl2 + Cl2 + Н2О
*2-ра стъпка:Определяне на вариацията на окисление и редукция:

Обърнете внимание, че манганът (Mn) се редуцира, а хлорът (Cl) се окислява.
MnCl2 = OxNox = 5
Cl2 = OxNox = 2
В случая с хлора можем да отбележим, че HCl води до 3 съединения (KCl, MnCl2и Cl2), но това, което ни интересува, е Cl2, защото вашият Nox е претърпял вариации. Всеки хлор, който образува Cl2 губят 1 електрон; как са необходими 2 хлора, за да се образува всеки Cl
2, тогава два електрона се губят.3-та стъпка:Инверсия на ∆ стойности:
В тази стъпка стойностите на ∆ се обменят между споменатите видове, ставайки техни коефициенти:
MnCl2 = OxNox = 5 → 5 ще бъде коефициентът на Cl2
Cl2 = OxNox = 2→ 2 ще бъде коефициентът на MnCl2
kmnO4 + HCl → KCl + 2 MnCl2 + 5 Cl2 + Н2О
Към този момент вече е възможно да се знаят два коефициента на уравнението.
Наблюдение: обикновено при повечето реакции това обръщане на стойности се извършва на 1-ви член. Но като общо правило това трябва да се прави в члена, който има най-голям брой атоми, които се подлагат на редокс. Ако този критерий не може да бъде изпълнен, ние инвертираме стойностите за члена с най-голям брой химически видове. Това е направено тук, тъй като 2-ри член има повече вещества.
Не спирайте сега... Има още след рекламата;)
4-та стъпка: Пробно балансиране:
kmnO4 + HCl → KCl + 2 MnCl2 + 5 Cl2 + Н2О
- Тъй като във втория член има два манганови атома, както е показано от коефициента, в първия също трябва да има. Така че имаме:
2 kmnO4 + HCl → KCl + 2 MnCl2 + 5 Cl2 + Н2О
- По този начин количеството калий (К) в 1-ви член е 2, което ще бъде същият коефициент за този атом във втория член:
2 kmnO4 + HCl → 2 KCl + 2 MnCl2 + 5 Cl2 + Н2О
- Количеството хлор (Cl) във втория член е общо 16, така че коефициентът на HCl на първия член ще бъде:
2 kmnO4 + 16 HCl → 2 KCl + 2 MnCl2 + 5 Cl2 + Н2О
- Броят на водородите в 1-ви член е 16, следователно коефициентът на вода (H2O) на 2-ри член ще бъде равно на 8, тъй като умножението на водородния индекс (2) с 8 е равно на 16:
2 kmnO4 + 16 HCl → 2 KCl + 2 MnCl2 + 5 Cl2 + 8 З.2О
- За да проверим дали уравнението е правилно балансирано, можем да видим два критерия:
1-ви) Проверете дали количеството на всеки атом в двата члена е равно:
2 kmnO4 + 16 HCl →2 KCl + 2 MnCl2 + 5 Cl2 + 8 Н2О
K = 2K = 2
Mn = 2 Mn = 2
Cl = 16 Cl = 16
Н = 16 Н = 16
O = 8 O = 8
2-ро) Вижте дали общият брой на изгубените електрони е равен на общия брой на получените електрони:
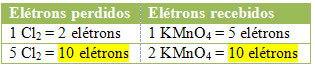
От Дженифър Фогаса
Завършва химия
Искате ли да се позовавате на този текст в училище или академична работа? Виж:
FOGAÇA, Дженифър Роча Варгас. "Roxi-редукционно балансиране"; Бразилско училище. Наличен в: https://brasilescola.uol.com.br/quimica/balanceamento-por-oxirreducao.htm. Достъп на 28 юни 2021 г.


