Идеите за конституцията на материята (атома) се появяват в древна Гърция, около 450 г. пр. Н. Е. а., главно от Демокрито и Левчипо. Атомът обаче всъщност получи научен характер едва след т.нар Атомната теория на Далтън.
НА Атомната теория на Далтън той е бил основополагащ за развитието на атомното знание, тъй като е служил като основа на други учени да познават атома и неговите характеристики.
Кой беше Джон Далтън?
Джон Далтън, химик по образование, е роден в Камбрия, Англия, през 1766 г. и умира в Манчестър през 1844 г. От ранна възраст животът му е бил предопределен за научни изследвания и преподаване, толкова много, че той е преподавал или допринасял за развитието на различни области на знанието.
Най-голямото му наследство като учен обаче е развитието на първата атомна теория. Чрез няколко експеримента, свързани със смесването на газове и познаването на произведенията, предложени от Лавоазие, атомната теория на Далтън се появява през 1808 г.
Постулати на атомната теория на Далтън
Атомната теория на Далтън се основава на експерименти, но нито един от тези експерименти не може да разкрие атома ясно. Следователно Далтън нарича атома най-малката част от материята.
Теорията на Далтън представя много повече постулати, отколкото доказателства. Вижте някои от тях:
Атомите са с масивна и сферична форма (подобно на билярдна топка);
Атомите са неделими;
Атомите са неразрушими;
Едно химичен елемент това е набор от атоми със същите свойства (размер и маса);
Атомите на различни химични елементи имат различни свойства помежду си;
За тяхното разграничаване може да се използва относителното тегло на два атома;
Съставният химикал се образува от една и съща комбинация от различни видове атоми;
Различните химични вещества се образуват чрез комбиниране на различни атоми.
Представления на атомния модел на Далтон
Далтън нарече атомния си модел билярдна топка и следователно започна да представя атомите на елементите, познати по негово време, посредством сферични символи.
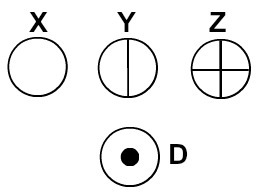
Атоми, представени съгласно атомната теория на Далтън
Всяко атомно представяне, което има конкретна подробност, показва различен химичен елемент. Дидактически книгите и упражненията за основно и средно ниво представляват атомите само от сфери с различни цветове.
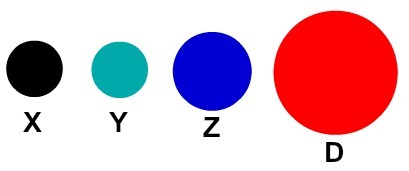
Дидактическо представяне на атомите
Принос на атомната теория на Далтън
разбиране за Закон за запазване на масата на Лавоазие
Френският химик Лавоазие твърди през 1785 г., че „При химична реакция масата се запазва, защото няма нито създаване, нито разрушаване на атомите ”. Атомната теория на Далтън доказа този факт, тъй като един от неговите постулати гласи, че атомът е неразрушим.
Следователно, ако извършваме изгарянето на въглища (C) в присъствието на кислороден газ (O2), ще имаме химическа реакция между един въглероден атом и два атома кислород. Тази реакция ще образува въглероден диоксид (CO2), който има абсолютно същите атоми, които са изграждали веществата преди реакцията.
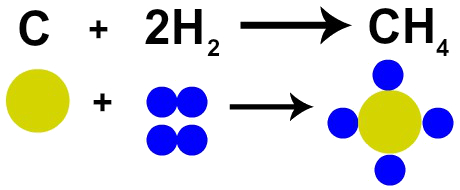
Представяне на закона на Лавоазие от атомния модел на Далтън
разбиране за прости вещества
Използвайки Атомният модел на Далтън, можем да разберем просто вещество, т.е. такова, което има атоми с една и съща характеристика, образуващи молекула. Следователно имаме атоми, принадлежащи към един и същ химичен елемент.
По вещество F2например имаме два флуорни атома, така че трябва да използваме два вида равни атоми в представянето според атомната теория на Далтън.

Просто представяне на веществото според Атомният модел на Далтън
разбиране за съставни вещества
В едно съединение имаме атоми с различни характеристики, образуващи молекулата. Следователно имаме различни химични елементи, образуващи веществото.
Вещество Н2О, например, има три атома: два водорода и един кислород. Вижте неговото представяне според атомния модел на Далтън:
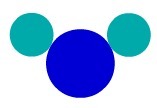
Представяне на съединено вещество според кожатаАтомният модел на Далтън
Разбиране на смесите
Разбирането на смес (обединение на две или повече различни вещества) чрез атомната теория на Далтън е просто: просто поставете две различни молекули в един и същ контейнер.

Представяне на втора смес Атомният модел на Далтън
Други научни приноси от Джон Далтън
въведе концепцията за атомна маса;
Той формулира закона за парциалното налягане на газовете (Законът на Далтън);
Открито зрително увреждане, наречено цветна слепота;
Изучава поведението на изпарения и газове при различни температури;
Той открил, че всички газове се разширяват (те се опитват да заемат определено място) в пространството по един и същи начин.
От мен Диого Лопес Диас
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/teoria-atomica-dalton.htm
