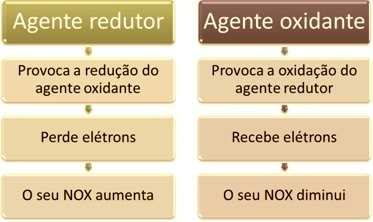
Една от основните характеристики, които отличават окислително-редукционната реакция (или редокс) от останалите е наличието на окислител и редуктор, което може да се определи, както следва:
Например, погледнете химическата реакция по-долу, където алуминият (Al) корозира във воден разтвор на солна киселина (HCl). Алуминиевите атоми пренасят електрони в Н катиони+(тук) и произвеждат катиона Al3+(тук):
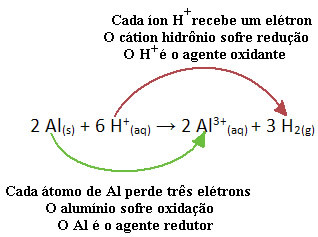
Имайте предвид, че тъй като Al е прехвърлял електрони, това означава, че той предизвика намалението на Н катионите+(тук); затова той е призован редуктор. Вече катионът Н+(тук) премахна електроните от алуминия, причиняващ окисление от този метал; следователно той действа като a окислител.
В ежедневието има много примери за ефективността на окислителите и редукторите. Погледнете някои от тях и не забравяйте обаче, че във всички случаи редукцията настъпва едновременно с окисляването; следователно, ако има редуциращ агент, има и окислител.
- Примери за редуциращи агенти:
- Във фотографски филми: фотографските филми съдържат чувствителни към светлина сребърни соли. В местата, където има честота на светлина, има намаляване на Ag йони +, което води до контраста, наблюдаван в негативите.

- Витамин Ц: Витамин С (L-аскорбинова киселина) е мощен редуциращ агент във воден разтвор. Той има изключителна способност да се окислява и затова се използва широко, особено в храни като антиоксидант, тоест той се добавя към други храни и ги предпазва от възможно окисляване, поради собствените си жертва. Пример за това са плодове като ябълки и круши, които потъмняват при контакт с кислород във въздуха, защото се окисляват. Но когато добавите малко количество портокалов или лимонов сок (които съдържат витамин С) към плодовете нарязан, това предотвратява появата на тази реакция, тъй като витамин С действа като редуциращ агент и се окислява преди плодовете.

- Водороден газ: водородният газ (Н2) се използва при ракетно задвижване и се счита за една от най-важните енергийни алтернативи, тъй като при изгарянето му се отделя голямо количество енергия и няма замърсители. В тази реакция водородът действа като редуктор, като се окислява от кислорода.
- Примери за окислители:
- При производството на оцет: когато виното е изложено на въздух, то се превръща в оцет, чийто основен компонент е оцетната киселина. Това е така, защото етиловият алкохол или етанолът, присъстващи във виното, се окисляват при контакт с атмосферния кислород, което води до оцетна киселина. По този начин кислородът е окислител. Дори произходът на термина „окисляване“ е свързан с реакцията с кислород.

- В ръждата: както е посочено в предишния пример, кислородът действа като окислител за алкохол; и прави това също в контакт с различни метали, като желязо, причинявайки процеса на ръждясване. В допълнение към кислорода във въздуха, други окислители в този случай са вода или киселинен разтвор.
- В избелващите средства: избелващият ефект на избелващите средства се дължи на присъствието на следните два редуциращи агента: o хипохлоритен анион (обикновено под формата на натриева сол - NaOCl), присъстващ, например, в белина; и водороден прекис (H2О2), предлагани на пазара като водороден прекис. Тези две съединения имат много силна склонност към окисляване и предизвикват редуциране на други химически видове. Следователно те са отговорни за окислителните вещества, които придават тъмен цвят на продуктите. Например в целулозата лигнинът се разгражда и става по-лек и пластичен. В случай на премахване на петна и избелване на тъкани, тези окислители причиняват окисляване на органични молекули като мазнини и багрила.

- В алкотестери: обикновен алкохол за еднократна употреба се състои от бистра тръба, съдържаща воден разтвор на дихроматната сол на калий и силициев диоксид, навлажнена със сярна киселина; смесен с оранжев цвят. Тази сол в контакт с алкохолните пари, съдържащи се в дъха на пияния шофьор, реагира, променяйки цвета си в зелен. Това означава, че е причинено окисляването на етанол (алкохол) до етанал.

От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/conceito-exemplos-agente-redutor-agente-oxidante.htm

