Текстът "Молекула с асиметричен въглерод и оптични изомери”Показа, че когато една молекула има само един асиметричен или хирален въглерод (с всички лиганди различни един от друг), той има два оптично активни изомера и един оптично неактивен изомер (смес рацемичен).
Сега нека разгледаме случая, че има два или повече различни асиметрични въглерода, т.е. те се считат за различни един от друг, защото поне един от техните лиганди не е еднакъв. Например, помислете за формулата на аспартама, който е 180 пъти по-сладък от захарозата (захарта) и поради това се използва в изкуствените подсладители:
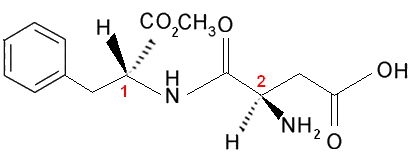
Имайте предвид, че тази молекула има два хирални въглерода, които са идентифицирани на изображението с числата 1 и 2. Тези въглероди имат своите четири групи на свързване, различни една от друга, така че те се считат за асиметрични. При сравняване на въглеродните лиганди 1 с въглеродните 2, виждаме, че единственият повтарящ се лиганд е Н (водородът), поради което са различни асиметрични въглероди.
Тази молекула и всички, които имат два асиметрични въглерода, винаги ще имат:
4 оптично активни изомера и 2 оптически неактивни изомера (две рацемични смеси).Знаем това, защото възможните вероятности са:

Всички други двойки изомери ще бъдат диастереоизомери (които не са огледални изображения един на друг), като смес от десен въглерод-1 и десен въглерод-2.
Обаче би било много трудно, ако трябва да продължим да разглеждаме всички възможности за всяка молекула, тъй като мнозина имат 3, 4, 5 или повече асиметрични въглероди.
По този начин най-лесният начин да се определи количеството оптично активни и неактивни изомери на молекула, която има няколко различни асиметрични въглероди е чрез математическите изрази, показани по-долу, които са предложени от Van't Hoff и Le Бел:
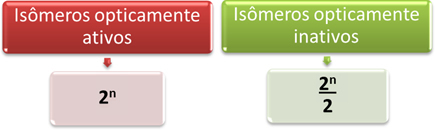
Където „n“ е количеството на различни асиметрични въглероди в молекулата. Например, в случая с аспартам, това са два асиметрични въглерода, така че имаме:
- Оптично активни изомери: 2не = 22 = 4;
- Оптично неактивни изомери: 2не = 22 = 2.
2 2
Даде точно сумата, която споменахме преди.
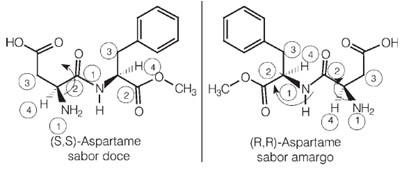
Интересното е, че един от енантиомерите на аспартама има този сладък вкус, който се използва в изкуствените подсладители, но един от неговите оптични изомери има горчив вкус.
Сега погледнете друг пример, молекулата на фруктозата:
OH O H OH OH OH
│ ║ │ │ │ │
H C ─ C ─ ° С ─ ° С ─ ° С ─ C ─ H
│ │ │ │ │
H OH H H H
Фруктозата има три асиметрични въглеродни атома, следователно, имаме 8 оптично активни изомера и 4 оптично неактивни изомера, които са 4 рацемични смеси.
- Оптично активни изомери: 2не = 23 = 8;
- Оптично неактивни изомери: 2не = 23 = 4.
2 2
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/isomeros-moleculas-com-carbonos-assimetricos-diferentes.htm

