Колкото по-висока е температурата, толкова по-голяма е скоростта на реакцията.
Това може лесно да се види в много ситуации от нашето ежедневие, както в следните примери:
- Когато искаме да забавим реакцията на разлагане на храната, понижаваме температурата, като я поставяме в хладилника;

- Ако искаме да ускорим реакцията на готвене на храната, просто я поставете в тенджера за готвене. налягане, което с увеличаване на налягането увеличава и температурата на кипене на течната вода, в която храната е;

- По принцип пожарите обикновено са опустошителни, тъй като температурата на околната среда се повишава, което води до увеличаване на скоростта на реакцията на горене;
- За забавяне на метаболитните химични процеси, намалявайки шансовете за увреждане на мозъка поради недостиг на кислород, някои операции се извършват чрез понижаване на телесната температура на пациента, достигайки наоколо 15 ° С;
- Ако поставим ефервесцентна таблетка в чаша гореща вода и друга в чаша студена вода, първата ще се разтвори много по-бързо.
Но какво обяснява пряко пропорционалното влияние на температурата върху скоростта на реакцията?
Това е така, както е обяснено в текста „Условия за възникване на химични реакции”, За да протече реакцията, е необходимо да се удовлетворят някои условия, като например частиците те трябва да се сблъскат ефективно и с минималната необходима енергия, която се нарича енергия на активиране.
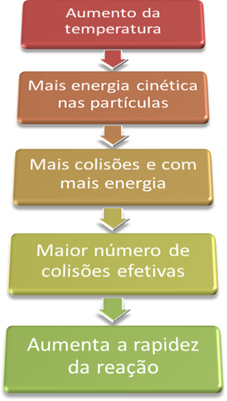
По този начин, когато повишаваме температурата на системата, ние също увеличаваме разбъркването на реагиращите частици и им осигуряваме повече кинетична енергия. С това ще се получат повече сблъсъци и с повече енергия, увеличавайки количеството частици, които ще реагират и, следователно, увеличавайки скоростта на реакцията.
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/temperatura-velocidade-das-reacoes.htm


