THE титруване е лабораторна процедура, използвана за определяне на концентрацията в количеството вещество (или концентрация в mol/L) на разтвор, съдържащ киселина или основа.
По време на титруването винаги има a смес от разтвори, съдържащи различни разтворени вещества с протичане на химична реакция. Тъй като смесените разтвори винаги имат киселина и основа, следователно протичащата химична реакция е а неутрализация.
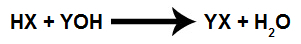
Химическо уравнение, представляващо титруване.
Процесът за определяне на моларната концентрация на неизвестен разтвор по време на титруване зависи от следните фактори:
• Познайте моларната концентрация на разтвора, който ще бъде смесен с неизвестното;
• Познаване на обема на разтвора с неизвестна концентрация;
• Познайте обема на разтвора с известна концентрация.
Формула, използвана при титруване
И в титруване настъпва неутрализация (равен брой молове киселина и основа), можем да използваме следната формула, за да определим моларната концентрация на неизвестния разтвор:
неВ = nБ
МВ.VВ = МБ.VБ
Забележка: Броят на моловете е произведението между моларната концентрация (M) и обема на разтвора (V).
Оборудване, необходимо за изпълнение на степен
• Бюрета: оборудване, използвано за измерване на обема на разтвора с известна концентрация;

• Ерленмайер: оборудване, използвано за получаване на разтвор с неизвестна концентрация;
• Универсална опора: оборудване, към което е фиксиран нокът;

• Нокът: оборудване, използвано за задържане на бюретата;

• Магнитна бъркалка: оборудване, използвано за разбъркване на разтвора, намиращ се в ерленмайеровата колба.

Стъпки на степен
-
1-ви етап: фиксирайте бюретата към универсалната опора с помощта на нокътя;
-
2-ри етап: поставете ерленмайеровата колба върху магнитната бъркалка;
-
3-ти етап: добавете определен обем вътре в колбата на Ерленмайер от разтвора с неизвестна концентрация. Например: добавете 10 mL от разтвора към Ерленмайерова колба;
- 4-ти етап: добавете фенолфталеин към разтвора в ерленмайеровата колба.
Забележка: Ако разтворът в ерленмайеровата колба е кисел, при добавяне на фенолфталеина разтворът ще остане непроменен на цвят, но ако разтворът е основен, той ще бъде розов червеникав.

Фенолфталеин, добавен към основен характерен разтвор.
-
5-ти етап: добавете магнитна лента вътре в колбата на Ерленмайер. След това включете магнитната бъркалка, така че течността вътре в Ерленмайера да се разбърква;
-
6-ти етап: добавете вътре в бюретата, до максималния й капацитет, обем от разтвор с известна концентрация, тоест ако бюретата е 50 mL, добавете 50 mL от този разтвор.
- 7-ма стъпка: отворете клапана на бюретата и оставете течността от вътрешността му да попадне в колбата на Ерленмайер.
Наблюдения, направени по време на титруването
Веднага след като бюретата се отвори върху колбата на Ерленмайер, започва реакцията на неутрализация, тоест киселината реагира с основата, като постепенно се образува сол и вода.
Тъй като реакцията на неутрализация протича със сместа, цветът на разтвора, присъстващ в Ерленмайер също се променя постепенно, което наричаме повратна точка, както следва:
- Ако беше безцветен, започва да изглежда розовочервеникав,
- ако бешерозовочервеникав, започва да става безцветен.
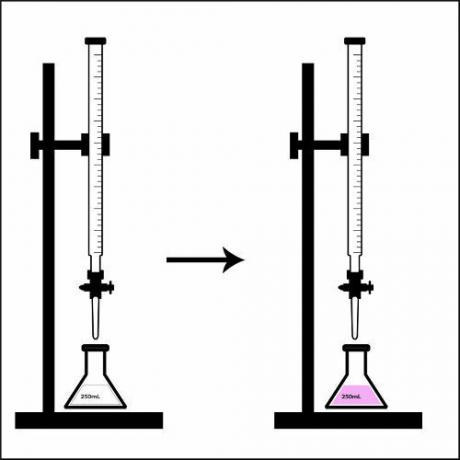
Представяне на повратната точка при титруване.
Когато разтворът, намиращ се в ерленмайеровата колба, напълно промени цвета си, тоест достигнал е повратната точка, казваме, че титруването е приключило. В този момент просто проверете използвания обем на разтвора с известна концентрация, който е бил там на бюретата.
От сумата между обема на разтвора с известна концентрация, който е определен в бюретата, и обем на неизвестния разтвор, който е ерленмайеровата колба, ние сме в състояние да определим неговата концентрация моларен.
От мен Диого Лопес Диаш
Източник: Бразилско училище - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-titulacao.htm



