В реакции на хидратация в алкадиени те са реакции на добавяне, тоест компонентите (хидроний и хидроксид) на водната молекула се добавят към алкадиен.
Вие алкадиени са въглеводороди, които имат отворена верига и две двойни връзки (образувани от сигма и пи) между въглеродните атоми, както можем да видим в следната структура:

Структурна формула на алкадиен
за реакция на хидратация в алкадиени е от съществено значение връзката pi, присъстваща в двойната връзка, да се разруши от въздействието на топлина и сярна киселина (H2САМО4). С разкъсването на връзката pi се появяват две места на свързване, всяка върху един от въглеродите, участващи в двойната връзка.

Поява на места за свързване с нарушаване на свързването на pi
Появата на места за свързване на молекулата алкадиен е необходима за йоните (H+ и о-) от водата се добавят към алкадиена, образувайки например алкохол (алкохол с два хидроксила).
Добавяне на H+ и о- в структурата на алкадиен
ЗАБЕЛЕЖКА: Добавянето на H+ и о- в структурата на алкадиените следва
Правилото на Марковников, т.е. H+ свързва се с най-хидрогенирания въглерод и ОН- се свързва с по-малко хидрогенирания въглерод.
Пример за приложението на правилото на Марковников при хидратацията на алкадиени
Тъй като има различни видове алкадиени по отношение на положението на двойните връзки, може да се окаже, че хидратацията на алкадиен образува различни съединения. Вижте следните случаи:
→ Натрупан или кондензиран алкадиен
Това е алкадиен, който има две двойни връзки, включващи едновременно три атома въглерод, тоест няма единична връзка, разделяща въглеродите, участващи в връзките удвоява.

Структурна формула на натрупан алкадиен
По време на реакцията на хидратация на редуващ се алкадиен, pi връзките се прекъсват, представлявайки Н+ добавени към по-хидрогенираните въглероди и ОН- добавя се към по-малко хидрогенирани въглероди:
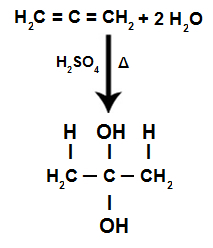
Натрупано уравнение за реакция на хидратация на алкадиен
Имаме, че при хидратацията на натрупания алкадиен, един и същ въглероден атом получава двата хидроксила, образувайки близнак алкохол, който е нестабилна структура.

Структура на близнака, образуван алкохол
Тъй като двойният алкохол е нестабилен, имаме образуване на водна молекула с компонентите на двата хидроксила и създаване на пи-връзка между въглерод и кислород.

Образуване на кетон от алкохол-близнак
Следователно, реакцията на хидратация на натрупаните алкадиени ще доведе до образуването на а кетон.
→ Конюгиран или алтернативен алкадиен
Това е алкадиен, който има две двойни връзки, включващи едновременно четири въглеродни атоми, т.е. има единична връзка, разделяща въглеродите, участващи в връзките удвоява.
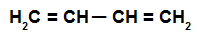
Структурна формула на редуващ се алкадиен
При редуващи се алкадиени възниква резонансът на техните двойни връзки. По този начин електроните на връзката pi променят позицията си (червени стрелки), както е показано на следната диаграма:
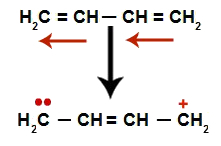
Диаграма, изобразяваща резонанса в променлив алкадиен
Като цяло имаме поява на двойна връзка точно между въглеродите, където преди това са били двете двойни създаването на две места за свързване, по един на всеки въглерод, който вече не създава двойната връзка (в примера въглерод 1 и 4). Въглеродните 1 и 4 от веригата получават Н+ и о- от водата.

Частична хидратация при редуване на алкадиен
След резонанса връзката pi на новата двойна връзка се прекъсва и се получава H+ и о- се добавят към молекулата алкадиен. OH се добавя към въглерода, най-близък до първата добавена OH група, тъй като претърпява електронното привличане на групата, която е по-електроотрицателна.

Прекратяване на хидратацията в редуващ се алкадиен
Поради резонанса казваме, че редуващият се алкадиен е претърпял 1,4 хидратация, образувайки диалкохол.
→ Alkadiene изолиран
Това е алкадиен, който има две двойни връзки, включващи най-малко пет атома едновременно. въглерод, тоест има поне две единични връзки, разделящи въглеродите, участващи в връзките. удвоява.

Структурна формула на изолиран алкадиен
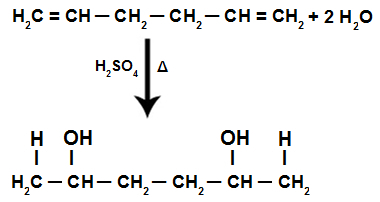
По време на реакцията на хидратация на изолиран алкадиен, пи връзките се разкъсват, Н+ добавени към по-хидрогенираните въглероди и ОН- добавени към по-малко хидрогенираните въглероди.

Изолирано уравнение за реакция на хидратация на алкадиен
Следователно, при добавянето на изолиран алкадиен имаме само образуването на диалкохол.
От мен Диого Лопес Диас
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/reacoes-hidratacao-alcadienos.htm


