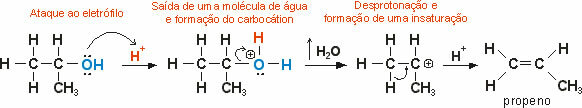
Нитрационните реакции са реакции на заместване, които протичат чрез азотна киселина (HNO3). Този тип реакция се проявява особено с алкани и с бензен и неговите производни, където един от водородните атоми, прикрепени към веригата или към ароматното ядро, се заменя с NO групата.2, като се получава нитросъединение и вода.
Вижте няколко примера:
1. Нитриране на алкан:
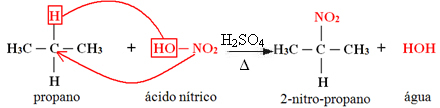
Когато алканът има повече от два въглерода, се образува смес от различни заместени съединения. Количеството на всяко получено съединение ще бъде пропорционално на следния ред на лекота, с който водородът се освобождава в молекулата:

В горния случай няма третичен въглерод, има само един вторичен и два първични; по този начин, най-голямото количество съединение, образувано като продукт, ще бъде 2-нитро-пропан.
Ако има достатъчно азотна киселина, друг водород може да бъде заменен от нитрогрупата, което води до 2-динитропропан (структура по-долу), съединение, широко използвано като добавка към дизеловото масло, повишаващо неговия октанов клас и намаляващо емисиите на сажди.
НА2
│
З.3C─C─CH3
│
НА2
2. Нитрация на бензен:
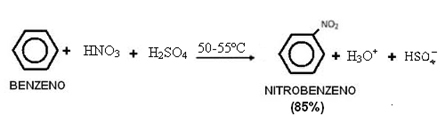
Имайте предвид, че тази реакция протича в присъствието на топлина, тъй като бензенът се нагрява със сулфанхидратна смес, т.е. концентрирана азотна киселина с концентрирана сярна киселина. Сярната киселина е катализатор, което води до увеличаване на скоростта на реакцията, тъй като бензенът бавно реагира с азотна киселина.
3. Нитриране на бензолни производни:
В такива случаи мястото на заместване ще зависи от заместителната група или функционалната група, прикрепена към ароматното ядро. Текстовете "Управляващи радикали в бензолния пръстен" и "Електронни ефекти на мета и орто-към-директори радикали”Обяснете повече за това как се случва.
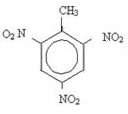
Ароматните пръстени могат да претърпят нитриране и да предизвикат експлозиви. Пример е тринитротолуен (2-метил-1,3,5-тринитробензен), по-известен като TNT и има няколко пигмента, използвани главно в тъканите.
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/reacoes-organicas-nitracao.htm