Вие оксиди те се състоят от два различни елемента, единият от които е кислород, който трябва да бъде най-електроотрицателният от двата.
Номенклатурата на неорганичните оксиди следва правила, които зависят от това дали оксидът е молекулярен, ковалентен или йонен. Нека разгледаме всеки случай:
* Номенклатура на молекулярни оксиди или ковалентна мрежа:
Молекулярни или ковалентни мрежови оксиди са онези, които имат кислород, прикрепен към a аметален, като въглерод (С), азот (N), сяра (S), флуор (F), наред с други. Номенклатурата на тези оксиди следва следното правило:

Правило за номенклатура за оксиди, образувани с метали
Префиксът моно пред свързания с кислород елемент не е задължителен.
Например имаме следния молекулен оксид: CO.
- Префикс, указващ количеството кислород: 1 кислород: моно;
- оксид на;
- Префикс, който показва броя на атомите на другия елемент: 1 въглерод: моно;
- Име на елемента, свързан с кислорода: въглерод.
И така, името ви е такова: CO = монокарбонов моноксид или въглероден окис.
Вижте още примери:
въглероден диоксид - CO2
Серен триоксид - SO3
Дихлоро хептоксид - Cl2О7
Азотен моноксид - N2О
Азотен триоксид - N2О3
Азотен моноксид -NO
Азотен диоксид - НЕ2
Азотен пентоксид - N2О5
Силициев диоксид - SiO2
Дифосфорен пентоксид - P2О5
Серен триоксид - SO3
* Номенклатура на йонни оксиди:
Йонните оксиди са онези, които имат кислород, свързан с а метал, като желязо (Fe), олово (Pb), натрий (Na), калций (Ca), сребро (Ag), наред с други. Обикновено електрическият заряд на кислорода е -2.
Посочената номенклатура за молекулни или ковалентни мрежови оксиди понастоящем се прилага и към металните оксиди и се счита за официална. Вижте няколко примера:
Железен моноксид - FeO
Оловен моноксид - PbO
Оловен диоксид - PbO2
Различен триоксид - Fe2О3
Съществува обаче специфична номенклатура за металните оксиди, която все още се използва широко. Тя се основава на валентността на елемента, свързан с кислорода.
Ако елементът има единична валентност, тоест, ако има само един начин да се свърже кислород и да се образува само един вид оксид, правилото за именуване ще бъде дадено от:

Правило за наименуване на едновалентни йонни оксиди
Примери:
- Натриев оксид - Na2О
- калциев оксид - CaO
- калиев оксид - K2О
- алуминиев оксид - Al2О3
- Сребърен оксид - Ag2О
Но има и йонни оксиди, образувани от елементи с повече от една валентност. В тези случаи правилото за именуване е както следва:
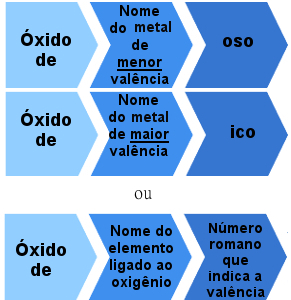
Правило за номенклатура за йонни оксиди с повече от една валентност
Примери:
Железен оксид - FeO
Железен оксид - Fe2О3
Меден оксид - Cu2О
меден оксид - CuO
Или:
Железен оксид II - FeO (железен нокс = +2)
Железен оксид III - Fe2О3 (Желязо nox = +3).
Меден оксид I - Cu2O (желязо nox = +1)
Меден оксид II - CuO (Iron nox = +2).
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/nomenclatura-dos-oxidos.htm

