НА йонизационна константа дава Вода(Kw), О водороден потенциал(pH) това е хидроксилионен потенциал (pOH) те са мерки важно за изчисления, включващи химичен баланс в киселинни и основни разтвори, както и при определяне на концентрацията на H йони+ и о- от въпросните решения.
Какво е Kw?
Йонният продукт на водата или Kw (това wозначава вода - вода, на английски), е константата, използвана за представяне на баланс, генериран от самойонизацията на водата. Дори и с много малка скорост, водата йонизира, произвеждайки H йони+ и о-, съгласно следното химическо уравнение:
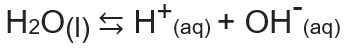
Анализирайки уравнението, осъзнаваме, че когато йонизация от молекула чиста вода се генерира Н йон.+ и OH йон-, това е концентрацията на тези йони винаги ще бъде еднаква. Дори когато има повишаване на температурата, което води до увеличаване на скоростта на йонизация, концентрациите остават същите.
Прочетете също:Йонизационна енергия
Не спирайте сега... Има още след рекламата;)
Въз основа на експериментални измервания се изчислява концентрацията на Н йони
+ и о- (в резултат на самойонизацията на водата) при 25 ° C и стойността на 1. 10-7 mol / L. Това е, от общо 1 милиард водни молекули, само два се подлагат на йонизация. Това показва, че чистата вода има ниска степен на йонизация и обяснява много ниската Електрическа проводимост чиста вода.Като се има предвид показаното по-горе, можем да напишем израз на константата на водния баланс:

Използване на стойности на концентрация на йони H+ и о- при 25 ° C, можем да изчислим стойността на Kw:
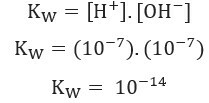
Както беше посочено по-рано, тази стойност на Кw се променя с повишаване на температурата, както е показано в таблицата по-долу:
T (° C) |
Кw |
10 |
0,29. 10-14 |
20 |
0,68. 10-14 |
25 |
1,00. 10-14 |
30 |
1,47. 10-14 |
40 |
2,92. 10-14 |
60 |
9,40. 10-14 |
За да научите повече за тази тема, прочетете нашия текст: Йонен воден продукт.
Какво е pH и pOH?

съкращението рН означава водороден потенциал и е създаден от датския биохимик Сорен Соренсен, през 1909 г., за да се улесни работата с концентрации на водородни йони [H+], които обикновено се изразяват в десетични числа. За да научите повече за тази тема, прочетете нашия текст: Какво е рН?
Този вид нотация показва съдържанието на H йони+ присъства в разтвора и се определя от математическия израз:
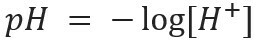
По същия начин можем да дефинираме pOH или хидроксилен потенциал, което ни казва Съдържание на OH йони- присъства в разтвора. Неговият математически израз е:
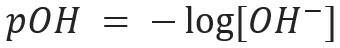
Във воден разтвор винаги ще има H йони+ и о- (поради йонизацията, понесена от водата), която ще се използва за характеризиране на разтвор в кисела или основен. Колкото повече H йони+ в разтвора има, толкова по-киселинно ще бъде. Следователно, присъствието на OH йони- в решението ще го направи по-основен. Ако има равновесие в количеството на тези йони, разтворът ще бъде класифициран като неутрален.
скала на pH
Скалата на pH се показва със стойности, вариращи от 0 до 14 (стойности, измерени при 25 ° C). Вижте скалата на pH на изображението по-долу:

Колкото по-ниско е рНна решението,по-голяма е неговата киселинност, и колкото по-близо до края на скалата, тоест по-близо до 14, толкова по-голям е нейният основен характер. Например, лимоновият сок има рН 2, докато белините имат рН 12.
Как да се изчисли pH и pOH
познавайки концентрация на йони, ние можем изчислете стойностите на рН и pOH на разтворите и, като знаем потенциалните стойности, изчисляваме концентрация на йони в разтвори. За целта се използват следните изрази:
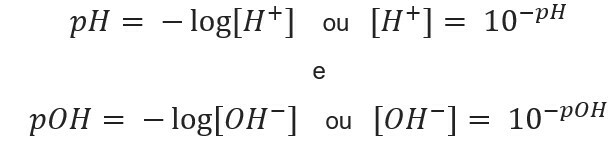
Нека да преминем към примерите:
Пример 1
Ако искаме да знаем рН на разтвор с [H+] = 0,001 mol / L, просто използвайте формулата, представена по-рано:
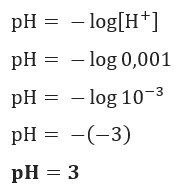
Пример 2
Сега, за да разберете каква е концентрацията на OH- на решение с pOH = 5, просто заменете стойността в следната формула:

Ако приложим една и съща скала на потенциалите за йонния баланс на водата, ще имаме:
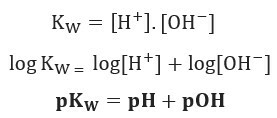
Както беше посочено, при 25 ° C, Kw = 10-14. Следователно:

С това можем да изчислим pOH на разтвор въз основа на неговото pH. Ако имаме разтвор с рН 3, тогава pOH ще бъде 11.
Знам повече: Неутрални, киселинни и основни среди
решени упражнения
Въпрос 1 (UEFS-BA) Концентрацията на OH йони–(тук) в даден разтвор на амониев хидроксид, при 25 ° C, е равно на 1.10–3 mol / L. POH на това решение е:
а) 0
б) 1
в) 3
г) 11
д) 13
Резолюция: Буква В. Ако имаме [OH–] = 10–3 mol / L, така че вашият pOH ще бъде равен на 3.
Виж:
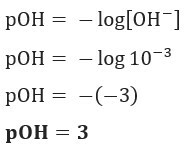
Въпрос 2 (UEA-AM) Обмислете следната информация, получена от етикета за минерална вода в град Порто Сегуро (BA):
нитрат 1,45 mg / L
рН при 25 ° C 4.51
Тази минерална вода е
а) киселинен и има [Н+] –].
б) киселинен и има [Н+]> [ОХ–].
в) неутрален и има [H+] = [ОН–].
г) основен и има [H+]> [ОХ–].
д) основен и има [H+] –].
Резолюция: Буква Б. Тъй като рН на минералната вода, посочена на етикета, е по-малко от 7, можем да кажем, че тя е киселинен разтвор и следователно концентрацията на H йони+ е по-голям от OH-.
Въпрос 3 (UEA-AM) Един от начините за бързо получаване на газообразен водород в лабораторията е чрез взаимодействие на прахообразен метален цинк със солна киселина (HCl), при концентрация 1,0 mol / L:
Zn (s) + 2 HCl (aq) → ZnCl2 (aq) + Н2 (ж)
Като се има предвид, че солната киселина е 100% йонизирана и че разтворът е при 25 ° C, правилно е да се твърди, че рН на разтвора на солната киселина, споменат в текста, е
- 0
- 1
- 3
- 13
- 14
Резолюция:Буква а. Можем да изчислим pH на разтвора, като използваме концентрацията на HCl, посочена в текста, тъй като, тъй като тя е 100% йонизирана, концентрацията на [H+] ще бъде същото, тъй като за всяка йонизирана молекула на НС1, по един Н йон+ ще се генерира. Следователно:
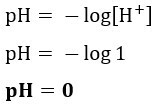
От Виктор Ферейра
Учител по химия