Полимеризация е името на химичния процес, който води до образуването на макромолекули (големи молекули), наречени полимери, чрез комбинацията от по-малки молекули, мономерите.
реакцията на полимеризация той е много разпространен в природата, както виждаме във въглехидратите (като нишесте) и протеините (като казеин в млякото). Това се случва и синтетично, тъй като по-голямата част от полимерите, използвани от хората в ежедневието им, са направени изкуствено.
Първият полимер, произведен от полимеризация синтетичен е бакелит, през 1909 г., от белгийския химик Лео Хендрик Бекеланд.
По принцип, за мономер да се комбинира с друг (независимо дали са еднакви или различни) в реакция на полимеризация, необходимо е съществуването на свободна валентност (химическа връзка, която трябва да се осъществи) и в двата мономера.
Тези валентности възникват в резултат на скъсване на връзките, чрез използване на катализатори (като никел), външни условия като светлина и топлина или от явлението резонанс в структурата (изместване на електроните).
При образуването на полипропилен (PP полимер), например използван в домакински съдове и играчки, pi връзка (π) във всяка молекула се разделя, както следва:
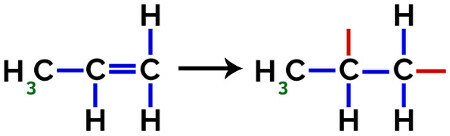
Счупване на pi връзка в пропилен
По този начин всеки пропиленов мономер може да се свърже с два други пропиленови мономера и да образува полимера РР или полипропилена (префиксът поли показва няколко мономерни единици). Най-честият начин за представяне на полимер е мономерът между скобите и отвън буквата n, която показва няколко мономера, както можем да видим в случая на полимера PP:
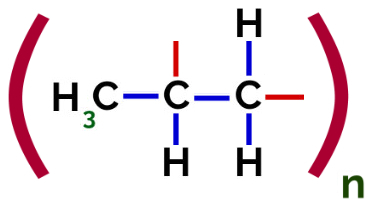
Представяне на полипропилен полимер
реакцията на полимеризация може да се направи по различни начини, както ще видим по-долу:
а) Реакция на допълнителна полимеризация
В това полимеризация, винаги има прекъсване на pi връзка в мономера, което кара две свободни валенции да се появят в структурата, както при образуването на полиетилен, полимер, широко използван във фармацевтичната опаковка.
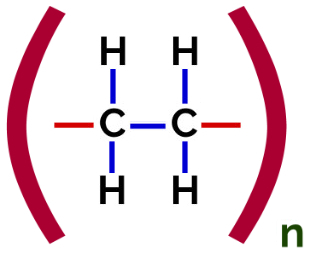
Добавка на полиетилен Полимерна структурна формула
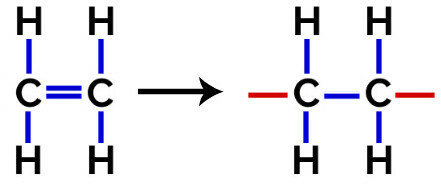
В полимеризация от полиетилен, молекулите на етилен (етен) се използват като мономер, който има pi връзка между двата въглеродни атома. Когато тази връзка се прекъсне, се появяват две свободни валенции, по една на всеки въглероден атом, който е участвал в pi връзката. Мономерите се обединяват точно във всяка от тези валентности, тоест валентността на едната е свързана с валентността на другата и т.н.
Не спирайте сега... Има още след рекламата;)
Уравнение за образуване на полиетилен
б) Реакция на добавена полимеризация 1.4
При тази полимеризация мономерите представят две редуващи се двойни връзки (една pi и една сигма), което благоприятства явлението на резонанса (редуващо се положението на pi електроните на pi връзката), както при образуването на синтетичен каучук (полибутадиен)

Структурна формула на полибутадиен
Мономерната единица на този полимер е бутадиен, който има две редуващи се двойни връзки. С резонанс структурата има двойна връзка между въглероди 2 и 3 и две свободни валенции на въглероди 1 и 4. Именно в тези свободни валентности на въглерод 1 и 4 мономерите се комбинират.

Резонанс в бутадиен
в) Реакция на кондензационна полимеризация или елиминиране
Това е реакция на полимеризация при които задължително два мономера (еднакви или различни) едновременно губят атоми или групи, което води до две свободни валентности във всеки един от тях. По този начин винаги има елиминиране на водород от мономер, който след това се присъединява към халоген (F, Cl, Br, I), OH, NH2или към CN на другия мономер.
И така, в полимеризация чрез елиминиране винаги има образуване на вода, халогенирана киселина (HCl, HI, HF, HBr), амоняк (NH3) или циановодородна киселина (HCN) в допълнение към полимера. Вижте например представянето на образуването на полиестер, материал, използван като плат:

Уравнение за образуване на полиестер
Полиестер-образуващи мономери са р-бензендиоена киселина и етан-1,2-диол. Това можем да видим в това полимеризация елиминирането на водните молекули се случва, тъй като двата мономера имат два хидроксила. В този процес киселината губи двата хидроксила, а алкохолът губи само водорода от своите хидроксили:

Полиестерна структура
Полиестерните мономери се свързват с кислорода в алкохола и въглерода в карбоксилната киселина.
От мен Диого Лопес Диас