Вие Въглеводороди са съставени образувани от въглерод (С) и водород (Н). Гъвкавостта на въглерода, който е основният елемент на тези съединения, благоприятства съществуването на огромно разнообразие от структури Следователно някои свойства, като точка на топене и точка на кипене, могат да се различават между отделните въглеводороди.
Те са предимно молекули аполарен, с силас междумолекулни индуциран дипол тип и плътност по - малка от The от вода. Идентифицирането на тези съединения може да се извърши чрез номенклатурата, която следва правилата, установени от Международния съюз за чиста и приложна химия (Iupac).
Прочетете също: Въглеродът - един от най-разпространените елементи във Вселената
Свойства на въглеводородите

Полярност: въглеводороди без наличие на хетероатоми са аполарен.
Междумолекулни сили: връзките между молекулите на въглеводорода са от типа индуциран дипол.
точка на топене и икипене: те варират в зависимост от размера, функцията и структурната организация на молекулата.
физическо състояние: при нормални условия на температура и налягане въглеводородите с четири или по-малко въглеродни атома са в газообразно състояние. Тези с 5 до 17 въглерода са в течно състояние, а въглеводородите с повече от 17 въглерода са твърди вещества.
Плътност: е по-малък от плътност вода, т.е. по-малко от 1,0 g / cm³.
Реактивност: алифатните и ненаситените въглеводороди са слабо реактивни; ненаситените съединения са по-склонни да реагират с други молекули, а цикличните въглеводороди с до пет въглерода са много реактивни.
Класификация на въглеводородите
Въглеводородите могат да бъдат класифицирани по структурна организация на веригата и от заведенията.Ненаситеност е наличието на двойна (и) или тройна връзка между въглеродните атоми, е появата на връзки тип pi (π). вече клонове те са като „клонове“, прикрепени към по-голяма въглеводородна структура. Цикличните вериги също могат да съдържат разклонения и / или ненаситеност - структурната организация на затворените вериги въглеводороди образува многоъгълници като квадрат, триъгълник, хексан и др.
Що се отнася до подреждането на атомите, въглеводородът може да има нормална или разклонена верига.
→ С въглеводороднормална, линейна или права линия: този с низ, който има само два края.

→ С въглеводородмрази разклонени: тази с верига, която има повече от два края. За да знаете къде и какви са клоновете, е важно да изберете правилно главната верига. Основната верига трябва да съдържа всички ненаситени и хетероатоми (ако има такива), както и най-голям брой последователни въглероди. Въглеродите, които не се съдържат в основната верига, са клонове.
Пример:

По отношение на неговото "затваряне", въглеводородът може да има затворена, отворена или смесена верига.
→ Верижни въглеводородис затворено или циклично: тези с вериги, в които атомите се организират, образувайки цикъл, многоъгълник или ароматен пръстен (затворен въглеводород с редуващи се ненаситености). Нямате свободни краища, освен ако няма клон. Всеки връх на полигона представлява въглерод и съответните водородни свързващи агенти.
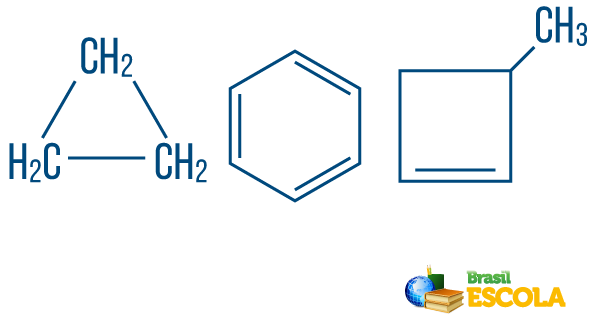
→ Отворени вериги или ациклични въглеводороди: са тези с вериги, които имат поне два края.

→ Въглеводород на низ от смесен тип: е образуван от пръстен или циклична верига, прикрепена към линейна част; има поне един край.
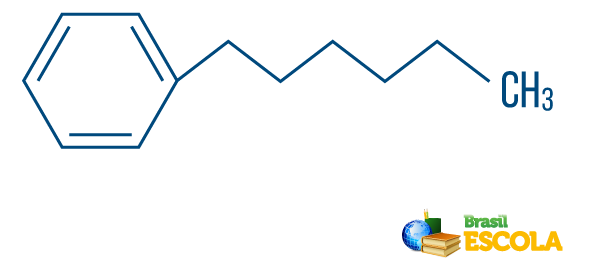
Прочетете също: Ароматни въглеводороди - примери и свойства
Номенклатура на въглеводородите
За всеки вид въглеводород има правило за именуване, установено от Iupac. Номенклатурата на тези съединения се прави, както следва:
1-ва част: местоположение и име на клонове (ако има такива);
2-ра част: терминът се прилага цикъл ако съединението е затворена верига, но ако е алифатна (отворена) верига, няма да е необходимо;
3-та част: префикс, указващ колко въглероди има в основната верига;
4-та част: местоположение и инфикс, указващи вида на ненаситеността в молекулата;
5-та част: суфикс „o”, подходящ за въглеводороди.
Ако молекулата има отворена структура, без разклоняване, номенклатурата ще започне в част 3.
Следващата таблица показва необходимата информация (префикс, инфикс и суфикс) за въглеводородната номенклатура като цяло. О префикс варира в зависимост от броя на въглеродните атоми; О инфикс, според броя на ненасищанията; това е наставка“О " се отнася до съединения от въглеводороден тип.
Префикс |
Infix |
Наставка |
||
1 въглерод |
срещнал- |
Само единични разговори |
-ан- |
-О |
2 въглерода |
и т.н. |
|||
3 въглерода |
опора |
1 двойна връзка |
-ен- |
|
4 въглерода |
но- |
|||
5 въглерода |
пент |
2 двойни връзки |
-диен- |
|
6 въглерода |
шестнадесетичен |
|||
7 въглерода |
hept- |
1 тройна връзка |
-в- |
|
8 въглерода |
окт- |
|||
9 въглерода |
не- |
2 тройни връзки |
-диин- |
|
10 въглерода |
дек- |
Първата стъпка в откриването на номенклатурата на органично съединение е идентифицирайте основната верига на въглеродните атоми, които трябва да съдържат ненаситени и възможно най-много последователни въглеродни атоми. След идентифициране на основната верига, въглеродите трябва да бъдат изброени - започване на преброяването от страната, която е най-близо до клоните и ненасищанията (ако има такива). НА локализация ще бъде номерът на въглерода, където се намира разклонението или ненаситеността. Понякога има само едно възможно място за радикална или двойна или тройна връзка, така че не е необходимо да се изразява местоположението на свързващия въглерод в номенклатурата.

НА номенклатура за клонове ще бъде дадено от броя на въглеродните атоми във всеки, плюс терминирането линия или ll. Когато има повече от един клон, се използва азбучен ред.
Вижте примерите по-долу:
→ Пример 1
CH3 - СН2 - СН3 → Пропан
1-ва част: префиксът „опора”Показва, че веригата има три въглерода.
2-ра част: инфиксът "-ан-”Сигнализира, че молекулата прави само връзки от типа сигма или просто.
3-та част: суфиксът "-О”Е характерно за въглеводородите.
→ Пример 2
CH2= СН-СН2-CH3 → Но-1-ен
При въглеводороди с ненаситеност е необходимо да се номерира и локализира въглеродът, в който се намира двойката, и номерирането трябва да бъде възможно най-малко. За това броят на въглерода трябва да започне от страната, която е най-близо до двойната връзка.
1-ва част: "но-" показва, че във веригата има четири въглерода.
2-ра част: "1-bg" се отнася до ненаситеност, разположена между въглерод 1 и 2.
3-та част: "-O" е характерната суфикс на въглеводороди.
→ Пример 3

1-ва част: "3-етил" сигнализира, че има въглероден клон на въглерод 2.
2-ра част: "-пент-" показва наличието на пет въглерода в основната верига.
3-та част: "-an-" е инфиксът, приложен към ненаситени вериги (без двойни или тройни връзки).
4-та част: "-O" е характерната суфикс на въглеводороди.
→ Пример 4
За вериги с повече от един клон, поставете радикалите в номенклатурата по азбучен ред. Ако в една и съща молекула има разклонения и ненаситеност, броят на въглеродите в основната верига трябва да бъде направен по такъв начин, че сборът от цифрите на местоположението да е възможно най-малък.
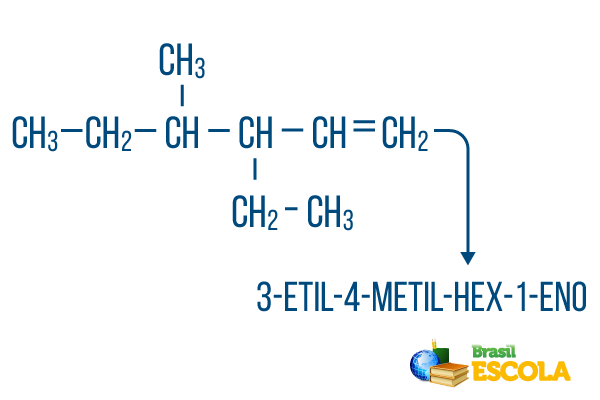
Броят на въглерода в основната верига се извършва отляво надясно, а сумата от цифрите за ненаситеност и местоположение на клона е: 1 + 4 + 3 = 8. Ако броят на въглерода беше отдясно наляво, съставната номенклатура щеше да бъде 4-етил-3-метил-5-ен, чийто сбор от местоположения би бил: 4 + 3 + 5 = 12, което е по-голямо от другата хипотеза, така че не трябва да се използва.
1-ва част: 3-етил-4-метил прави препратка към радикалите по азбучен ред и съответните им местоположения.
2-ра част: шестнадесетичен означава, че в основната верига има 6 въглерода.
3-та част: 1-бр показва наличието на двойна връзка върху въглерод 1.
4-та част: "-O" е характерната суфикс на въглеводороди.
→ Пример 5
За затворени низове важат правилата за именуване, но думата цикъл започва името на съединението, което показва, че е затворен или цикличен въглеводород.
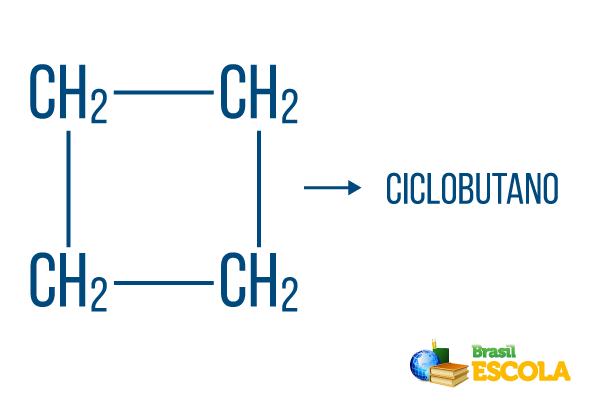
1-ва част: цикъл- показва, че е затворен низ.
2-ра част: -но- обозначава съществуването на 4 въглерода във веригата
3-та част: -Ое характерната суфикс на въглеводороди.
Прочетете също: Класификация на въглеродните вериги
Видове въглеводороди
Въглеводородите могат да бъдат разделени на алкани, алкени, алкини и алкадиени - които се класифицират като според установяването на веригата (двойни (и) или тройни връзки) - и циклани, които са веригите затворен.
→ Алкани: са въглеводороди, които нямат ненаситеност. Общата формула за алкани е СнеЗ.2n + 2, и незнамение съставен е от префикс + an + О.
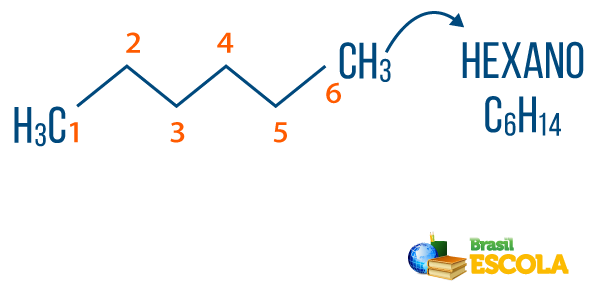
Вие алкани може да се намери в природата, като газ метан (СН4), който се освобождава от животни и се произвежда в процесите на разлагане, както и в рафинериите и нефтохимическата промишленост. Съединения като пропан (° С3З.7), бутан (° С4З.10), който съставлява нашия газ за готвене (LPG), и октан (° С8З.18), присъстващи в автомобилното гориво, са странични продукти от Нефт.

→ алкени или алкени: са въглеродни вериги, които имат ненаситеност, двойна връзка. Общата му формула е CнеЗ.2н, а твоя? И твоя незнамение съставен е от Pпоправка + en + o.

О етиленов газ (° С2З.4), използван в земеделието за ускоряване на узряването на плодовете, принадлежи към функцията алкен. Съединението се използва и в производството на суровини полиетилен, използвани в производството на пластмасови съдове.
→ Алкини или ацетиленова: въглеводороди с тройна връзка. Общата му формула е CнеЗ.2n - 2. НА номенклатура съставен е от префикс + в + o.

О ацетилен или етин (С2З.2) е газ от алкиновата функция, използван в заварки и метални прорези. Това съединение може да достигне температури до 3000 ° C, което позволява извършването на ремонти на потопени части на кораб.

→ алкадиени или диени: въглеродни вериги с две ненаситени, т.е. две двойни връзки между въглеродните атоми. Общата формула за тази функция е C.неЗ.2n - 2. Осъзнайте, че това е същата формула като алкините, което означава, че може да се случи изомерия между съединения (една и съща молекулна формула за различни съединения).
Номенклатурата на алкадиена се състои от Pпоправка + dien + o.
Пример:

→ Въглеводороди със затворена верига: молекулите се организират по цикличен начин, са склонни да образуват многоъгълник и, както при отворените вериги, могат да възникнат заведения и / или разклонения. Циклоните, циклите, циклините и бензолите са въглеводороди със затворена верига.
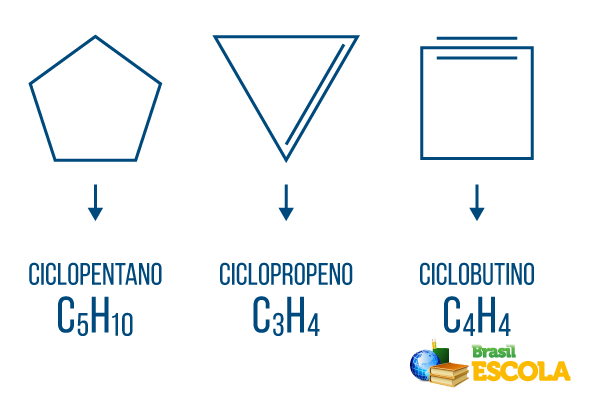
Циклони или циклоалкани: циклични вериги, състоящи се само от единични връзки. Общата му формула е CнеЗ.2н. Номенклатура: ciclo + префикс + an + o.
Цикли или циклоалкени: затворени въглеводородни вериги със заведение. Общата му формула е CнеЗ.2n-2. Номенклатура: ° Сiclo + префикс + en + О.
-
Циклини или циклоалкини: затворени вериги въглеводороди с наличието на две двойни връзки. Общата му формула е CнеЗ.2n-4. Номенклатура: ° Сiclo + префикс + в + o.
бензоли
Бензен е вид затворена верига въглеводород с шест въглерода където връзките варират между единични и двойни. Тези съединения са токсичен и силно канцерогенни, като се използват като органични разтворители в химични процеси.
За да се счита въглеводородът за ароматен, трябва да има поне един бензенов пръстен, който е силно реактивен, следователно подлежи на две или повече заместители, което ще видим тук като последици. Когато има два свързващи радикала, ще имаме конкретни имена за всяка двойка позиции.
Радиали на 1,2 въглерода бензен → орто
Радикали при 1,3 въглерода на бензола → цел
Радиали върху въглерод 1,4 бензен → за
Аноменклатурата на ароматно съединение се извършва, както следва:
1-ва част: позициониране на лигандите (орто, цел или да).
2-ра част: име на радикала или радикалите, прикрепени към бензола (метил, етил, пропил ...). Името, дадено на радикали, следва правилото на другите въглеводороди.
- 3-та част: -Б.отрова, което е характерният термин за ароматни въглеводороди.
Примери:
→ Орто-диметил-бензен

1-ва част: Оrto- показва, че радикалите са разположени върху въглероди 1 и 2.
2-ра част: -диметил- се отнася до двата радикала, и двата с един въглерод.
3-та част: -бензен е характерният термин за ароматни въглеводороди.
→ Орто-етил-метил-бензен
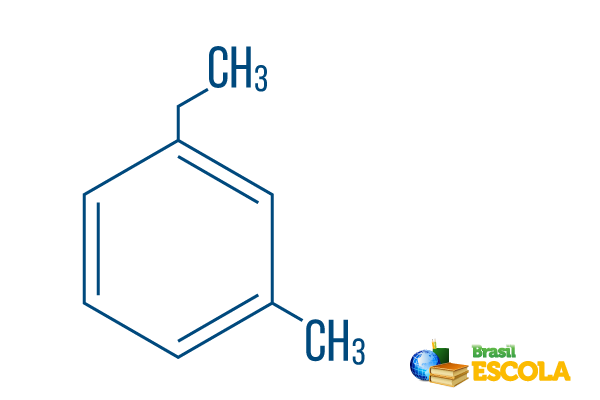
1-ва част: мо- показва, че радикалите са разположени върху въглерод 1 и 3.
2-ра част: етил-метил- се отнася до количеството въглерод във всеки радикал етил The двувъглероден клон и метил разклоняване с един въглерод - поставен в номенклатурата по азбучен ред.
3-та част: -бензен е характерният термин за ароматни въглеводороди.
→ Пара-диетил-бензен
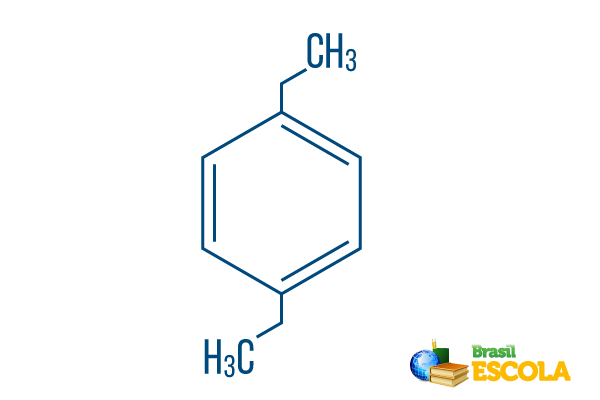
1-ва част: Pрало- показва, че радикалите са върху въглероди 1 и 4 на бензола.
2-ра част: -диетилов- прави препратка към два радикала от този тип етил, т.е. два клона с по два въглерода всеки.
3-та част: -бензен е характерният термин за ароматни въглеводороди.
Прочетете също:Откриване на структурата на бензола
решени упражнения
(Unesp) - Октанът е една от основните съставки на бензина, който е смес от въглеводороди. Молекулната формула на октана е:
а) C8H18
б) C8H16
в) C8H14
г) С12Н24
д) C18H38
Отговор: буква а). Анализиране на съставната номенклатура октан, това е алкан, т.е. молекула, състояща се само от единични връзки. Ако общата формула за алкани е CнеЗ.2n + 2, замествайки „n“ с осем, което е количеството въглерод в основната верига - и уникално в този случай -, ще имаме, че молекулната формула на октана е C8H18.
(UFSCar-SP) - Обмислете следните твърдения за въглеводородите.
I) Въглеводородите са органични съединения, състоящи се само от въглерод и водород.
II) Само ненаситени въглеводороди с права верига се наричат алкени.
III) Циклоалканите са наситени алифатни въглеводороди с обща формула CnH2n.
IV) Представляват ароматни въглеводороди: бромобензен, р-нитротолуен и нафтален.
Следните твърдения са верни:
а) само I и III.
б) само I, III и IV.
в) само II и III.
г) само III и IV.
д) само I, II и IV.
Отговор: Буква а).
II - Алкените са съединения с двойна връзка, т.е. ненаситени, но те могат да имат разклонения във веригата си, като не са изключително линейни.
IV - Брометобензен и р-нитротолуенови съединения принадлежат към други органични функции.
от Лайса Бернардес
Учител по химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/hidrocarbonetos.htm



