Батерия е устройство, в което електрически ток се произвежда от химическа енергия, идваща от реакция на оксидоредукция, тоест един вид реагент губи електрони (окисление), докато друг вид получава електрони (редукция).
Вижте изображенията на реакциите на окисление и редукция, които се случват във всеки стек:
Окисление: X → и + X+
Вид X губи електрон и се превръща в катион.
Намаление: Y.- + и → Y
анионът Y- получава електрон и се трансформира в неутрален Y вид.
Основни компоненти на стека
Основните компоненти на стека са:
Анод: отрицателен електрод, в който протича реакцията на окисление, тоест загуба на електрони;
Катод: положителен електрод, в който протича редукционната реакция, тоест електронно усилване;
Електролитичен разтвор (солен мост) или проводящ материал (като графитна лента): е начинът, чрез който електроните, отдадени от анода, достигат до катода.
Основи на това как работи батерията
Функционирането на стека възниква от следните събития:
1-ви принцип: Анодно окисление
Металът в анода, тъй като има по-голяма тенденция да губи електрони, се превръща в катион, както наблюдаваме в уравнението по-долу:
Zn → Zn2+ + 2 и
2-ри принцип: редукция на катода
Катионите, които са част от материала, присъстващ в катода (за пример ще използваме мед), при получаване електроните от анода се трансформират в метална мед, както можем да видим в уравнението по-долу:
Задник2+ + 2e → Cu
първи купчини
а) Батерията на Алесандро Волта
Купчината на Алесандро (първата купчина в историята), сглобена през 1800 г., е оформена от интеркалирани метални дискове, както е на изображението по-долу:

Сглобка, подобна на „Обратно към купчината“ на Алесандро
Дисковете бяха преплетени, защото имаха различен състав. Единият е направен от цинков метал, а другият е направен от мед, винаги отделен от памук, напоен със саламура (разтвор, образуван от вода и сол).
Б) Купчината на Даниел
Купчината на Даниел, сглобена през 1836 г., се състоеше от две полуклетки, свързани с проводящ проводник и солен мост.
Полуклетка 1: това беше анодът, тоест отрицателният полюс на батерията.
Той е съставен от цинкова плоча и част от тази плоча е потопена в разтвор, образуван от вода и цинков сулфат (ZnSO4).
Половинка клетка 2: това беше катодът, тоест положителният полюс на батерията.
Той е съставен от медна плоча и част от тази плоча е потопена в разтвор, образуван от вода и меден сулфат (CuSO4).
солен мост
U-образна тръба, която съдържа разтвор, образуван от вода и калиев хлорид (KCl), който свързва двете полуклетки (цинк и мед) и има стъклена вата в двата края.
батерии в момента
В момента има няколко модела на стекове, но като цяло те изглеждат така:
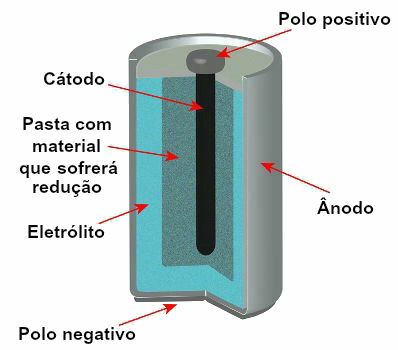
Схема, представяща модела на текущ стек
Най-използваните модели са така наречените Leclanché батерия и алкалната батерия, които имат следните разлики:
The) Лекланска купчина
Той има анод, образуван от метален цинк;
Той има катод, образуван от паста с амониев хлорид, вода, нишесте и манганов диоксид;
Той има графитна лента, която служи като проводник за електроните, които се отклоняват от катода към анода.
Б) Алкална батерия
Той има анод, образуван от метален цинк или кадмий;
Той има катод, образуван от живачен оксид, никелов оксид и йод;
Той трябва да има смесена основа в материала, който съставлява катода.
От мен Диого Лопес Диас
Източник: Бразилско училище - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-pilha.htm


