В текста "Как действат катализаторните вещества?”, Беше показано, че катализаторите са в състояние да увеличат скоростта на реакциите, тъй като намаляват енергията на активиране, необходима за възникването на реакцията. Те правят това чрез промяна на реакционния механизъм, комбиниране с реагентите и образуване на междинно съединение, което от своя страна се превръща в продукти и катализатор.
Извиква се един от начините това да се случи Хомогенна катализа, когато катализаторът образува еднофазна система с реагентите.
Това означава, че реагентите, продуктите и катализаторът трябва да са в една и съща фаза, т.е. в едно и също състояние.
Изследването на този вид катализа е важно за науката и индустрията, тъй като няколко важни реакции за производството могат да се ускорят с малки количества катализатори.
Пример за хомогенна катализа, използвана в промишлеността, е междинен етап в производството на сярна киселина (Н2САМО4 (aq)), при което се образува серен триоксид (SO3 (g)) чрез реакцията на горене на серен диоксид (SO2 (g)), показано по-долу:
2 ТАКА2 (g) + O2 (g) → 2 ОС3 (g)
Тази реакция протича твърде бавно, така че се добавя катализатор, азотен диоксид (NO).2 (g)). Този катализатор се комбинира със серен диоксид, за да образува междинно съединение (активиран комплекс), което е азотен моноксид (NO(ж)).
Не спирайте сега... Има още след рекламата;)
След това това междинно съединение реагира с кислороден газ (O2 (g)) за регенерация на катализатора. Вижте по-долу как се случва това и наблюдавайте как всички те са в газовата фаза, образувайки хомогенна среда:
катализаторактивиран комплекс
Стъпка 1: 2 OS2 (g) + 2 НЕ2 (g)→ 2 ОС3 (g) + 2 НЕ(ж)
Стъпка 2: 2 НЕ(ж)+ 1 O2 (g) → 2 НЕ2 (g)
Глобална реакция: 2 SO2 (g) + O2 (g) → 2 ОС3 (g)
Обърнете внимание, че катализаторът участва само в междинните етапи, но не се консумира. В края на реакцията той се възстановява напълно. Реакцията с този механизъм, направена в два етапа, изисква по-малко енергия за активиране и следователно тя протича по-бързо.
Графично представяне:
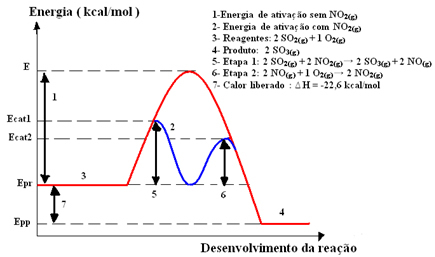
От Дженифър Фогаса
Завършва химия
Искате ли да се позовавате на този текст в училище или академична работа? Виж:
FOGAÇA, Дженифър Роча Варгас. "Хомогенна катализа"; Бразилско училище. Наличен в: https://brasilescola.uol.com.br/quimica/catalise-homogenea.htm. Достъп на 27 юни 2021 г.