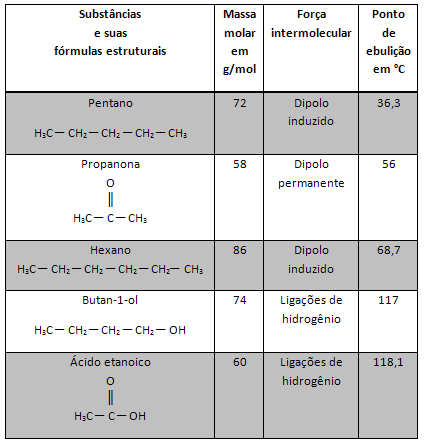
Изследването на силата на a киселина е много важно за определяне на способността на киселинния разтвор да провежда електрически ток, тъй като това се отнася до количеството йони, които това вещество произвежда при контакт с вода (йонизация). Когато една киселина е твърде силна, тя произвежда твърде много хидрониеви катиони (H3О+) и много аниони (X-). Вижте уравнението за йонизация на бромоводородната киселина:
HBr + H2O → H3О+ + Br-
При йонизиране водородът, присъстващ в молекулата на киселината, взаимодейства с молекулата на водата и образува хидроний. Но за да се случи това събитие, водородният атом трябва непременно да се йонизира. Йонизиращият се водород е този, способен да образува хидрониев катион.. За да разберем дали водородът може да се йонизира, ние вземаме предвид класификацията на киселината като хидрацидна (без кислород в състава си) или оксикиселина (има кислород в състава си).
а) Хидрациди
Целият водород в хидрацид се счита за йонизиращ се.
Примери:
- HCl: йонизиращ се водород, като по този начин се получава хидроний;
Не спирайте сега... Има още след рекламата;)
- З.2S: Два йонизируеми водорода, след което се получават два въглерода
б) Оксиацид
В оксикиселина, само водородът, който е свързан с кислороден атом в молекулата, се счита за йонизиращ се. За това е необходимо да се изгради неговата структурна формула. Вижте няколко примера:
З.3ПРАХ4 (фосфорна киселина)
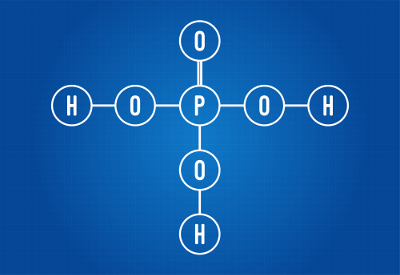
Структурна формула на фосфорната киселина
Виждаме, че в структурата на фосфорната киселина има три водорода, свързани с кислорода, така че има три йонизируеми водорода. Йонизационното уравнение ще бъде:
З.3ПРАХ4 + 3 Н2O → 3 H3О+ + PO4-3
З.2САМО4 (сярна киселина)
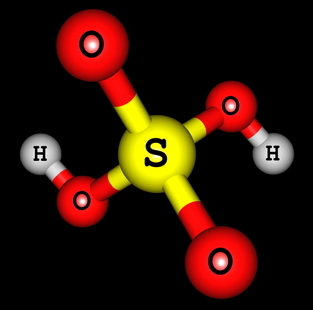
Структурна формула на сярна киселина
Виждаме, че в структурата на сярната киселина има два водорода, свързани към кислорода, така че има два йонизируеми водорода. Йонизационното уравнение ще бъде:
З.2САМО4 + 2 Н2O → 2 H3О+ + ОС4-2
От мен Диого Лопес Диас
Искате ли да се позовавате на този текст в училище или академична работа? Виж:
ДНИ, Диого Лопес. "Йонизиращи се водороди"; Бразилско училище. Наличен в: https://brasilescola.uol.com.br/quimica/hidrogenios-ionizaveis.htm. Достъп на 28 юни 2021 г.
Химия

Дисоциация и йонизация, италиански учен Волта, електрически ток, шведски физически химик Сван Август Арениус, Теория на Арениус, положителни йони, катиони, отрицателни йони, аниони, сода каустик, готварска сол, полярни молекули, дисоциация йонен,