Вие алдехиди и кетони те са много сходни органични функции. И двете имат в структурата си карбонилната функционална група (C = O), с единствената разлика, че в случая на алдехиди, той винаги се появява в края на въглеродната верига, т.е. един от карбонилните въглеродни лиганди е водород; кетоните имат карбонил между два други въглеродни атома.
Функционална група алдехиди:Функционална група кетони:
О О
║ ║
C C ─ H C C ─ C
Поради тази причина има случаи на функционална изомерия между алдехидите и кетоните. Например, по-долу представяме два функционални изомера, които имат еднаква молекулна формула (С3Н6O), но единият е алдехид (пропанал), а другият е кетон (пропанон). Вижте как това напълно променя техните свойства и приложения:
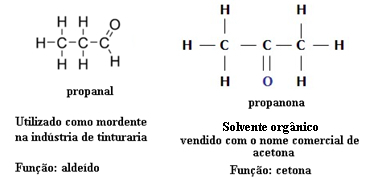
Пример за функционална изомерия между алдехид и кетон
Представете си, че сте в лаборатория и откривате флакон с безцветна течност, която има само молекулната формула С3Н6О. Какво бихте направили, за да разберете дали това е кетон или алдехид?
За да решавате проблеми като този,
съществуват методи за диференциране на алдехиди и кетони, базирани на реакцията на тези съединения срещу слаби окислители. Както е показано по-долу, когато са изправени пред слаби окислители, алдехидите реагират, като се окисляват, докато кетоните не реагират. Ние го казвамеалдехидите действат като редуциращи агенти, но кетоните не, те реагират само като редуциращи агенти в контакт с енергийни окислители.Алдехиди + Слаби окислители → карбоксилна киселина
О О
║ ║
C ─ C ─ H + [O] → C ─ C ─ OH
Кетони + слаби окислители → Не реагирайте
О
║
C ─ C ─ C + [O] → Не се получава реакция
Въз основа на това е достатъчно след това да се извърши тази реакция и да се види дали съединението реагира или не. Ако реагира, знаем, че е алдехид; ако не реагира, това е кетон.
В допълнение, продуктите, образувани в тези реакции на окисление на алдехид, са доста видими, с настъпващи промени в цвета, както ще бъде показано по-късно.
Има три основни метода за диференциране на алдехиди и кетони, които са:
1- Толенс реактивен: Този реагент е амонячен разтвор на сребърен нитрат, т.е. той съдържа сребърен нитрат (AgNO3) и излишък от амониев хидроксид (NH4ОН):
AgNO3 + 3 NH4ОХ → Ag (NH3) ОХ + NH4НА3 + 2 Н2О
Tollens Reactive (кръстен на германския химик Бернхард Толенс (1841-1918))
Както е обяснено в текста Изработване на сребърно огледало, когато алдехидът е в контакт с реактив на Tollens, той се окислява до съответната карбоксилна киселина, докато сребърните йони се редуцират до Ag0 (метално сребро). Ако тази реакция се проведе, например, в епруветка, това метално сребро ще се отложи върху стените на епруветката, което води до образуването на филм, наречен сребърно огледало. Този наблюдаван резултат е много красив и се използва в производствения процес на промишлено огледало.
Реакцията, която протича, може да бъде представена по следния начин:
О О
║ ║
R ─ C ─ H + H2O → R ─ C ─ OH + 2e- + 2 H+
2 Ag+ + 2e- → 2 Ag0
2 NH3 + 2 Н+ → 2 NH4+
О О
║║
R C ─ H + 2 Ag+ + 2 NH3 + Н2О → R C ─ OH + 2 Ag0 + 2 NH4+
алдехид Толенс реактивенкарбоксилова киселина метално сребро (сребърно огледало)
От друга страна, ако поставим кетона да реагира с реактив на Tollens, образуването на метално сребро няма да настъпи, тъй като кетоните не могат да намалят йоните Ag.+.
2- Фелинг реактивен: Тази реакционна способност е син разтвор на меден сулфат II (CuSO4) в основна среда, тъй като се смесва с друг разтвор, образуван от натриев хидроксид (NaOH) и натриев и калиев тартарат (NaOOC-CHOH-CHOH-COOK). Тартаратът се добавя към разтвора на меден II сулфат, за да го стабилизира и предотврати утаяването му.
CUSO4 + 2 NaOH → Na2САМО4 + Cu (OH)2
Fehling Reactive (кръстен на германския химик Херман фон Фелинг (1812-1885))
В контакт с реактивния на Фелинг алдехид образува карбоксилната киселина чрез нейното окисление, докато медните йони (Cu)2+), присъстващи в средата, се редуцират, образувайки червеникавокафява утайка (по-подобна на тухла), която е меден оксид. Кетоните, от друга страна, не реагират - защото те не могат да намалят Cu йони2+.
О О
║ ║
R ─ C ─ H + 2 Cu (OH)2 → R ─ C ─ OH + Задник2О + 2 Н2О
алдехид червеникаво-кафява утайка
3- Реактивът на Бенедикт: Тази реакционна способност също се образува от разтвор на меден II сулфат (Cu (OH)2) в основна среда, но се смесва с натриев цитрат.
Както при реагента на Фелинг, в случая на реакцията между алдехида и реактива на Бенедикт има и медни йони (Cu2+) присъстват в средата, които са редуцирани и образуват червен меден оксид.
Този реагент се използва широко при тестове за откриване на присъствието и съдържанието на глюкоза в урината. Глюкозата има алдехидна група в структурата си, така че тя реагира с реагента на Бенедикт, присъстващ в ленти за тези тестове. Оттам просто сравнете цвета на лентата с цвета на кантара върху опаковката на продукта.

Реактивът на Бенедикт се използва за определяне на съдържанието на глюкоза в урината.
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/diferenciacao-aldeidos-cetonas.htm

