تعتمد كمية السعرات الحرارية على تكوين الطعام. لذلك ، لتحديد كمية الحرارة التي يطلقها الطعام بشكل تجريبي والتي يمكن أن يمتصها الجسم ، نستخدم جهازًا يسمى المسعر.
يقيس هذا الجهاز الحرارة الصادرة عن الطعام عند حرقه. هناك عدة أنواع من المسعرات. تم إنشاء أولهم في عام 1780 بواسطة Lavoisier و Laplace وكان a مسعر الجليد.
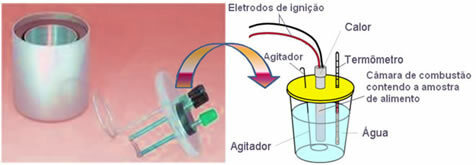
في الوقت الحاضر ، الأكثر استخدامًا والذي يأخذ في الاعتبار مفهوم السعرات الحرارية الموضح أعلاه هو مسعر الماء. هذا الجهاز مغطى بمادة عازلة لمنع فقدان الحرارة من الوسط ؛ ويتم وضع الطعام المراد تحليله في غرفة الاحتراقالذي يحتوي على غاز الأكسجين و أقطاب كهربائية. تخضع هذه الأقطاب الكهربائية لتفريغ كهربائي وتسبب اشتعالها واحتراقها للطعام.
تمتص كتلة الماء المعروفة الموجودة في المسعر الحرارة المنبعثة من الطعام المحترق و ميزان الحرارة يقيس الزيادة في درجة حرارة الماء. بالإضافة إلى ذلك ، يحتوي المسعر على أ المحرض مما يسمح لدرجة حرارة الماء بالبقاء موحدة طوال الوقت.
لذا ، إذا استخدمنا ، على سبيل المثال ، كتلة مقدارها 1 جرام من السكر وكان المسعر يحتوي على 1000 جرام من الماء ، ولاحظنا ذلك في النهاية من التفاعل ، ارتفعت درجة حرارة الماء من 20 درجة مئوية إلى 24 درجة مئوية ، أي أنها زادت بمقدار 4 درجات مئوية ، ويمكننا بعد ذلك الوصول إلى قيمة الطاقة في السكر. يحب؟ حسنًا ، بالنظر إلى مفهوم السعرات الحرارية الأولي ، لدينا:
| ارفع من 1 درجة مئوية → 1 كالوري لكل جرام من الماء |
| ارفع من 4 درجات مئوية → 4 سعرات حرارية لكل جرام من الماء |
لذا فإن 1 جرام من الماء يمتص 4 ليمونات. ومع ذلك ، تم استخدام 1000 جرام من الماء ، وبالنظر إلى أنه تم امتصاص كل الحرارة المنبعثة من الاحتراق ، فإن إجمالي الطاقة التي يمتصها الماء كانت 4000 كالوري أو 4 كيلو كالوري. لذلك نستنتج أن:
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
| قيمة الطاقة للسكر = 4000 كالوري / جرام أو 4 كيلو كالوري / جرام. |
التحول إلى النظام الدولي للوحدات:
1 كيلو كالوري 4.18 كيلو جول
4 كيلو كالوري / جرام ×
س = 16.72 كيلوجول / غرام
بالإضافة إلى ذلك ، يمكننا استخدام المعادلة التالية لحساب كمية الحرارة التي يتخلى عنها الماء أو يمتصها:
| س = م. ç. ر |
أين:
Q = الحرارة التي يتم التخلي عنها أو امتصاصها بواسطة الماء ؛
م = كتلة الماء
ج = حرارة محددة للماء ، والتي تساوي 1.0 كالوري / جم. ° C أو 4.18 J / g. درجة مئوية ؛
Δt = التغير في درجة الحرارة التي يعاني منها الماء ، والذي يُعطى بانخفاض درجة الحرارة النهائية بمقدار الدرجة الأولى (tF - تأنا).
باستخدام هذه الصيغة نحصل على نفس النتيجة:
س = م. ç. ر
س = 1000 جم. 1.0 كالوري / غرام درجة مئوية. (24-20) درجة مئوية
س = 4000 كال
Q = 4.0 كيلو كالوري
أو
س = م. ç. ر
س = 1000 جم. 4.18 كيلوجول / غرام. درجة مئوية. (24-20) درجة مئوية
س = 16.72 كيلو جول
بقلم جينيفر فوغاسا
تخرج في الكيمياء
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
فوغا ، جينيفر روشا فارغاس. "قياس السعرات الحرارية الغذائية باستخدام جهاز قياس السعرات الحرارية" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/medindo-as-calorias-dos-alimentos-por-meio-um-calorimetro.htm. تم الوصول إليه في 27 يونيو 2021.