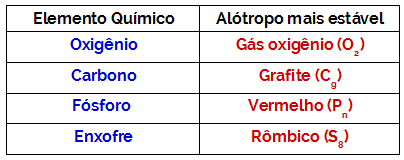
أسئلة حول موازين كيميائية في Enem متكررة جدا. مع وضع هذا في الاعتبار ، أنشأنا هذه المادة ، والتي تقدم أهم الموضوعات حول هذا الفرع من الكيمياء الفيزيائية التي تم تناولها في اختبار المدرسة الثانوية الوطنية (Enem).
من بين القضايا المتعلقة بالتوازن الكيميائي ، لدينا ثابت التوازن من حيث التركيز في مول / لتر ومن حيث الضغط ، ثابت التوازن الأيوني ، ثابت التأين ، إزاحة التوازن ، الأس الهيدروجيني والأس الهيدروجيني ، ثابت التحلل المائي ، المخزن المؤقت وثابت الذوبان.
من بين الموضوعات المذكورة أعلاه ، اكتسب بعضها أهمية أكبر في Enem:
تحول التوازن
ثابت التأين
الرقم الهيدروجيني
تحلل ملحي
درس فيديو عن التوازن الكيميائي في Enem
1. تحول التوازن في العدو
1.1- (Enem 2015) يتكون نقص الأكسجة أو داء المرتفعات من نقص الأكسجين (O2) في الدم الشرياني للجسم. لهذا السبب ، يعاني العديد من الرياضيين من عدم الراحة (الصداع ، والدوخة ، وضيق التنفس) عند ممارسة النشاط البدني على ارتفاعات عالية. في ظل هذه الظروف ، سيكون هناك انخفاض في تركيز الهيموجلوبين المؤكسج (HbO2) في توازن الدم حسب العلاقة:
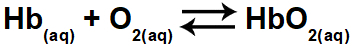
يحدث التغيير في تركيز الهيموجلوبين المؤكسج في الدم بسبب:
أ) ارتفاع ضغط الدم.
ب) ارتفاع درجة حرارة الجسم.
ج) خفض درجة حرارة البيئة.
د) انخفاض الضغط الجزئي للأكسجين.
هـ) انخفاض كمية خلايا الدم الحمراء.
الهيموغلوبين المؤكسج (HbO2) في المواد المتفاعلة (الجانب الأيمن) من المعادلة. يسأل التمرين عن أي من الخيارات قد يؤدي إلى تغيير الهيموغلوبين المؤكسج في الدم ، أي أنه سيحول التوازن إلى اليسار أو اليمين.
خطأ. زيادة تدفق الدم ليس له علاقة بزيادة ضغط الدم.
ب) خطأ. لا تغير درجة الحرارة الميزان المقدم.
ج) خطأ. لا تغير درجة الحرارة الميزان المقدم.
د) صحيح. يقلل تقليل الضغط الجزئي للأكسجين من كمية الهيموجلوبين المؤكسج ، مما يؤدي إلى تحويل التوازن إلى اليسار.
هـ) خطأ. سيؤدي انخفاض عدد خلايا الدم الحمراء إلى انخفاض عدد الهيموجلوبين والهيموجلوبين المؤكسج.
1.2- (العدو 2011) أصبحت المشروبات الغازية أكثر فأكثر أهدافًا لسياسات الصحة العامة. تحتوي منتجات الصمغ على حمض الفوسفوريك ، وهو مادة ضارة بتثبيت الكالسيوم ، وهو معدن يمثل المكون الرئيسي لمصفوفة الأسنان. تسوس الأسنان هو عملية ديناميكية من عدم التوازن في عملية إزالة المعادن من الأسنان ، وفقدان المعادن بسبب الحموضة. من المعروف أن المكون الرئيسي لمينا الأسنان هو ملح يسمى هيدروكسيباتيت. الصودا ، من خلال وجود السكروز ، تقلل من درجة حموضة البيوفيلم (البلاك البكتيري) ، مما يؤدي إلى إزالة المعادن من مينا الأسنان. تستغرق آليات دفاع اللعاب من 20 دقيقة إلى 30 دقيقة لتطبيع مستوى الأس الهيدروجيني ، وإعادة تمعدن السن. تمثل المعادلة الكيميائية التالية هذه العملية:

بالنظر إلى أن الشخص يستهلك المشروبات الغازية يوميًا ، فقد تحدث عملية إزالة المعادن من الأسنان نتيجة لزيادة تركيز:
أ) يا-، الذي يتفاعل مع أيونات الكالسيوم2+، وتحويل التوازن إلى اليمين.
ب) ح+الذي يتفاعل مع هيدروكسيل OH-، وتحويل التوازن إلى اليمين.
ج) يا-، الذي يتفاعل مع أيونات الكالسيوم2+، وتحويل التوازن إلى اليسار.
د) ح+الذي يتفاعل مع هيدروكسيل OH-، وتحويل التوازن إلى اليسار.
ه) كاليفورنيا2+الذي يتفاعل مع هيدروكسيل OH-، وتحويل التوازن إلى اليسار.
الإجابة الصحيحة: حرف الباء
القرار
تؤدي عملية إزالة المعادن إلى تغيير التوازن إلى اليمين. عندما يشرب الشخص الصودا ، فإنه يتناول مادة حمضية ، أي زيادة كمية H+ في المنتصف. يقوم H+ يتفاعل بسرعة مع OH- من التوازن ، وتقليل كمية OH-. بهذه الطريقة ، يتم تحويل التوازن إلى اليمين ، وإزالة المعادن من السن.
1.3- (Enem-2013) يعد التطهير إحدى خطوات معالجة المياه ، حيث تكون المعالجة بالكلور هي الطريقة الأكثر استخدامًا. تتكون هذه الطريقة من إذابة غاز الكلور في محلول تحت الضغط وتطبيقه على الماء المراد تطهيره. معادلات التفاعل الكيميائي المتضمنة هي:

يتم التحكم في عملية التطهير بواسطة حمض هيبوكلوروس ، الذي لديه إمكانية تطهير أكبر بحوالي 80 مرة من أنيون هيبوكلوريت. يعتبر الرقم الهيدروجيني للوسط مهمًا لأنه يؤثر على مدى تأين حمض هيبوكلوروس. لكي يكون التطهير أكثر فعالية ، يجب أن يكون الرقم الهيدروجيني للماء المراد معالجته أقرب إلى:
أ) 0
ب) 5
ج) 7
د) 9
هـ) 14
الإجابة الصحيحة: حرف الباء
وفقًا للنص ، يتم تنفيذ أفضل إجراء مطهر بواسطة مادة HClO. لذلك ، يجب توجيه كل تفسير واستنتاج نحو طريقة للحصول على هذه المادة.
مادة HClO موجودة في الميزان الثاني ، لذا من التكتيكات المثيرة للاهتمام تحويل هذا التوازن إلى اليسار. لهذا ، وفقًا لـ مبدأ Le Chatelier، لدينا خيار زيادة كمية H.+ (إضافة مادة حمضية ، درجة الحموضة أقل من 7) أو زيادة كمية Cl-.
من الجدير بالذكر أنه في المعادلة الأولى يوجد توازن كيميائي آخر والذي يمثل نوع HClO-، التي لها صلة بـ H+، وتحويل التوازن إلى اليسار. هذه خطوة لا نريدها.
لذلك ، يجب أن نستخدم درجة الحموضة الحمضية (أقل من 7). ومع ذلك ، لا ينبغي أن يكون هذا الرقم الهيدروجيني حمضيًا جدًا لتجنب الكثير من كاتيونات H.+ في المنتصف.
نرى أيضا:التوازن الكيميائي في الكهوف
2. الرقم الهيدروجيني والتحلل المائي المالح في Enem
2.1- (Enem-2017) يمكن الحصول على العديد من المنتجات الطبيعية من النباتات من خلال عملية الاستخراج. لاباكول من فئة النافثوكينون. يحتوي هيكلها على enol hydroxyl (pKa = 6.0) الذي يسمح بعزل هذا المركب من نشارة الخشب عن طريق الاستخراج بمحلول مناسب ، متبوعًا بالترشيح البسيط. ضع في اعتبارك أن pKa = -log Ka وأن Ka هو الثابت الحمضي لتفاعل تأين lapachol.

ما الحل الذي يجب استخدامه لاستخراج lapachol من نشارة الخشب ipê بشكل أكثر كفاءة؟
أ) محلول نا2كو3 لتشكيل ملح لاباكول.
ب) محلول عازل حمض الخليك / أسيتات الصوديوم (الرقم الهيدروجيني = 4.5).
ج) محلول NaCI لزيادة القوة الأيونية للوسط.
د) محلول نا2فقط4 لتشكيل زوج أيوني مع lapachol.
ه) محلول HCI من أجل استخراجه من خلال تفاعل الحمض القاعدي.
يشير البيان إلى أن pKa للمادة 6.0. يجب استخدام قيمة pKa هذه في تعبير pKa:
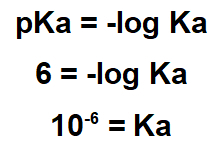
نظرًا لأن Ka الخاص بك صغير ، فإن lapachol مادة حمضية ، لذلك لإزالته ، من المفيد استخدام مادة أساسية.
أ) صحيح. الملح أساسي ، لأنه يأتي من قاعدة قوية (لأنه من عائلة IA) ، وثاني أكسيد الكربون3 يأتي من حمض ضعيف (H2كو3).
ب) خطأ. المحلول المنظم حمضي ، ونحن بحاجة إلى قاعدة.
ج) خطأ. كلوريد الصوديوم هو ملح متعادل ، لأنه يأتي من قاعدة قوية (لأنه من عائلة IA) ، ويأتي الكلور من حمض قوي (حمض الهيدروكلوريك).
د) خطأ. في2فقط4 هو ملح محايد ، حيث يأتي Na من قاعدة قوية (لأنه من عائلة IA) ، و SO4 يأتي من حمض قوي (H2فقط4).
انه مزيف. حمض الهيدروكلوريك هو حمض ، ونحن بحاجة إلى قاعدة.
2.2- (العدو- 2014) بهدف تقليل الآثار البيئية ، تحدد التشريعات البرازيلية أن المخلفات الكيميائية التي يتم إطلاقها مباشرة في الجسم المتلقي لها درجة حموضة بين 5.0 و 9.0. تحتوي النفايات السائلة المائية المتولدة في عملية صناعية على تركيز أيون الهيدروكسيل يساوي 1.0.10-10 مول / لتر. للامتثال للتشريع ، قام الكيميائي بفصل المواد التالية ، المتوفرة في مستودع الشركة: CH3COOH ، نا2SO4، CH3أوه ، ك2كو3 و نيو هامبشاير4Cl.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
من أجل إطلاق البقايا مباشرة في الجسم المستقبل ، ما هي المادة التي يمكن استخدامها لضبط الرقم الهيدروجيني؟
أ) CH3COOH
سلة مهملات2فقط4
ج) CH3أوه
د) ك2كو3
ه) NH4Cl
الإجابة الصحيحة: الحرف د
القرار
الخطوة 1: حدد الرقم الهيدروجيني للبقايا.
يشير التمرين إلى أن البقايا تحتوي على تركيز هيدروكسيد يساوي 10-10.
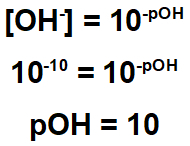
لذلك ، يمكننا حساب الرقم الهيدروجيني لهذه البقايا:

مما سبق ، لدينا أن البقايا لها طابع حمضي ، حيث أن الرقم الهيدروجيني لها أقل من 7. وبالتالي ، من أجل تحييده ، من الضروري استخدام مادة ذات طابع أساسي.
الخطوة 2: حدد طبيعة كل ملح للإشارة إلى أيهما أساسي ، مثل CH3COOH (البديل أ) هو حمض ، و CH3OH (البديل ج) عبارة عن فئة عضوية كحولية ذات طابع حمضي.
ب) ملح محايد ، حيث يأتي Na من قاعدة قوية (لأنه من عائلة IA) ، و SO4 يأتي من حمض قوي (H2فقط4).
د) الملح الأساسي ، حيث يأتي K من قاعدة قوية (لأنه من عائلة IA) ، و CO3 يأتي من حمض ضعيف (H2كو3).
ه) ملح حامض ، مثل NH4 يأتي من قاعدة ضعيفة (NH4OH) ، و Cl يأتي من حمض قوي (HCl).
2.3- (العدو- 2014) لاحظ الباحث أن الملصق الموجود على إحدى الجرار التي يحتفظ فيها بتركيز إنزيمات الجهاز الهضمي غير مقروء. إنه لا يعرف ما هو الإنزيم الذي يحتويه الزجاج ، لكنه يشك في أنه بروتين معدي يعمل في المعدة عن طريق هضم البروتين. مع العلم أن الهضم في المعدة حمضي وأن الأمعاء أساسية ، يقوم بتجميع خمسة أنابيب اختبار مع الطعام بشكل مختلف ، أضف تركيز الإنزيم إلى المحاليل ذات الرقم الهيدروجيني المحدد وانتظر لمعرفة ما إذا كان الإنزيم يعمل في أي منها هم. أنبوب الاختبار الذي يجب أن يعمل فيه الإنزيم للإشارة إلى صحة فرضية الباحث هو الأنبوب الذي يحتوي على:
أ) مكعب البطاطس في محلول مع الرقم الهيدروجيني = 9.
ب) قطعة من اللحم في محلول مع الرقم الهيدروجيني = 5.
ج) بياض البيض المسلوق في محلول مع الرقم الهيدروجيني = 9.
د) جزء من المعكرونة في محلول مع الرقم الهيدروجيني = 5.
ه) كرة الزبدة في محلول مع الرقم الهيدروجيني = 9.
الإجابة الصحيحة: حرف الباء
يتطلب التمرين من الطالب تفسيرًا جيدًا وارتباطًا بالمعرفة الكيميائية الحيوية للأطعمة. يبلغ أن الباحث يعتقد أن الإنزيم هضمي ، ويعمل عند درجة الحموضة الحمضية ويعمل على البروتينات (لأنه بروتياز).
إذا كان هذا الإنزيم يعمل في بيئة حمضية ، فيجب أن يكون الرقم الهيدروجيني أقل من 7. تتكون اللحوم من البروتينات ، بينما تتكون المعكرونة من الكربوهيدرات. إذن الجواب الصحيح هو البديل ب.
2.4- (العدو- 2012) أسقطت ربة منزل بالخطأ الماء من جراء إذابة سمكة في الثلاجة ، مما ترك رائحة قوية وكريهة داخل الجهاز. من المعروف أن رائحة السمك المميزة ترجع إلى الأمينات ، وأن هذه المركبات تتصرف كقواعد. في الجدول ، تم سرد تركيزات الهيدروجين لبعض المواد الموجودة في المطبخ ، والتي تفكر ربة المنزل في استخدامها عند تنظيف الثلاجة.

من بين المواد المدرجة ، أي منها مناسب للتخفيف من هذه الرائحة؟
أ) الكحول أو الصابون
ب) عصير الليمون أو الكحول
ج) عصير الليمون أو الخل
د) عصير ليمون أو لبن أو صابون
هـ) صابون أو صودا / رماد صودا
الإجابة الصحيحة: الحرف ج
القرار
يقترح التمرين مشكلة تكون فيها ثلاجة ربة المنزل لها رائحة قوية ناتجة عن مادة ذات طبيعة أساسية. وبالتالي ، يتم التساؤل عن المواد التي ستكون مثيرة للاهتمام لحل هذه المشكلة.
لتحييد قاعدة ، من الضروري استخدام مادة ذات طبيعة حمضية أو مع درجة حموضة أقل من 7. كيف قدم التمرين قيم تركيزات الهيدروجين+ من المواد ، كان يكفي استخدام كل واحدة في التعبير أدناه:

هكذا:
العصير: الرقم الهيدروجيني = 2
الحليب: الرقم الهيدروجيني = 6
الخل: الرقم الهيدروجيني = 3
الكحول: الرقم الهيدروجيني = 8
الصابون: الرقم الهيدروجيني = 12
البرميل: الرقم الهيدروجيني = 12
المواد ذات الطابع الحمضي هي العصير والخل والحليب. وبالتالي ، فإن البديل ج فقط هو الذي يجلب مواد ذات طبيعة حمضية.
3. ثابت التوازن في العدو
3.1- (Enem-2016) يمكن حرق الإطارات بعد تآكلها الكامل لتوليد الطاقة. من بين الغازات المتولدة في الاحتراق الكامل للمطاط المعالج بالفلكن ، بعضها ملوثات وتسبب الأمطار الحمضية. لمنعهم من الهروب إلى الغلاف الجوي ، يمكن تحويل هذه الغازات إلى محلول مائي يحتوي على مادة مناسبة. ضع في اعتبارك معلومات المادة المدرجة في الجدول أدناه:

من بين المواد المدرجة في الجدول ، أكثر المواد القادرة على إزالة الغازات الملوثة بكفاءة هي (أ)
أ) الفينول.
ب) بيريدين.
ج) ميثيل أمين.
د) فوسفات هيدروجين البوتاسيوم.
ه) كبريتات هيدروجين البوتاسيوم.
الإجابة الصحيحة: الحرف د
القرار
يطرح التمرين مشكلة حيث تعمل الغازات الملوثة على تعزيز المطر الحمضي. ثم يسأل عن أي من المواد المذكورة سيكون مثيرًا للاهتمام لتحييد هذه الغازات ، وبالتالي تجنب المطر الحمضي.
لتجنب المطر الحمضي ، يجب تحييد الغازات الحمضية باستخدام محلول أساسي. المواد التي تحمل هذه الخاصية هي تلك التي تطلق مجموعات OH بشكل تفضيلي- في المنتصف. في الجدول ، يعتبر البيريدين والميثيلامين وفوسفات الهيدروجين البوتاسيوم من المواد الأساسية.
وبالتالي ، من أجل تحديد المادة القادرة على إزالة الغازات الملوثة بشكل أكثر كفاءة ، يجب علينا تحليل قيمة ثابت التأين. كلما زاد الثابت ، زادت القدرة على إطلاق OH-. لذلك فوسفات هيدروجين البوتاسيوم إنها أنسب مادة في هذه الحالة.
3.2- (Enem-2015) تُستخدم العديد من الأحماض في الصناعات التي تتخلص من نفاياتها السائلة في المسطحات المائية ، مثل الأنهار والبحيرات ، مما قد يؤثر على التوازن البيئي. لتحييد الحموضة ، يمكن إضافة ملح كربونات الكالسيوم إلى النفايات السائلة بكميات مناسبة ، حيث ينتج بيكربونات ، التي تحيد الماء. يتم تقديم المعادلات المتضمنة في العملية:

بناءً على قيم ثوابت التوازن للتفاعلات II و III و IV عند 25ا C ، ما هي القيمة العددية لثابت التوازن للتفاعل I؟
أ) 4.5 × 10-26
ب) 5 × 10-5
ج) 0.8 × 10-9
د) 0.2 × 105
هـ) 2.2x1026
الإجابة الصحيحة: حرف الباء
القرار
هذا التمرين ينطوي على تأين مستمر. في البداية ، من الضروري فهم أن المعادلة I هي في الواقع نتيجة (مجموع) المعادلات II و III و IV. لذلك ، لبدء القرار ، يجب أن نستخدم مبادئ قانون هيس.
الخطوة 1: استخدام قانون هيس.
بقلب المعادلة II والحفاظ على المعادلتين الثالث والرابع ، لدينا:
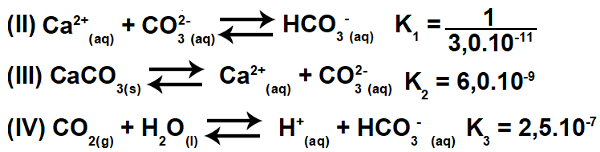
وبالتالي ، يمكننا أن نلاحظ أن أنيون CO3-2 والكاتيون H.+ سيتم حذفه ، وسيؤدي مجموع المعادلات إلى المعادلة الأولى.
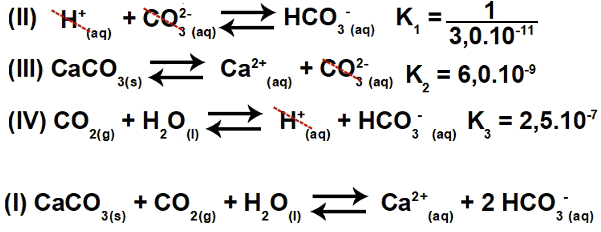
الخطوة 2: حساب ثابت
يتم دائمًا إعطاء ثابت التوازن لمعادلة التأين بضرب ثوابت المعادلات الأخرى:

بي ديوغو دياس