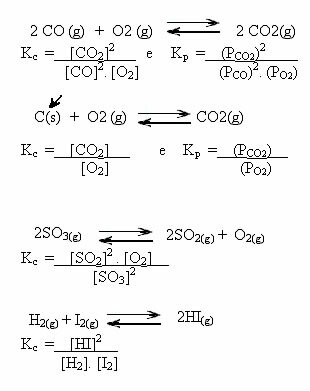
Для іонних сполук число окислення (Nox) являє собою заряд, який набуває іон при здійсненні іонного зв’язку.Наприклад, хлорид натрію - це іонна сполука, що утворюється, коли натрій втрачає електрон до хлору; таким чином, натрій стає катіоном з електричним зарядом +1, а хлор-аніоном із зарядом -1. Ці значення складають їх відповідний Nox.
Однак молекулярні сполуки ні втрачають, ні отримують електрони, тому їх Nox вважається таким теоретичний електричний заряд, який би набув елемент, якщо розірвати ковалентний зв’язок, а електронна пара залишила б більш електронегативний елемент. Наприклад, у випадку соляної кислоти (HCl) хлор є найбільш електронегативним елементом, тому він би сильніше залучав до себе електронну пару, спільну з воднем. Таким чином, ми маємо, що Nox хлору дорівнює -1 (оскільки в ньому на один електрон більше, ніж у водню), а водню дорівнює +1 (оскільки водень втратив електрон до хлору).

* Щоб завантажити зображення у форматі PDF, Натисніть тут!
Отже, ми можемо зробити таке визначення:

Не зупиняйтесь зараз... Після реклами є ще щось;)
У разі одиничних іонів Nox еквівалентний власному електричному заряду. Наприклад:
О2-: Nox = -2
Кл-: Nox = -1
В+: Nox = +1
Віра2+: Nox = +2
Ал3+: Nox = +3
Нарешті, у випадку елемента або простих речовин, що складаються з атомів лише одного типу елемента, маємо, що Nox дорівнює нулю.Ось кілька прикладів та таких речовин: O2, немає2, H2, Він тощо.
Крім того, Nox вказує на схильність елемента до окислення або відновлення, оскільки коли відбувається окислення (втрата електронів), Nox збільшується. У разі відновлення (виграшу електронів) відбувається навпаки, Nox зменшується. Для того, щоб розглянути цей випадок, спостерігаємо реакцію окислення-відновлення вуглекислого газу нижче:
0 0 +4-2
Çn (и) + ні2 (г) → n CO2 (г)
Зверніть увагу, оскільки вони є елементом (C) і простою речовиною (O2), Nox реагентів дорівнював нулю. Однак після реакції вуглець окислюється, тому зауважте, як збільшився ваш Nox (від 0 до +4). З іншого боку, кисень був знижений, тому його Nox зменшився, переходячи від 0 до -2.
Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. "Поняття кількості окислення (NOx)"; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/conceito-numero-oxidacao-nox.htm. Доступ 28 червня 2021 року.