Коли ми готуємо їжу вдома, ми використовуємо горіння кулінарного газу. Одне з речей, яке ми можемо побачити у полум’ї, яке виникає при згорянні цього газу, полягає в тому, що його колір, як правило, дуже світло-блакитний. Однак у більшості реакцій горіння, наприклад, при спалюванні свічки, полум’я жовте.

Тоді виникає питання:
"Якщо кожен пожежа є результатом реакції горіння, чому деякі полум'я мають різні кольори?"
Щоб зрозуміти, як це відбувається, ми повинні зрозуміти, що таке реакція горіння і які речовини присутні в кожній із згаданих реакцій.
Реакція горіння відбувається, коли паливо (окислюваний матеріал) витрачається окислювачем (газоподібним матеріалом, що містить кисень) для отримання теплової енергії (тепла).
Іншим важливим моментом, який ми повинні знати про реакції горіння, є те, що вони можуть відбуватися в повна або неповна. Якщо для споживання палива достатньо кисню, реакція буде повною і вироблятиме вуглекислий газ (CO2) і вода (H2О). В іншому випадку горіння буде частковим, неповним, утворюючи чадний газ (СО) та воду; або вуглець (С) і вода.
В обох випадках, що ми аналізуємо, окислювачем є кисень, присутній у повітрі. Однак паливо буває різним. Газом для приготування є фактично скраплений нафтовий газ (LPG), який являє собою суміш вуглеводнів (алканів), основним паливом є бутан (C4H10). Отже, газ для приготування складається з молекул алкану, які мають лише три-чотири атоми вуглецю, саме тому для повного його згоряння потрібно мало кисню. Ця реакція може бути виражена наступним чином:
1С4H10 (г) + 13/2 O2 (г) → 4 CO2 (г) + 5 годин2О(g), ∆H <0
У випадку зі свічками парафін є паливом для реакції, і він складається із суміші алканів з атомами вуглецю, що діапазон від 20 до 36. Таким чином, для повного проходження цієї реакції потрібно набагато більше кисню. Дивіться приклад:
1С24H50 (с) + 70/2 O2 (г) → 25 CO2 (г) + 25 год2О(g), ∆H <0
У повітрі недостатньо кисню для повного згоряння, тому воно відбувається не повністю, як показано нижче:
1С24H50 (с) +49/2 O2 (г) → 24 CO(g) + 25 год2О(g), ∆H <0
1С24H50 (с) +25/2 O2 (г) → 24C(s) + 25 год2О(g), ∆H <0
Неповні реакції виробляють менше енергії, ніж повне згоряння. Це пояснює різницю між кольорами полум’я, оскільки жовте полум’я, характерне для неповного згоряння, має меншу енергію. Синє полум'я характерно для повного згоряння з більшою енергією.
Це також пояснює утворення сажі полум’ям свічки (фото нижче), яке є вуглецем, який вважається продуктом неповного згоряння.
Але чому в пальнику Бунзена можна отримати жовте та синє полум’я, коли паливо не змінюється?
У випадку пальника Бунзена це досягається регулюванням впуску газу та повітря. Якщо вікно закрито, що спричиняє потрапляння невеликої кількості повітря, полум’я буде жовтим, оскільки в ньому буде мало кисню для повного згоряння. Якщо регулювання газоповітряної суміші адекватне, ми отримуємо синє полум’я.
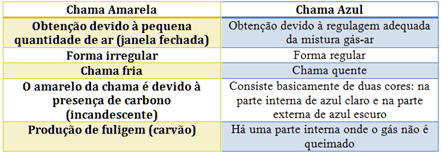
Подивіться характеристики кожного з них у таблиці нижче:
Дженніфер Фогача
Закінчив хімію
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/combustao-chamas-cores-diferentes.htm