Органічна хімія - це широка область хімії, яка вивчає сполуки вуглецю.
До знань з органічної хімії можна підходити кількома способами, і, обмірковуючи це, ми склали запропоновані вправи, вступні іспити та питання Enem, щоб перевірити свої знання.
Також використовуйте коментарі до резолюцій, щоб дізнатись ще більше про тему.
Запропоновані вправи
питання 1
Подивіться на органічні сполуки нижче та визначте органічні функції відповідно до виділених функціональних груп. Після цього назвіть речовини.
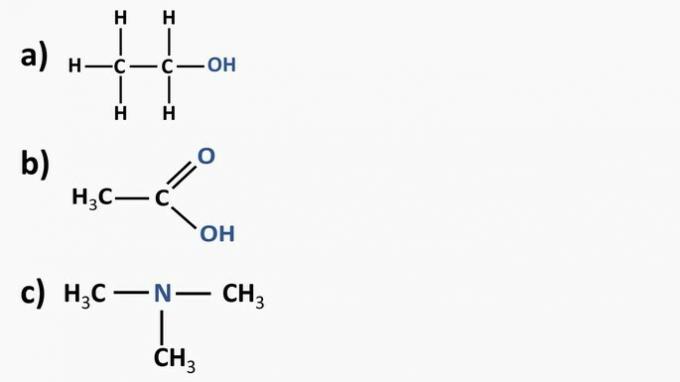
Відповідь:
а) Органічна сполука: етанол
- органічна функція: алкоголь
- Загальна формула: R — OH
- Ідентифікація: гідроксил (ОН), пов'язаний з вуглецевим ланцюгом
б) Органічна сполука: етанова кислота.
- Органічна функція: карбонова кислота
- Загальна формула: R — COOH
- Ідентифікація: карбоновий радикал (COOH), пов'язаний з вуглецевим ланцюгом
в) Органічна сполука: триметиламін
- Органічна функція: амін (третинний)
- Загальна формула:
- Ідентифікація: азот пов'язаний з трьома вуглецевими ланцюгами
питання 2
В органічній хімії сполуки розпізнаються ланцюгами, утвореними вуглецем та воднем. Однак інші елементи можуть бути частиною хімічної структури цих сполук, наприклад кисень.
Виберіть альтернативу, де дві органічні сполуки мають кисневі органічні функції.
а) хлороформ та етилметанат
б) пропанол та пропанова кислота
в) етен та етандіол
г) етанамід та бензол
Правильна відповідь: б) пропанол та пропанова кислота
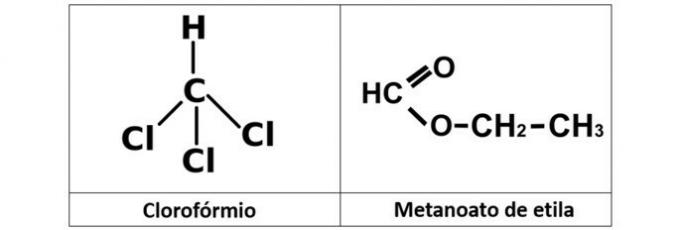
а) НЕПРАВИЛЬНО. Ми маємо хлороформ (CHCl3), який є алкилгалогенидом, та ефір етиламетаноату (C3H6О2), який містить у своїй структурі кисень.
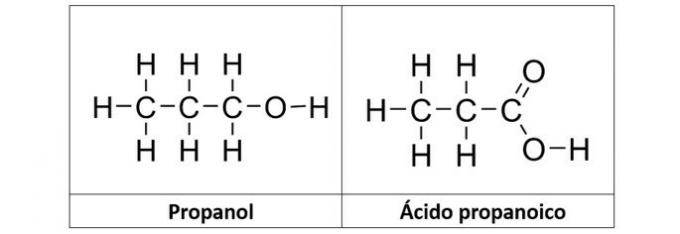
б) ПРАВИЛЬНО. У цій альтернативі ми маємо дві сполуки, які мають кисневі органічні функції. Пропанол (C3H8О) - це спирт, що утворюється трьома вуглецями. Пропанова кислота (C3H6О2) є карбоновою кислотою.
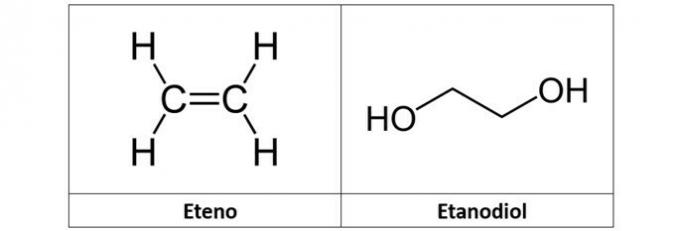
в) НЕПРАВИЛЬНО. Етилен (C2H4), який також називають етиленом, є вуглеводнем алкенного типу. Вже етандіол (C2H6О2) - це спирт із двома гідроксилами у своїй структурі.
г) НЕПРАВИЛЬНО. Етанамід (C2H5NO) є амідом, а бензол - ароматичним вуглеводнем і, отже, утворюється лише за рахунок вуглецю та водню.

питання 3
Подивіться на структуру органічної сполуки нижче та перевірте справжні твердження.

(01) З'єднання має органічну азотну функцію.
(02) Це первинний амін, оскільки він зв’язаний лише з одним воднем.
(03) Назва сполуки - діетиламін.
Правильна відповідь:
(01) ПРАВИЛЬНО. Азотиста органічна функція, присутня в сполуці, є аміном.
(02) НЕПРАВИЛЬНО. Це вторинний амін, оскільки азот пов'язаний з двома вуглецевими ланцюгами.
(03) НЕПРАВИЛЬНО. Назва сполуки - диметиламін, оскільки до азоту приєднано два метильних радикали.
питання 4
Евгенол, представник сімейства фенілпропаноїдів, являє собою ароматичну органічну сполуку, яка міститься в гвоздиці - прянощі, яка використовувалася з давніх часів.

Дотримуйтесь структурну формулу сполуки та визначте присутні органічні функції.
а) Спирт і ефір
б) Фенол та ефір
в) Спирт і ефір
г) Фенол та складний ефір
д) Спирт і вуглеводні
Правильна альтернатива: б) Фенол та ефір.
Евгенол має кисневі органічні функції у своєму ланцюзі, тобто, крім атомів вуглецю та водню, кисень є гетероатомом.
Органічна функція фенолу характеризується гідроксилом (-ОН), приєднаним до ароматичного кільця. В ефірній функції кисень знаходиться між двома вуглецевими ланцюгами.
питання 5
ЕДТА, повне найменування якого є етилендіамінтетраоцтова кислота, є органічною сполукою, що має багато застосувань. Його здатність зв’язувати іони металів робить його хелатуючим агентом, який широко використовується як в лабораторії, так і в промисловості.
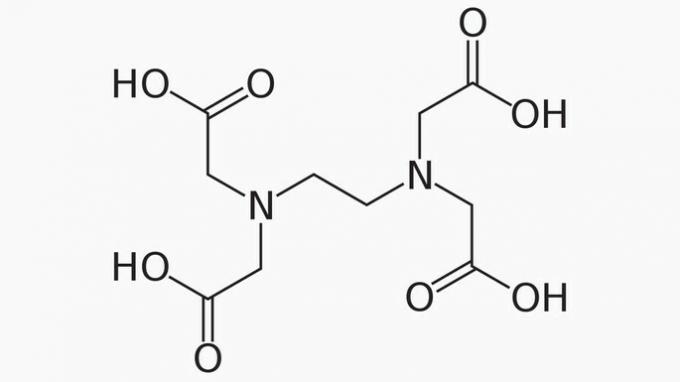
Щодо ЕДТА, то правильно стверджувати, що вуглецевий ланцюг є:
а) Відкриті, однорідні та ненасичені.
б) Закриті, неоднорідні та насичені.
в) Відкриті, неоднорідні та ненасичені.
г) Закритий, однорідний і насичений.
д) Відкриті, неоднорідні та насичені.
Правильна відповідь: д) Відкрита, неоднорідна і насичена.
Мережа EDTA класифікується на:
ВІДЧИНЕНО. Відповідно до розташування атомів вуглецю в структурі ЕДТА ми бачимо, що завдяки наявності кінців ланцюг сполуки розкривається.
ГЕТЕРОГЕННИЙ. Окрім сполук вуглецю та водню, вуглецевий ланцюг має гетероатоми азоту та кисню.
НАСІЧЕНИЙ. Зв'язки між атомами вуглецю насичені, оскільки ланцюг має лише одинарні зв'язки.
Дізнайтеся більше на: Органічна хімія.
питання вступного іспиту
питання 1
(UFSC) Спостерігайте за неповними органічними структурами та визначайте правильні елементи:
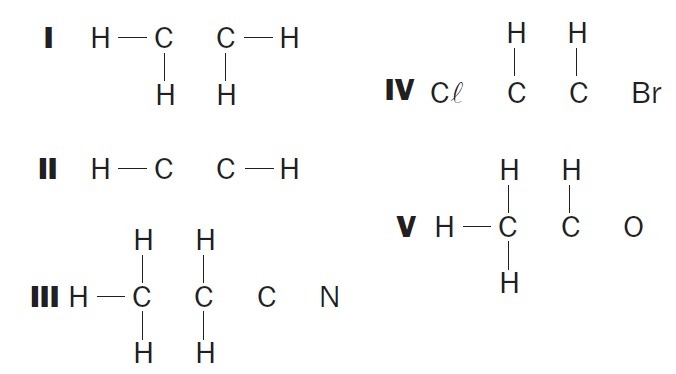
(01) У структурі I відсутній єдиний зв’язок між атомами вуглецю.
(02) У структурі II відсутній потрійний зв’язок між атомами вуглецю.
(03) У структурі III відсутні два одинарних зв’язки між атомами вуглецю та потрійний зв’язок між атомами вуглецю та азоту.
(04) У структурі IV бракує двох одинарних зв’язків між атомами вуглецю та галогенами та подвійного зв’язку між атомами вуглецю.
(05) У структурі V відсутній єдиний зв’язок між атомами вуглецю та єдиний зв’язок між атомами вуглецю та кисню.
Правильні альтернативи: 02, 03 та 04.
Окрім вуглецю, обов’язкового хімічного елемента в органічних сполуках, інші структури можуть бути присутніми в структурах і зв’язані ковалентними зв’язками, де електрони діляться.
Валентність елементів визначає кількість зв'язків, які можуть утворитися, як показано в таблиці нижче.
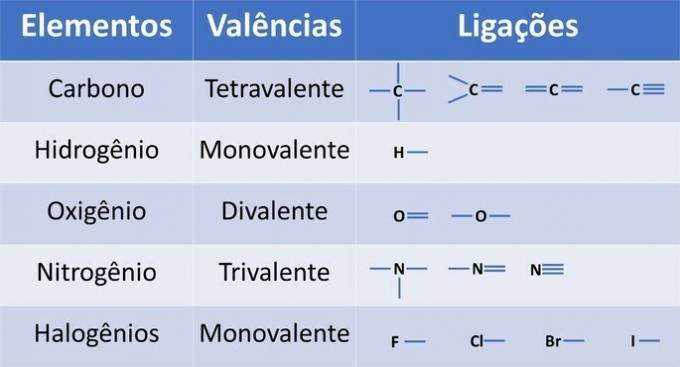
З цієї інформації ми маємо:
(01) НЕПРАВИЛЬНО. У структурі відсутній подвійний зв’язок між атомами вуглецю з утворенням сполуки етену.
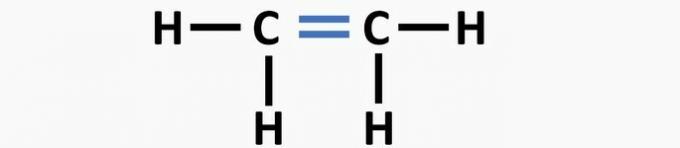
(02) ПРАВИЛЬНО. У структурі відсутній потрійний зв’язок між атомами вуглецю з утворенням сполуки етину.
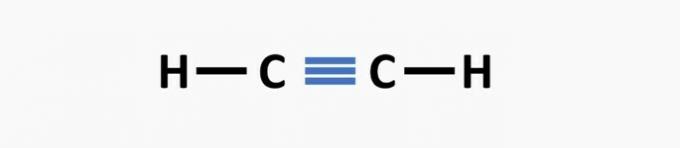
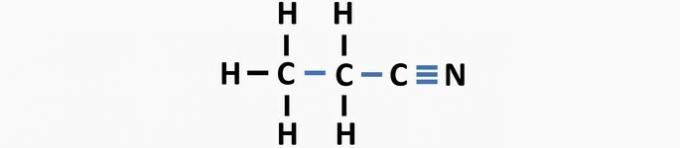
(03) ПРАВИЛЬНО. У структурі відсутні одинарні зв’язки між вуглецями та потрійні зв’язки між вуглецем та азотом, утворюючи сполуку пропаннітрил.
(04) ПРАВИЛЬНО. У структурі відсутні одинарні зв’язки між вуглецем та галогеном та подвійні зв’язки між вуглецями для утворення дихлоретенової сполуки.
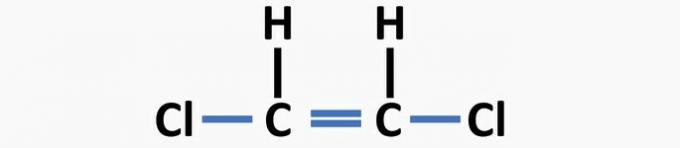
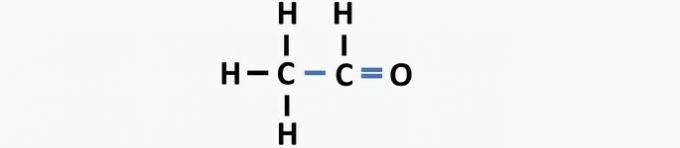
(05) НЕПРАВИЛЬНО. У структурі відсутній єдиний зв’язок між вуглецями та подвійний зв’язок між вуглецем та киснем з утворенням етанольної сполуки.
питання 2
(UFPB) Будова органічної сполуки молекулярної формули С5H8Що представляє розгалужену, ненасичену, гетерогенну та аліциклічну ланцюги:

Правильна альтернатива: d.
Вуглецеві ланцюги можна класифікувати наступним чином:
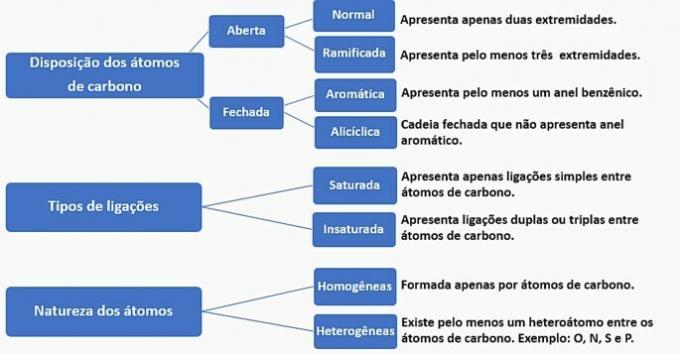
Відповідно до цієї інформації ми маємо:
а) НЕПРАВИЛЬНО. Ланцюг класифікується як нормальний, насичений, однорідний і аліциклічний.
б) НЕПРАВИЛЬНО. Ланцюг класифікується як нормальний, ненасичений, однорідний і відкритий.
в) НЕПРАВИЛЬНО. Ланцюг класифікується як розгалужена, ненасичена, однорідна і відкрита.
г) ПРАВИЛЬНО. Ланцюг класифікується як розгалужена, ненасичена, неоднорідна та аліциклічна
- Він має гілку: метильний радикал;
- Має ненасиченість: подвійний зв’язок між вуглецями;
- Він має гетероатом: кисень, зв’язаний з двома вуглецями;
- Він представляє замкнутий ланцюг: вуглеці, зв’язані по колу без присутності ароматичного кільця.
д) НЕПРАВИЛЬНО. Ланцюг класифікується як розгалужена, ненасичена, неоднорідна і відкрита.
питання 3
(Сентек-БА) У структурі, показаній нижче, нумеровані вуглеці мають, відповідно:
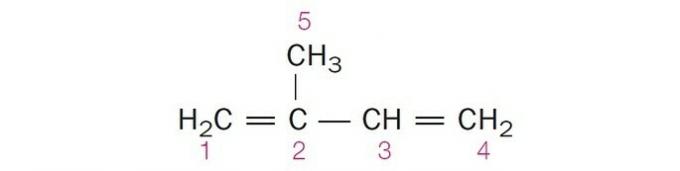
а) sp2, sp, sp2, sp2, sp3.
б) sp, sp3, sp2, sp, sp4.
в) сп2, sp2, sp2, sp2, sp3.
г) sp2, sp, sp, sp2, sp3.
д) сп3, sp, sp2, sp3, sp4.
Правильна альтернатива: c) sp2, sp2, sp2, sp2, sp3.
Оскільки він має 4 електрони у валентній оболонці, вуглець є чотиривалентним, тобто має тенденцію утворювати 4 ковалентні зв’язки. Ці облігації можуть бути одинарними, подвійними або потрійними.
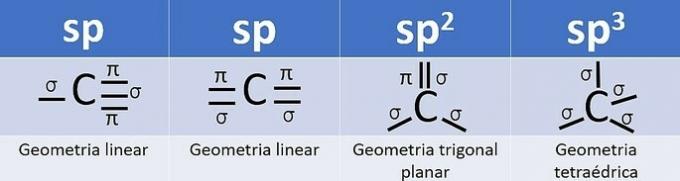
Кількість гібридних орбіталей - це сума сигма-зв'язків (σ) вуглецю, оскільки зв'язок не гібридизує.
- sp: 2 сигма-посилання
- sp2: 3 сигма-посилання
- sp3: 4 сигма-посилання
Відповідно до цієї інформації ми маємо:
а) НЕПРАВИЛЬНО. Вуглець 2 має sp-гібридизацію2, оскільки він має 3 σ-зв’язки та один зв’язок .
б) НЕПРАВИЛЬНО. Вуглець не має sp-гібридизації4 а sp-гібридизація відбувається, коли між вуглецями існує потрійний або два подвійні зв’язки.
в) ПРАВИЛЬНО. Сума σ-зв’язків на кожному вуглеці дає альтернативну гібридизацію.
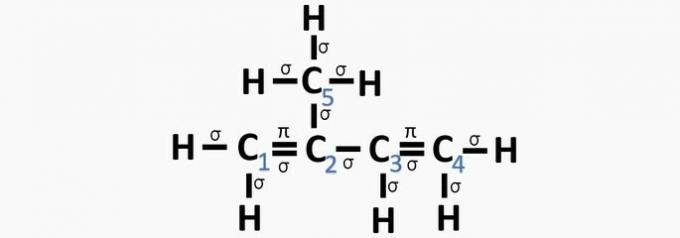
г) НЕПРАВИЛЬНО. Sp-гібридизація відбувається, коли між вуглецями існує потрійний або два подвійні зв’язки.
д) НЕПРАВИЛЬНО. Вуглець не має sp-гібридизації4 а sp-гібридизація відбувається, коли між вуглецями існує потрійний або два подвійні зв’язки.
питання 4
(UFF) Існує газоподібний зразок, утворений однією з таких сполук: CH4; Ç2H4; Ç2H6; Ç3H6 або С3H8. Якщо 22 г цього зразка займають об'єм 24,6 л при тиску 0,5 атм і температурі 27 ° C (Дано: R = 0,082 л .атм. К–1.mol–1), робиться висновок, що це газ:
а) етан.
б) метан.
в) пропан.
г) пропілен.
д) етен.
Правильна альтернатива: в) пропан.
1-й крок: перетворіть одиницю температури з Цельсія в Кельвін.
2-й крок: обчисліть кількість молей сполуки, використовуючи загальне рівняння газу.
3-й крок: обчисліть молярну масу сполуки.
4-й крок: знайдіть вуглеводень, який має молярну масу 44 г / моль.
Метан
Ефін
Етан
пропілен
Пропан
Таким чином, зроблено висновок, що газ, який відповідає інформації в заяві, є пропаном.
питання 5
(ITA) Розглянемо такі речовини:
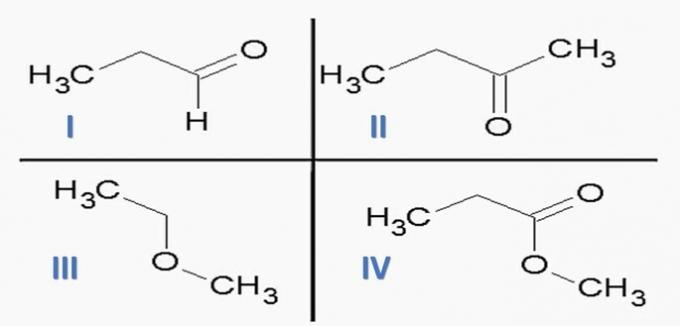
та наступні хімічні функції:
. карбонова кислота;
B. алкоголь;
ç. альдегід;
d. кетон;
і. складний ефір;
f. ефір.
Варіант, який ПРАВИЛЬНО пов'язує речовини з хімічними функціями:
а) Id; IIc; IIIe; IVf.
б) Ic; IId; IIIe; ПДВ
в) Ic; IId; IIIf; IVe.
зробила; IIc; IIIf; IVe.
д) Іа; IIc; IIIe; IVd.
Правильна альтернатива: в) Ic; IId; IIIf; IVe.
Органічні функції визначаються структурами та групують органічні сполуки зі схожими характеристиками.
Хімічні функції, наявні в альтернативних варіантах:
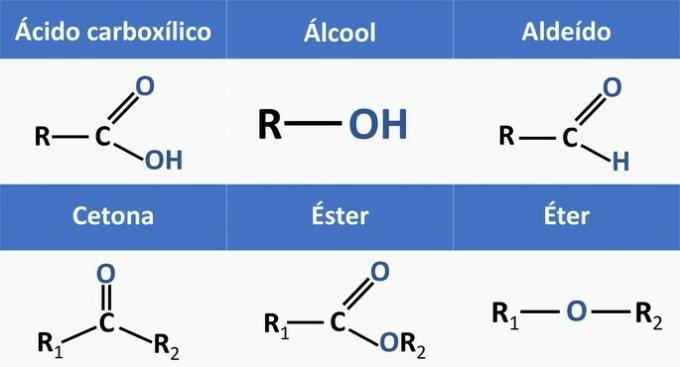
Аналізуючи вищезазначені структури та сполуки, присутні в заяві, маємо:
а) НЕПРАВИЛЬНО. Функції органу правильні, але послідовність неправильна.
б) НЕПРАВИЛЬНО. Серед сполук немає карбонової кислоти.
в) ПРАВИЛЬНО. Функціональні групи, присутні в сполуках, представляють наступні хімічні функції.

г) НЕПРАВИЛЬНО. I - альдегід, а II - кетон.
д) НЕПРАВИЛЬНО. Серед сполук немає карбонової кислоти.
Дізнайтеся більше на: Органічні функції.
Запитання ворогів
питання 1
(Enem / 2014) Один із методів визначення вмісту етанолу в бензині полягає у змішуванні відомих обсягів води та бензину в певній пляшці. Після струшування колби та очікування певного періоду вимірюють обсяги двох не змішуваних фаз: однієї органічної та іншої водної. Етанол, який колись змішується з бензином, тепер змішується з водою.
Щоб пояснити поведінку етанолу до і після додавання води, необхідно це знати
а) щільність рідин.
б) розмір молекул.
в) температура кипіння рідин.
г) атоми, присутні в молекулах.
д) тип взаємодії між молекулами.
Правильна альтернатива: д) тип взаємодії між молекулами.
Міжмолекулярні сили впливають на розчинність органічних сполук. Речовини, як правило, розчиняються між собою, коли вони мають однакову міжмолекулярну силу.
Дивіться в таблиці нижче кілька прикладів органічних функцій та типу взаємодії між молекулами.
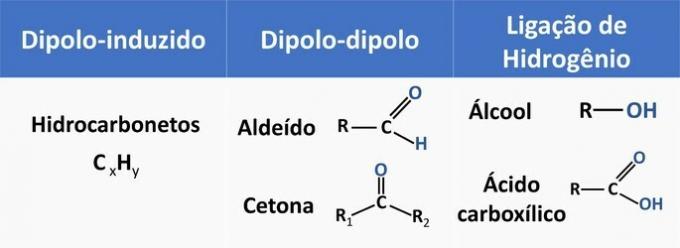
Етанол вважається полярним розчинником, оскільки у своїй структурі він має полярну групу (—ОН). Однак його вуглецевий ланцюг, будучи неполярним (СН), здатний взаємодіяти з неполярними розчинниками. Тому етанол розчиняється як у воді, так і в бензині.
Відповідно до цієї інформації ми маємо:
а) НЕПРАВИЛЬНО. Щільність пов’язує масу тіла із займаним об’ємом.
б) НЕПРАВИЛЬНО. Розмір молекул впливає на полярність сполук: чим більший вуглецевий ланцюг, тим неполярнішою стає речовина.
в) НЕПРАВИЛЬНО. Температура кипіння корисна для розділення молекул: дистиляція відокремлює сполуки з різною температурою кипіння. Чим нижча температура кипіння, тим легше випаровується молекула.
г) НЕПРАВИЛЬНО. Альдегід має у своїй структурі вуглець, водень та кисень. Ця сполука здійснює диполь-дипольні взаємодії, тоді як спирт, маючи ті самі елементи, здатний утворювати водневі зв’язки.
д) ПРАВИЛЬНО. Взаємодія етанолу з водою (водневий зв'язок) більш інтенсивна, ніж з бензином (індукована дипло).
питання 2
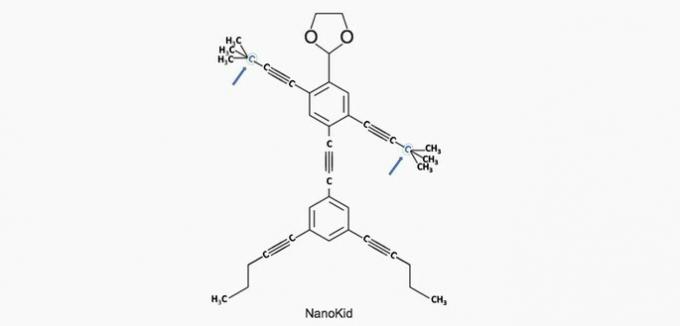
(Enem / 2013) Молекули нанопутяни вони нагадують людські фігури і були створені для стимулювання інтересу молоді до розуміння мови, вираженої в структурних формулах, широко використовуваних в органічній хімії. Прикладом є NanoKid, представлений на малюнку:
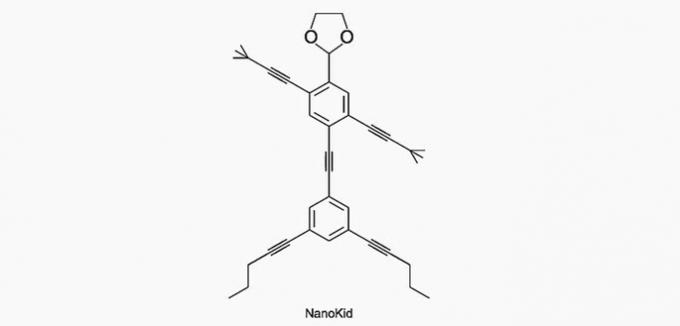
Де в організмі NanoKid є четвертинний вуглець?
а) Руки.
б) Голова.
в) Скриня.
г) Живіт.
д) Ноги.
Правильна альтернатива: а) Руки.
Вуглець класифікується наступним чином:
- Первинна: зв’язується з вуглецем;
- Вторинний: зв’язується з двома вуглецями;
- Третинний: пов'язується з трьома вуглеводами;
- Четвертинний: зв’язується з чотирма вуглецевими атомами.
Див. Приклади нижче.

Відповідно до цієї інформації ми маємо:
а) ПРАВИЛЬНО. Вуглець у руці пов'язаний з чотирма іншими вуглеводами, тому він є четвертинним.
б) НЕПРАВИЛЬНО. Голова складається з первинних вуглеводнів.
в) НЕПРАВИЛЬНО. Скриня складається з вторинного та третинного вуглецю.
г) НЕПРАВИЛЬНО. Черевце складається з вторинних вуглеводнів.
д) НЕПРАВИЛЬНО. Ноги складаються з первинних вуглеців.
питання 3
(Enem / 2014) Деякі полімерні матеріали не можуть бути використані для виробництва певних видів артефактів, як для обмеження механічних властивостей або легкістю, з якою вони зазнають деградації, утворюючи для цього небажані побічні продукти застосування. Отже, перевірка стає важливою для визначення природи полімеру, який використовується при виготовленні артефакту. Один з можливих методів заснований на розкладанні полімеру з отриманням мономерів, які його породили.
Контрольоване розкладання артефакту, що утворює діамін Н2N (СН2)6NH2 і кислота HO2C (СН2)4CO2H. Тому артефакт був виготовлений з
а) поліестер.
б) поліамід.
в) поліетилен.
г) поліакрилат.
д) поліпропілен.
Правильна альтернатива: б) поліамід.
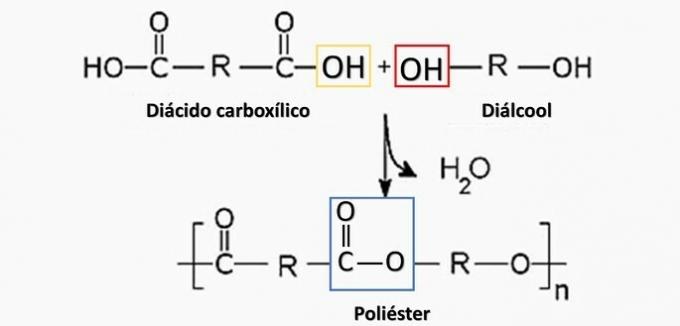
а) НЕПРАВИЛЬНО. Поліестер утворюється в реакції між дикарбоновою кислотою (—СООН) та спиртовим спиртом (—ОН).
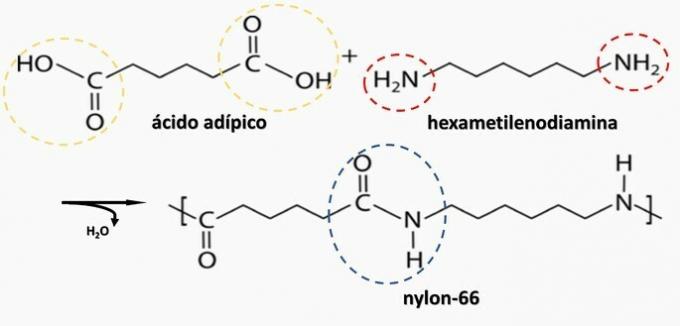
б) ПРАВИЛЬНО. Поліамід утворюється шляхом полімеризації дикарбонової кислоти (—COOH) з діаміном (—NH2).
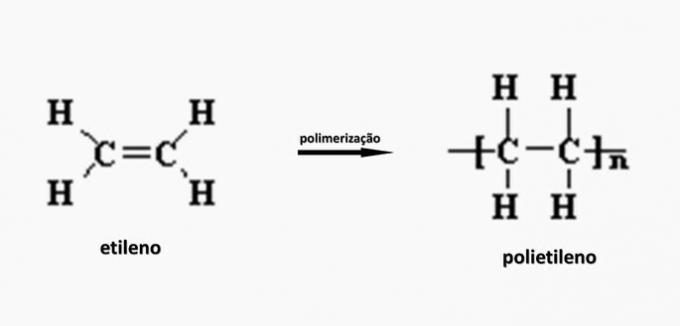
в) НЕПРАВИЛЬНО. Поліетилен утворюється при полімеризації мономеру етилену.
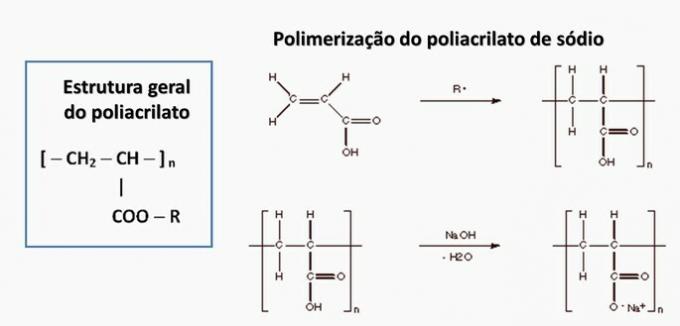
г) НЕПРАВИЛЬНО. Поліакрилат утворений сіллю, отриманою з карбонової кислоти.
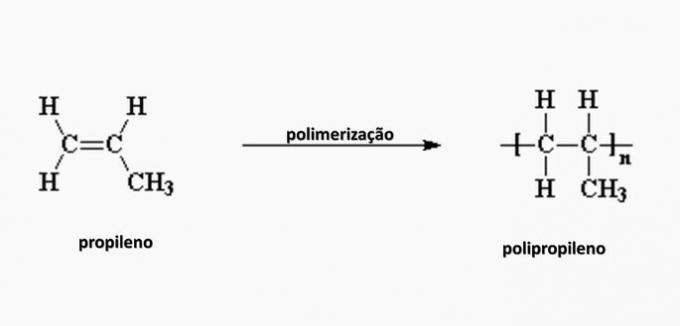
д) НЕПРАВИЛЬНО. Поліпропілен утворюється при полімеризації мономеру пропілену.
питання 4
(Enem / 2008) Китай зобов'язався відшкодувати Росію за вилив бензолу з промисловості Китайська нафтохімія в річці Сонгхуа, притоці річки Амур, яка є частиною кордону між ними країн. Президент Федерального агентства водних ресурсів Росії запевнив, що бензол не дійде до трубопроводів Росії питної води, але попросив населення кип’ятити проточну воду і уникати риболовлі в річці Амур та її притоки. Місцева влада зберігає сотні тонн вугілля, оскільки мінерал вважається ефективним поглиначем бензолу. Інтернет: (з адаптаціями). Беручи до уваги вжиті заходи щодо мінімізації шкоди навколишньому середовищу та населенню, це правильно стверджувати
а) вугілля, помістившись у воду, реагує з бензолом, усуваючи його.
б) бензол більш леткий, ніж вода, і тому його потрібно кип’ятити.
в) орієнтація на уникнення риболовлі зумовлена необхідністю збереження риби.
г) бензол не забруднює труби питної води, оскільки природним чином зливається на дні річки.
д) забруднення, спричинені розливом бензолу в китайській промисловості, будуть обмежені річкою Сонгхуа.
Правильна альтернатива: б) бензол є більш летким, ніж вода, і тому його потрібно кип'ятити.
а) НЕПРАВИЛЬНО. Вугілля містить у своїй структурі кілька пор і використовується як адсорбент, оскільки здатний взаємодіяти із забрудненнями і утримувати їх на своїй поверхні, але не усуваючи.
б) ПРАВИЛЬНО. Чим більша летючість речовини, тим легше вона переходить у газоподібний стан. Тоді як температура кипіння води становить 100 ° С, бензолу - 80,1 ° С. Це тому, що вода є полярною сполукою, а бензол - неполярною сполукою.
Тип взаємодії молекул різний і також впливає на температуру кипіння речовин. Молекула води здатна утворювати водневі зв’язки, тип взаємодії набагато сильніший, ніж той, який здатний утворювати бензол з індукованим диполем.
в) НЕПРАВИЛЬНО. У харчовому ланцюзі одна істота стає їжею іншої відповідно до взаємодії видів у певному місці. Коли токсична речовина потрапляє в навколишнє середовище, відбувається поступове накопичення і риба забруднений, потрапляючи в організм людини, може брати з собою бензол і викликати мутації ДНК і навіть навіть рак.
г) НЕПРАВИЛЬНО. Бензол має меншу щільність, ніж вода. Таким чином, тенденція полягає в тому, що навіть під водою воно продовжує поширюватися.
д) НЕПРАВИЛЬНО. Сезонні зміни можуть ще більше посилити проблему, оскільки низькі температури знижують здатність біологічного розкладу хімічних речовин під дією сонця або бактерій.
питання 5
(Enem / 2019) Вуглеводні - це органічні молекули, що мають ряд промислових застосувань. Наприклад, вони містяться у великих кількостях у різних нафтових фракціях і, як правило, розділяються фракційною дистиляцією залежно від температури кипіння. У таблиці представлені основні фракції, отримані при перегонці нафти при різних температурних інтервалах.
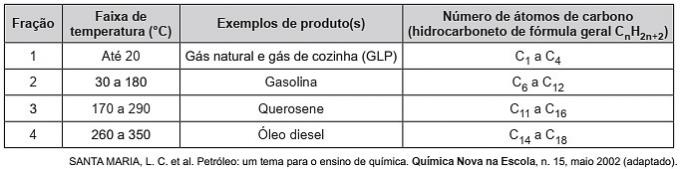
У фракції 4 поділ сполук відбувається при більш високих температурах, оскільки
а) їх щільність більша.
б) кількість гілок більша.
в) його розчинність у маслі більша.
г) міжмолекулярні сили більш інтенсивні.
д) вуглецевий ланцюг важче розірвати.
Правильна альтернатива: г) міжмолекулярні сили більш інтенсивні.
Вуглеводні взаємодіють під дією індукованого диполя, і цей тип міжмолекулярної сили посилюється із збільшенням вуглецевого ланцюга.
Отже, важчі фракції нафти мають вищу температуру кипіння, оскільки ланцюги сильніше взаємодіють через індукований диполь.
Докладніше про вправи з коментарем, див. Також:
- Вправи на вуглеводні
- Вправи на органічні функції
- Питання хімії в Enem



