Основними неорганічними функціями є: кислоти, основи, солі та оксиди.
Неорганічні сполуки мають різні властивості і присутні у багатьох ситуаціях у нашому повсякденному житті. З цієї причини ця тема багато обговорюється на вступних іспитах, в Enem та на змаганнях.
Щоб допомогти вам підготуватися до іспитів, ми створили цей список 15 питань з коментованими резолюціями та різними підходами до кожної неорганічної функції.
Загальні поняття
1. (FGV) Деякі сполуки, розчиняючись у воді, утворюють водний розчин, який проводить електрику. З сполук нижче:
| Я В2ТІЛЬКИ4 |
| II. О2 |
| III. Ç12H22О11 |
| IV. KNO3 |
| В. СН3КУХ |
| БАЧИВ. NaCl |
Вони утворюють водний розчин, який проводить електрику:
а) лише I, IV і VI
б) лише I, IV, V і VI
в) усі
г) лише я і VI
д) тільки пила
Правильна альтернатива: б) лише I, IV, V та VI.
Провідність електрики в розчині відбувається завдяки утворенню електрично заряджених видів - іонів, як це виявив Арреній у своїх експериментах.
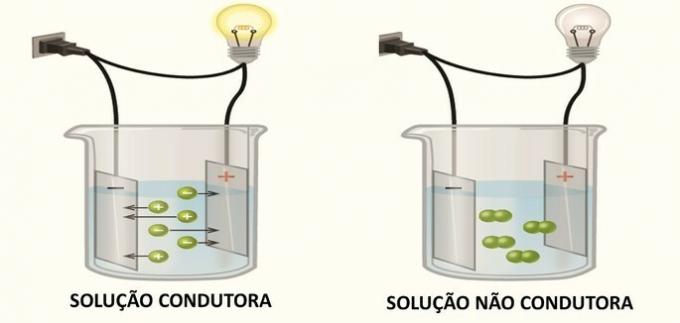
Коли іони утворюються в розчині, катіони (позитивний заряд) мігрують до негативного полюса та аніонів (негативний заряд) мігрують до позитивного полюса, замикаючи електричний ланцюг і дозволяючи пройти ланцюжок.
Сполуки, які у розчині утворюють нейтральні види, не проводять електрику.
Відповідно до цієї інформації ми маємо:
Я ПРИВІД
У розчині сіль дисоціює і утворюються іони.
II. НЕ ВОДИТЬ
Двохатомний кисень при кімнатній температурі є інертною молекулою.
III. НЕ ВОДИТЬ
Представлена формула призначена для сахарози, молекулярної сполуки, яка при контакті з водою її молекули розсіюються, але не втрачають своєї ідентичності.
IV. ПРИВІД
У розчині сіль дисоціює і утворюються іони.
В. ПРИВІД
Оцтова кислота - це слабка кислота, яка має невелику іонізовану частину в розчині.
БАЧИВ. ПРИВІД
У розчині сіль дисоціює і утворюються іони.
2. (Маккензі-СП)
Наведене вище рівняння являє собою реакцію
а) іонної дисоціації.
б) який має в якості реагенту двокислоту.
в) загальної іонізації, утворюючи катіон гідроксонію.
г) іонізації, утворюючи фосфідний аніон.
д) який при повній іонізації утворює одновалентний аніон.
Правильна альтернатива: в) повної іонізації, утворюючи катіон гідроксонію.
Фосфорна кислота - це хімічна сполука, яка іонізується при контакті з водою і виділяє іони Н+.
Іонізація відбувається у три етапи:
| Перший крок | |
| Другий етап | |
| третій крок | |
| сума кроків |
Катіони (H+), що виділяється, реагує з водою, утворюючи іон гідроксону (H3О+).
Відповідно до цього міркування ми повинні:
а) НЕПРАВИЛЬНО. Дисоціація відбувається в іонних сполуках, а фосфорна кислота є молекулярною сполукою.
б) НЕПРАВИЛЬНО. Фосфорна кислота є трикислотою, оскільки вона містить три іонізуються водню.
в) ПРАВИЛЬНО. Катіон гідроксонію, який також називають гідронієм, є видом, що утворюється в результаті з'єднання іонізуючого водню з водою.
г) НЕПРАВИЛЬНО. Вироблений аніон - фосфат (). Формула фосфіду:
д) НЕПРАВИЛЬНО. Утворений аніон () тривалентний, оскільки має 3-заряд.
3. Правильно пов’язуйте сполуки, наведені нижче, з відповідними неорганічними функціями.
| Я HBr, H3ПИЛ4 та H2CO3 | () кислоти |
| II. CO2, ТІЛЬКИ2 та Ал2О3 | () бази |
| III. Ал2(ОН)3, KOH та NH4ой | () солі |
| IV. NaCℓ, KNO3 та BaSO4 | () оксиди |
Кислоти - це сполуки, що мають іонізуючі водні.
(Я) кислоти: HBr, H3ПИЛ4 та H2CO3
Основи мають гідроксильний іон.
(III) бази: Al2(ОН)3, KOH та NH4ой
Солі - це іонні сполуки, утворені катіонами та аніонами.
(IV) солі: NaCℓ, KNO3 та BaSO4
Оксиди - це сполуки, що утворюються в результаті з’єднання кисню з іншими елементами, крім фтору.
(II) оксиди: CO2, ТІЛЬКИ2 та Ал2О3
Кислоти
4. Напишіть назву таких кислот:
а) HCl і HBr
Соляна кислота та бромиста кислота.
Вищевказані сполуки являють собою гідрати. Кислоти цього класу мають формулу НхA, де x являє собою кількість воднів (H), а A відповідає зв'язаному аметалу.
Номенклатура цих речовин складається наступним чином:
| H | Кл | |
| Кислота | Хлор | гідричний |
| Хлористого-воднева кислота |
| H | бр | |
| Кислота | Бром | гідричний |
| бромоводородна кислота |
б) HNO3 та HNO2
Азотна кислота та азотна кислота.
Вищевказані сполуки являють собою оксикислоти з двома окисними числами. Кислоти цього класу мають формулу НхАТ, утворюючись з водню, неметалу та кисню.
Номенклатура цих речовин складається наступним чином:
| H | N | О3 |
| Кислота | Нітрат | ich |
| Азотна кислота. Азот у цій сполуці становить +5. |
Найменшою сполукою Nox є азотна кислота: HNO2.
| H | N | О2 |
| Кислота | Нітрат | кістка |
| Азотна кислота. Азот у цій сполуці становить +3. |
в) HClO, HClO2, HClO3 і HClO4
Хлорна, хлорна, хлорна та хлорна кислоти.
Вищезазначені сполуки являють собою оксикислоти з чотирма окисними числами. Кислоти цього класу мають формулу НхAO, утворюючись з водню, кисню та неметалу з сімейства 7A.
Номенклатура цих речовин складається наступним чином:
| Nox +1 | Кислота | бегемот | префікс елемента | кістка |
| Nox +3 | Кислота | - | префікс елемента | кістка |
| Nox +5 | Кислота | - | префікс елемента | ich |
| Nox +7 | Кислота | за | префікс елемента | ich |
З'єднання, наведені в альтернативі, названі таким чином:
| H | Кл | О | |
| Кислота | бегемот | хлор | кістка |
| Соляна кислота. Норма хлору в цій сполуці становить +1. |
| H | Кл | О2 |
| Кислота | хлор | кістка |
| Хлорна кислота. Кількість хлору в цій сполуці становить +3. |
| H | Кл | О3 |
| Кислота | хлор | ich |
| Хлорна кислота. Кількість хлору в цій сполуці становить +5. |
| H | Кл | О4 | |
| Кислота | за | хлор | ich |
| Хлорна кислота. Норма хлору в цій сполуці становить +7. |
5. (UVA-CE) кислоти HClO4, H2MnO4, H3ПИЛ3, H4Субота2О7щодо кількості іонізуваних воднів можна класифікувати на:
а) монокислота, двокислота, трикислота, тетракислота.
б) монокислота, двокислота, трикислота, трикислота.
в) монокислота, двокислота, діацид, тетракислота.
г) монокислота, монокислота, діакислота, трикислота.
Правильна альтернатива: в) монокислота, діацид, діацид, тетракислота.
Іонізація представлених кислот відбувається наступним чином:
Структурні формули показують нам, що іонізуючі водні пов'язані з киснем.
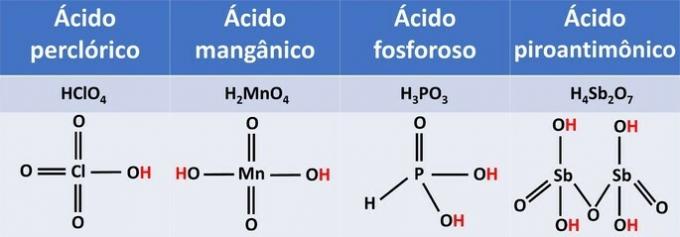
За кількістю іонізуючих воднів кислоти можна класифікувати на:
| HClO4 | іонізуючий водень | монокислота |
| H2MnO4 | Два іонізуються водню | двокислота |
| H3ПИЛ3 | Два іонізуються водню | двокислота |
| H4Субота2О7 | Чотири іонізуються водню | тетрацид |
Для оксикислот іонізуючими воднями є ті, які безпосередньо приєднані до кисню. Фосфорна кислота має один із трьох воднів, приєднаних до центрального елементу, фосфору, і тому є діацидною кислотою.
6. (UESPI) Нехай кислоти перераховані нижче із відповідними ступенями іонізації у відсотках (α%):
|
HClO4 (α% = 97%) |
H2ТІЛЬКИ4 (α% = 61%) |
H3BO3 (α% = 0,025%) |
H3ПИЛ4 (α% = 27%) |
HNO3 (α% = 92%) |
Перевірте правильність твердження:
а) Н3ПИЛ4 сильніший за Н2ТІЛЬКИ4.
б) HNO3 це м’яка кислота.
в) HClO4 слабший, ніж HNO3.
г) Н3ПИЛ4 це сильна кислота.
д) Н3BO3 це слабка кислота.
Правильна альтернатива: д) Н3BO3 це слабка кислота.
Значення відповідає ступеню іонізації і обчислюється за формулою:
Чим вище значення , тим сильніша кислота, оскільки це означає, що в розчин потрапляє більше іонізованих речовин.
Відповідно до цього міркування ми повинні:
а) НЕПРАВИЛЬНО. Чим вище значення , тим сильніша кислота. H2ТІЛЬКИ4 має вищий ступінь іонізації, ніж Н3ПИЛ4.
б) НЕПРАВИЛЬНО. HNO3 він має ступінь іонізації більше 90%. Це сильна кислота.
в) НЕПРАВИЛЬНО.4 має вищий ступінь іонізації, ніж HNO3 будучи, отже, сильнішим за нього.
г) НЕПРАВИЛЬНО. H3ПИЛ4 це помірна кислота, оскільки вона має ступінь іонізації від 5% до 50%.
д) ПРАВИЛЬНО. H3BO3 він має ступінь іонізації менше 5% і тому є слабкою кислотою.
Основи
7. Введіть назву таких основ:
а) LiOH і Be (OH)2
Гідроксид літію та гідроксид берилію.
Представлені бази мають фіксований заряд, і тому номенклатура складається наступним чином:
LiOH: гідроксид літію.
Будь (ОН)2: гідроксид берилію.
б) CuOH і Cu (OH)2
Гідроксид купруму та гідроксид міді.
Мідь має два окислювальні числа: +1 і +2. Один із способів назвати змінну nox base такий:
| Nox +1 | CuOH | купрум гідроксид |
| Nox +2 | Cu (OH)2 | гідроксид міді |
в) Sn (OH)2 і Sn (OH)4
Гідроксид олова (II) та гідроксид олова (IV).
Олово має два окислювальні числа: +2 та +4. Номенклатура змінної основи nox також може бути виконана наступним чином:
| Nox +2 | Sn (OH)2 | Гідроксид олова II |
| Nox +4 | Sn (OH)4 | Гідроксид олова IV |
8. (Fiam-SP) Для боротьби з кислотністю шлунка, спричиненою надлишком соляної кислоти, прийнято приймати всередину антацид. З наведених нижче речовин, що містяться у повсякденному житті людей, найбільш придатними для боротьби з кислотністю є:
а) сода.
б) апельсиновий сік.
в) вода з лимоном.
г) оцет.
д) молоко магнезії.
Правильна альтернатива: д) магнезіальне молоко.
Антациди - це речовини, що використовуються для підвищення рН шлунку, оскільки надлишок соляної кислоти спричинює зниження рН і, як наслідок, підвищення кислотності.
Для боротьби з кислотністю шлунка рекомендується приймати всередину речовина з основним характером, оскільки при взаємодії зі шлунковою кислотою вона виробляє нейтралізуючу реакцію, утворюючи сіль і воду.
Відповідно до цього міркування ми повинні:
а) НЕПРАВИЛЬНО. Соду використовувати не можна, оскільки вона містить вугільну кислоту у своєму складі.
б) НЕПРАВИЛЬНО. Апельсин використовувати не можна, оскільки він містить у своєму складі лимонну кислоту.
в) НЕПРАВИЛЬНО. Лимон використовувати не можна, оскільки він містить у своєму складі лимонну кислоту.
г) НЕПРАВИЛЬНО. Оцет застосовувати не можна, оскільки він містить у своєму складі оцтову кислоту.
д) ПРАВИЛЬНО. Слід використовувати молоко магнезії, оскільки воно містить в своєму складі основу гідроксиду магнію.
Утворюється реакція нейтралізації:
9. (Осек) Сильна база, мабуть, пов’язана з групою ОН-:
а) дуже електропозитивний елемент.
б) дуже електронегативний елемент.
в) напівметалу.
г) метал, що дає 3 електрони.
д) неметалевий.
Правильна альтернатива: а) дуже електропозитивний елемент.
Міцною основою є та, яка має високий ступінь дисоціації, тобто вільні гідроксильні іони в розчині.
Іон гідроксилу має негативний заряд, оскільки йому вдається залучити електрон до себе при дисоціації через електронегативність кисню.
Таким чином, дуже електропозитивний елемент має здатність втрачати електрони і віддавати їх гідроксилу, залишаючись у катіонній формі в розчині.
а) ПРАВИЛЬНО. Дуже електропозитивні елементи, такі як лужні метали та лужноземельні метали, утворюють міцні основи.
б) НЕПРАВИЛЬНО. Елемент, більш електронегативний, ніж кисень, спричинив би сутичку за електрон.
в) НЕПРАВИЛЬНО. Напівметал має велику електронегативність.
г) НЕПРАВИЛЬНО. Іон гідроксилу має 1-заряд. метал, який дає 3 електрони, утворить основу з 3 гідроксилами.
Приклад:
д) НЕПРАВИЛЬНО. Найсильнішими основами є основи, утворені металами.
солі
10. Напишіть назву таких солей:
a-N-A2CO3
Карбонат натрію.
Це тип нейтральної солі, і її номенклатура подана наступним чином:
| аніон | катіон |
| В+ | |
| карбонат | натрію |
| Карбонат натрію |
б) KNaSO4
Сульфат натрію та калію.
Це тип подвійної солі, і її номенклатура така ж, як і нейтральна сіль, і назви двох катіонів написані.
| аніон | катіони | |
| К+ | В+ | |
| Сульфат | калію | натрію |
| Сульфат натрію та калію |
в) NaHCO3
Моноводень карбонат натрію.
Це тип кислотної солі, і її номенклатура подана наступним чином:
| Кількість воднів | аніон | катіон |
| 1 | В+ | |
| Мононуклеоз | карбонат | натрію |
| Моноводень натрію карбонат |
Популярна назва цієї сполуки - бікарбонат натрію.
г) Al (OH)2Кл
Дигідроксихлорид алюмінію.
Це тип основної солі, і її номенклатура подана наступним чином:
| Кількість гідроксилів | аніон | катіон |
| 2 | Кл- | Ал3+ |
| Ді | хлорид | алюміній |
| Дигідроксіхлорид алюмінію |
Ця сполука також відома як двоосновний хлорид алюмінію.
д) CuSO4. 5 годин2О
Пентагідрат мідного сульфату.
Це тип гідратованої солі, і її номенклатура подана наступним чином:
| аніон | катіон | кількість молекул води |
| Дупу2+ | 5 | |
| Сульфат | мідь | пента |
| Пентагідрат мідного сульфату |
11. (Unirio) Солі - це також продукти, отримані реакцією повної або часткової нейтралізації іонізуючих воднів кислот з основами або гідроксидами, відповідно до загальної реакції:
Кислота + основа Сіль + вода
Виходячи з цього твердження, яка єдина кислота, яка не має усіх пов’язаних з нею можливих продуктів?
а) соляна кислота утворює лише нейтральну хлоридну сіль.
б) азот виробляє лише нейтрально-нітратну сіль.
в) фосфорний утворює лише нейтральну фосфатну сіль.
г) сульфід може утворювати або нейтральну сульфідну сіль, або кислотну сіль, сульфід кислоти або сірководень.
д) сірчана може утворювати або нейтральну сульфатну сіль, або кислу сіль, кислий сульфат або гідросульфат.
Неправильна альтернатива: в) фосфорний утворює лише нейтральну фосфатну сіль.
а) ПРАВИЛЬНО. Соляна кислота має лише один іонізуючий водень, який реагуватиме на утворення води. Потім сіль утворюється аніоном кислоти, в даному випадку хлоридом, і катіоном основи.
Приклади:
б) ПРАВИЛЬНО. У азотній кислоті є лише один іонізуючий водень, який реагуватиме на утворення води. Потім сіль утворюється аніоном кислоти, в даному випадку нітратом, і катіоном основи.
Приклади:
в) НЕПРАВИЛЬНО. Фосфорна кислота має три іонізуються водню і, отже, вона може зазнавати часткову або повну іонізацію. У цьому випадку можуть утворюватися три типи солей:
- Повна нейтралізація, що генерує a нейтральна сіль:
- Часткова нейтралізація, що генерує a кисла сіль:
- Часткова нейтралізація, що генерує a основна сіль:
г) ПРАВИЛЬНО. При повній нейтралізації утворюється нейтральна сіль, а при частковій - кисла.
- Повна нейтралізація:
- Часткова нейтралізація:
д) ПРАВИЛЬНО. При повній нейтралізації утворюється нейтральна сіль, а при частковій - кисла.
- Повна нейтралізація:
- Часткова нейтралізація:
| Я В2B4О7.10 год2О | THE. основна сіль |
| II. Mg (OH) Cl | Б. подвійна сіль |
| III. NaKSO4 | Ç. кисла сіль |
| IV. NaHCO3 | Д. гідратована сіль |
Правильна асоціація між ними:
а) AI, BIII, CIV, DII
б) AII, BIV, CIII, DI
в) AI, BII, CIII, DIV
г) AII, BIII, CIV, DI
Правильна альтернатива: г) AII, BIII, CIV, DI
| ІІ. основна сіль: Mg (OH) Cl | У своїй структурі він має гідроксил. |
| BIII. подвійна сіль: NaKSO4 | У своїй структурі він має два катіони металу. |
| CIV. кисла сіль: NaHCO3 | У своїй структурі він має водень. |
| DI. гідратована сіль: Na2B4О7.10 год2О | У своїй структурі він має молекули води. |
Оксиди
13. Напишіть назву таких оксидів:
сталь2 і ні2О3
Двоокис вуглецю та триоксид азоту.
Ці оксиди є молекулярними оксидами, оскільки кисень зв’язаний з неметалами. Номенклатура для цього класу складається наступним чином:
| кількість кисню | Кількість вуглеців |
| 2 | 1 |
| Двоокис вуглецю або вуглекислий газ |
| кількість кисню | Кількість азотів |
| 3 | 2 |
| триоксид азоту |
б) Ал2О3 і далі2О
Оксид алюмінію та оксид натрію.
Ці оксиди є іонними оксидами, оскільки кисень зв’язується з металами. Метали, пов'язані з киснем, мають фіксований заряд. Тому номенклатура для цього класу складається наступним чином:
Ал2О3: оксид алюмінію
В2O: оксид натрію
б) Cu2O і CuO
Оксид міді I та оксид міді II.
Ці оксиди є іонними оксидами, оскільки кисень зв’язаний з металом. Метал, зв’язаний з киснем, має змінний заряд. Один із способів назвати цей клас такий:
| Nox +1 | Дупу2О | оксид міді I |
| Nox +2 | CuO | оксид міді II |
в) FeO та Fe2О3
Оксид заліза та оксид заліза.
Ці оксиди є іонними оксидами, оскільки кисень зв’язаний з металом. Метал, зв’язаний з киснем, має змінний заряд. Номенклатуру змінного оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду оксиду (NOx) також можна зробити наступним чином:
| Nox +2 | FeO | оксид заліза |
| Nox +3 | Віра2О3 | оксид заліза |
14. (UEMA) Нейтральні атоми певного репрезентативного елемента M мають два електрони у своїй валентній оболонці. Правильні формули для нормального оксиду та броміду:
(Дані: O = 6A та Br = 7A.)
а) М2O та MBr
б) МО2 та MBr2
в) MO та MBr2
г) М2О2 в2бр
в2O та MBr2
Правильна альтернатива: в) MO та MBr2
М-елементи мають два електрони у валентній оболонці. Для зв’язку з іншими елементами він може втратити ці два електрони і утворити катіон М.2+.
Кисень належить до сімейства 6A і йому потрібні ще 2 електрони, щоб набути стійкості за допомогою електронної конфігурації благородного газу, як це визначено правилом октету.
Так само брому, який є з сімейства 7А, потрібен лише 1 електрон, щоб мати 8 електронів у валентній оболонці.
Відповідно до цієї інформації ми маємо:
а) НЕПРАВИЛЬНО. Для утворення сполуки M2O та MBr, елемент M повинен утворювати катіон M+.
б) НЕПРАВИЛЬНО. Кисень має 2-, а не 1- заряд, як це представлено при утворенні сполуки МО2.
в) ПРАВИЛЬНО. Відповідно до валентності іонів альтернатива є правильною.
г) НЕПРАВИЛЬНО. Бромід має 1-, а не 2- заряд, як показано при утворенні сполуки М2Br.
д) НЕПРАВИЛЬНО. Катіон елемента має заряд 2+, а не заряд 1+, як показано при утворенні М сполуки.2О.
15. (PUC-MG) Зверніть увагу на хімічні реакції нижче:
| Я MgO + H2О |
| II. CO2 + H2О |
| III. К2O + 2HCl |
| IV. ТІЛЬКИ3 + 2NaOH |
Неправильне твердження:
а) Реакції II та IV включають оксиди кислот або ангідриди.
б) У реакціях I та III беруть участь основні оксиди.
в) Сіль, що утворюється в реакції IV, називається сульфатом натрію.
г) Сіль, що утворюється в реакції III, називається хлоридом калію.
д) Основний характер оксидів підкреслюється, коли кисень зв’язується з більшою кількістю електронегативних елементів.
Неправильна альтернатива: д) Основний характер оксидів зростає в міру зв’язування кисню з більшою кількістю електронегативних елементів.
а) ПРАВИЛЬНО. Коли кислі оксиди, такі як діоксид вуглецю та триоксид сірки реагують з водою, вони утворюють кислоту в розчині.
б) ПРАВИЛЬНО. При взаємодії з водою основні оксиди, такі як оксид магнію та оксид калію, утворюють основу в розчині.
в) ПРАВИЛЬНО. В2ТІЛЬКИ4 є формулою сульфату натрію.
г) ПРАВИЛЬНО. KCl - це формула хлористого калію.
д) НЕПРАВИЛЬНО. Основний характер оксидів підкреслюється, оскільки кисень зв'язується з більшою кількістю елементів. електропозитивні, як лужні та земно-лужні метали, оскільки при реакції з водою вони утворюють сильні основи, а при взаємодії з кислотами утворюють сіль і воду.