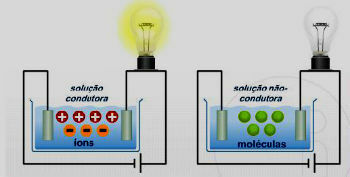
Moleküllerin polaritesi çok önemli bir husustur, çünkü maddelerin özellikleri, diğer faktörlerin yanı sıra, moleküllerinin polar veya polar olmaması gerçeğiyle belirlenir.
Bir molekülün polaritesinin belirlenmesi şu şekilde yapılabilir: Dipol Momenti veya Sonuç Dipol Momenti, kimin sembolü 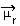 . Moleküldeki her bağın sadece dipol momentinden bahsediyorsak, sembol Yunanca mi (µ) harfidir.
. Moleküldeki her bağın sadece dipol momentinden bahsediyorsak, sembol Yunanca mi (µ) harfidir.

Dipol momenti sıfıra eşitse molekül polar olmayacaktır, ancak sıfır değilse polar olduğu anlamına gelir.

Ortaya çıkan bu dipol momenti belirlemede dikkate alınması gereken iki önemli şey vardır. Bakalım neymişler:
1) elektronegatiflik farkı Reaksiyona katılan elementlerin atomları arasında. Örneğin, flor bağdaki elektron çiftini hidrojenden çok daha fazla çektiği için, HF molekülünün elektronegatiflikte belirgin bir farkı vardır. Bu nedenle, elektrik dipolleri ile yüklerin dağılımı simetrik değildir.
Bu dipol, en çok elektronu, yani en az elektronegatif atomu yoğunlaştıran uca bakan bir vektör ile temsil edilir. Dolayısıyla, bu durumda, tek olan vektör, aşağıda belirtildiği gibi ortaya çıkan vektör olacaktır:
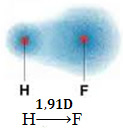
Vektör değerinin debye biriminde (D=3.33.3) verilen dipol momenti ile aynı olduğuna dikkat edin. 10-30 kulomb. metro). Dipol momenti sıfır olmadığı için molekül ve bağ kutupsal.
Şimdi durma... Reklamdan sonra devamı var ;)
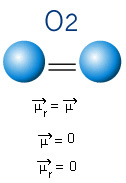
Aşağıdaki molekülde de sadece iki atomlu bir molekülümüz var, ancak bu durumda basit bir maddeye karşılık geliyor, yani sadece bir tür elementten oluşuyor. Dolayısıyla elektronegatiflik farkı yoktur; atomlar ayrıca simetrik olarak dağılmış elektronları da çeker. Ortaya çıkan dipol momenti sıfıra eşittir, dolayısıyla hem bağ hem de molekül apolar.
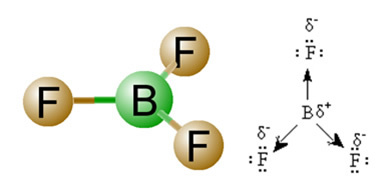
2) Molekül Geometrisi, yani vektörlerin uzamsal düzenlemesi. BF molekülü3 florun en elektronegatif olduğu üç polar bağa sahiptir, bu nedenle vektörler ona doğru yönlendirilir. Ancak atomların uzamsal dizilimi düz üçgen olduğundan, bu durum elektronların merkez atom etrafında simetrik bir dağılıma sahip olmasını sağlar. Böylece sonuç, bu üç vektörün birbirini yok etmesi ve dipol momentinin sıfıra eşit olmasıdır. Bu nedenle, BF molekülü3 é özür dilemek.
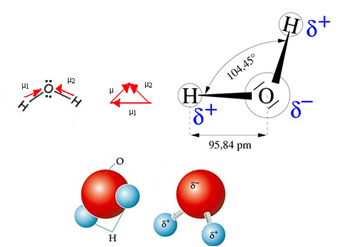
Su molekülünün iki vektörü vardır, ancak uzaysal geometrisi düz değil, V şeklindedir. Aşağıdaki şekilde vektörlerinin birbirlerini iptal etmediğini, elektronların asimetrik olarak dağıldığını ve en elektronegatif atom olan oksijende daha konsantre olduğuna dikkat edin. Böylece dipol momenti sıfırdan farklıdır ve su molekülü kutupsal:
Jennifer Foğaça tarafından
Kimya mezunu