Bir kimyasal reaksiyonun gerçekleşmesi için dört temel koşulun karşılanması gerekir, bunlar:
1. Reaktifler;
2. Reaktifler arasında kimyasal afinite olmalıdır;
3. Reaktif partikülleri arasındaki çarpışmalar etkili olmalıdır;
4. Aktivasyon enerjisine ulaşılmalıdır.
Her bir duruma kısaca bakın:
1.Reaktifler arasındaki temas:
Bu durum açıktır, çünkü tepkenler asitler ve bazlar durumunda olduğu gibi birbirlerine çok fazla afiniteye sahip olsalar bile ayrılırlarsa reaksiyon gerçekleşmez. Parçacıklarının çarpışabilmesi, tepkenlerin bağlarını kırabilmesi ve ürünlerin bağlarını oluşturabilmesi için temas kurmaları gerekir.

2.Kimyasal afinite:
Gördüğümüz gibi, reaktiflerin temas ettirilmesi gereklidir, ancak yeterli değildir. Örneğin sodyumu suyla temas ettirirsek son derece şiddetli bir reaksiyon oluşur ama altın koyarsak hiçbir fark görmeyeceğiz. Bunun nedeni, farklı maddelerin birbirleriyle farklı kimyasal afiniteleri olması veya hiç afiniteleri olmamasıdır. Kimyasal afinite ne kadar büyük olursa, reaksiyon o kadar hızlı olur.
Bahsedilen örneklerde sodyumun su ile ilgisi o kadar fazladır ki, havadaki nem ile temas etmemesi için metalik sodyum gazyağı içinde depolanır. Altın hareketsizdir, bu yüzden Mısır lahitleri gibi altın anıtlar bu kadar uzun süre dayanır.

3.Çarpışma teorisi:
Kimyasal afinitesi olan bileşiklerde bile reaksiyonun devam etmesi için partiküllerinin, atomlarının veya moleküllerinin etkili bir şekilde çarpışması gerekir. Çarpışan tüm parçacıklar bunu etkili bir şekilde yapmaz, ancak kırılmayla sonuçlanan şoklar. reaktif bağları ve yeni bağların oluşumu, doğru yönde ve enerji ile meydana gelenlerdir. yeter.
Şimdi durma... Reklamdan sonra devamı var ;)
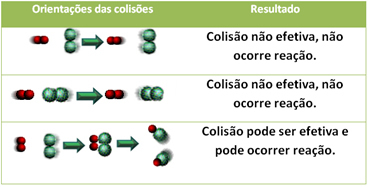
Aşağıda, reaksiyonun meydana gelmesiyle sonuçlanan iki etkisiz çarpışma ve bir etkili çarpışma durumu gösterilmiştir.
4.Aktivasyon enerjisi ve aktive kompleksi:
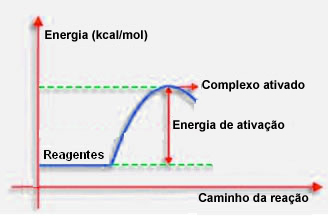
Bir önceki maddede belirtildiği gibi, etkili çarpışma, elverişli kılavuzluğun yanı sıra yeterli enerjiye ihtiyaç duyar. Her tepkimenin gerçekleşmesi için gereken minimum enerji miktarına aktivasyon enerjisi denir.
İyi yönlendirilmiş şok sırasında, reaktanların aktivasyon enerjisine eşit veya daha büyük bir enerjisi varsa, reaktanlar ve reaktanlar arasında bir ara yapı olan başlangıçta aktive olan bir kompleks oluşacaktır Ürün:% s. Aktive edilmiş komplekste zayıflamış reaktif bağları ve yeni ürün bağları oluşur.
Böylece aktivasyon enerjisi, reaksiyonun gerçekleşmesi için bir tür bariyer görevi görür, çünkü ne kadar büyükse, reaksiyonun gerçekleşmesi o kadar zor olacaktır. Bazı durumlarda reaktiflere enerji sağlamak gerekir. Örneğin, pişirme gazının havadaki oksijenle etkileşime girme afinitesi vardır, ancak kibriti bir araya getirdiğimizde enerji sağlamamız gerekir, aksi takdirde reaksiyon gerçekleşmez. Ancak bir kez başladığında, reaksiyonun kendisi diğer molekülleri aktive etmek ve reaksiyonun devam etmesini sağlamak için yeterli enerjiyi serbest bırakır.
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "Kimyasal Reaksiyonların Oluşma Koşulları"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/condicoes-para-ocorrencia-reacoes-quimicas.htm. 27 Haziran 2021'de erişildi.