Maddelerin molekülleri, sanki tek bir düzlemdeymiş gibi, hepsi düz değildir. Ne de olsa uzayda dağılmışlardır ve atomları farklı düzenlemeler veya düzenlemeler alırlar. Böylece her madde türünün molekülleri için farklı geometrik şekiller vardır.
Bir molekülün geometrisini belirlemenin en basit yollarından biri, değerlik kabuğu elektron çiftlerinin (RPECV) itilmesi. Bu teoriye göre, merkezi atomun elektron çiftleri şu şekilde işlev görür: elektronik bulutlar birbirini iten şey. Bu şekilde birbirlerinden mümkün olduğunca uzağa yönlendirilirler. Moleküler geometri, merkezi atomun etrafındaki elektronik çiftlerin sayısına bağlı olacaktır.
Bu elektronik bulut, bağlara katılan (tekli, ikili veya üçlü) ve katılmayan elektronlardan oluşabilir. Böylece sahibiz:
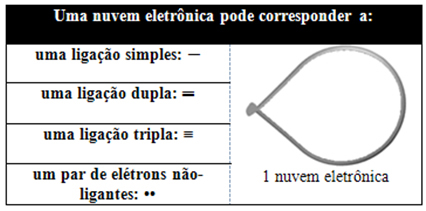
Bu bulutu, merkezinde merkezi atom bulunan bağlı bir balon veya balon olarak düşünmek yardımcı olur. Örneğin, merkezi atomun etrafında yalnızca iki elektron bulutu bulunan bir molekülde, daha büyük aralarındaki olası mesafe 180º'lik bir açıdır ve sonuç olarak molekülün geometrisi olacaktır. doğrusal.
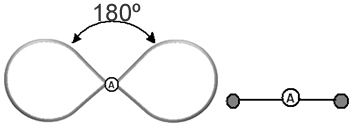
Bu nedenle, çoğu molekülün moleküler geometrisinin nasıl olacağı hakkında bir çıkarımda bulunabiliriz. moleküllerdeki atom sayısı ve merkez atomun yaptığı bağlar, molekül çiftlerinin olup olmadığını kontrol eder. elektronlar.
Aşağıdaki örneklere bakın:
- 2 atomlu moleküller: her zaman olacak doğrusal
Örneğin:
H ─ H, H ─ Cl, F ─ F, O = O, C ≡ O.
- 3 atomlu molekül: köşeli veya üçgen
eğer merkez atom bir çift bağlanmayan elektrona sahip olmak geometri olacak açısalSO molekülünde olduğu gibi2:
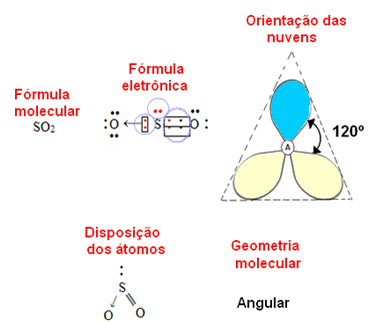
Mavi elektron bulutunun bağlara katılmayan elektron çiftlerini temsil ettiğini ve sarı olanı ise bağlara katılan elektron çiftleri olarak düşünün.
- 4 atomlu molekül: düzlem trigonal (veya üçgen) veya piramidal (veya trigonal piramit)
Merkez atomun eşleşmemiş (bağ olmayan) bir elektron çifti yoksa, moleküler geometri düz üçgendir (veya üçgen). BF örneğine bakın3:

Atomun bağlayıcı olmayan elektron çiftleri varsa, molekülün geometrisi amonyak durumunda olduğu gibi piramidal (veya trigonal piramit) olacaktır:

- 5 atomlu molekül: dört yüzlü
Metan Geometrisi Örneği:
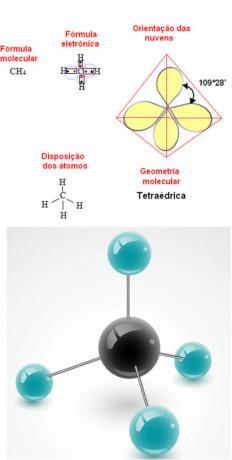
- 6 atomlu molekül: üçgen bipiramit veya üçgen piramit.
Bir örnek fosfor pentaklorürdür (PCI5), fosfor ve klor arasında 90º'lik ve diğerleri 120º'lik bir açıyla bazı bağlantıları olan, üçgen tabanlı bir çift piramit oluşturan:
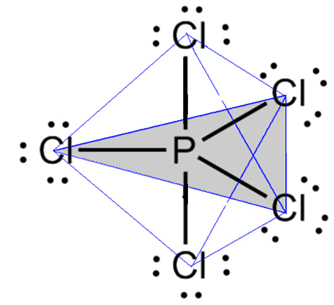
- 7 atomlu molekül: oktahedral
Örnek: kükürt heksaflorür (SF6), açıları 90º olan.

Jennifer Foğaça tarafından
Kimya mezunu
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/quimica/determinacao-geometria-das-moleculas.htm
