Küçük harflerin dengeli reaksiyon katsayılarına karşılık geldiği ve büyük harflerin reaktanlar olduğu ve ürünlerin hepsinin gaz olduğu aşağıdaki genel tersinir reaksiyonu düşünün:

Reaksiyon yönlerinin her biri ayrı ayrı ele alındığında gelişme hızları (Td) şu şekilde verilir:
*Doğrudan reaksiyon: aA + bB → cC + dD
Herşeydoğrudan = Kdoğrudan. [BU]. [B]B
*Ters reaksiyon: cC + dD → aA + bB
Herşeyters = Ktersine çevirmek. [Ç]ç. [D]d
Madde miktarındaki konsantrasyon cinsinden kimyasal denge sabiti (Kç) ve kısmi basınç açısından (KP) K'ye bölünerek verilecektirdoğrudan K tarafındantersine çevirmek.
Böylece sahibiz:
Kdoğrudan. [BU]. [B]B = 1 → Kdoğrudan__ = __[Ç]ç. [D]d___
Ktersine çevirmek. [Ç]ç. [D]d Ktersine çevirmek [BU]. [B]B
olmak, Kç =_Kdoğrudan_
Ktersine çevirmek
Böylece sahibiz:
Kç =__[Ç]ç. [D]d___ veya KP =__(Praça)ç. (pD)d___ |
Burada p, dengedeki her maddenin kısmi basıncıdır.
Bu şekilde, her konsantrasyon reaksiyondaki ilgili maddenin katsayısına karşılık gelen bir üsse yükseltilir ve Kç birimi yoktur*.
Ayrıca vurgulanması gereken çok önemli bir husus da bu ifadedene katı bileşenler ne de saf sıvılar temsil edilmemelidir., çünkü sadece varyasyona maruz kalabilen maddeler bu ifadeye katılır. Katı haldeki bir maddenin madde miktarındaki konsantrasyonu sabittir ve bu nedenle zaten K'nin kendi değerine dahil edilmiştir.ç. Aynı şey su gibi saf sıvılar için de geçerlidir. Kısacası, sadece gaz halindeki ve sulu çözeltideki maddeler ifadeye katılır.
Şimdi durma... Reklamdan sonra devamı var ;)
Aşağıdaki örneklere dikkat edin:
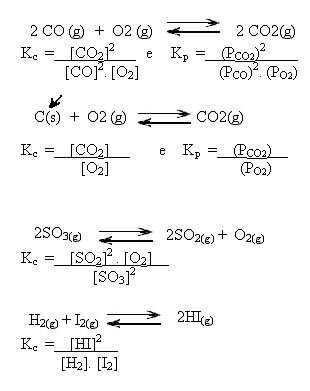
K değerleriç tepkenlerin ve ürünlerin konsantrasyonunun aynı olup olmadığını veya birinin diğerinden daha büyük olup olmadığını bize gösterebilir:
- Eğer Kç veya KP bire eşittir (Kç = 1), bu, reaktanların ve ürünlerin konsantrasyonunun eşit olduğu anlamına gelir;
- değeri ise Kç veya KP uzun ol, bu, ürünlerin daha büyük konsantrasyonda olduğu anlamına gelir, çünkü K ifadesindeç ürünler payda;
- değeri ise Kç veya KP düşük, bu, reaktiflerin daha yüksek konsantrasyonda olduğu anlamına gelir, çünkü K ifadesindeç reaktifler paydadadır.
*Kç ve KP bunlar boyutsuz sayılardır, yani herhangi bir büyüklükle veya büyüklükler arasındaki ilişkiyle ilgili birimi olmayan saf sayılardır.
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "Denge Sabitleri Kc ve Kp"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm. 28 Haziran 2021'de erişildi.


