Ö Thomson atom modeli 1898 yılında İngiliz fizikçi Joseph John Thomson veya basitçe J.J. Thomson tarafından önerildi. birkaç sahip olduktan sonra elektronun varlığına dair deneysel kanıttarafından önerilen atomun bölünmezliği teorisini alt üst etti. John Dalton.
Thomson, modeline dayanarak, varlığını doğruladı ve kanıtladı. elektronlar (negatif elektrik yüklü parçacıklar) atomda, yani atomda atom altı parçacıklar bulunur.
Zihin Haritası: Thomson Atom Modeli
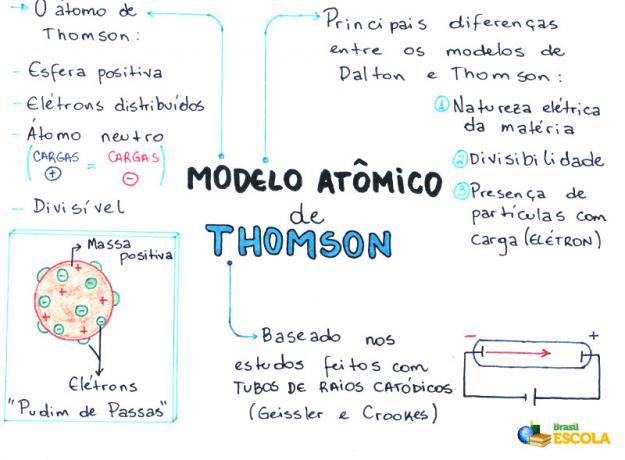
* Zihin haritasını PDF olarak indirmek için, Buraya Tıkla!
Thomson atom modelini önerdi bilim adamları Geissler ve Crookes tarafından inşa edilen katot ışın tüpü ile yapılan deneyler ve radyoaktivite ile ilgili keşiflere dayanmaktadır. Bu tüpün bir temsiline bakın:
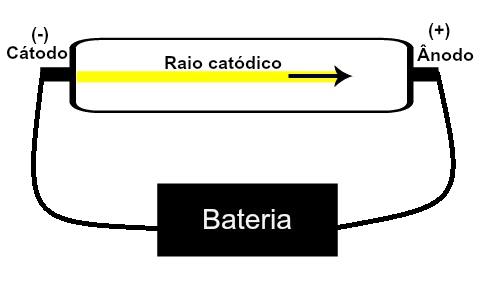
Nadir, düşük basınçlı bir gaz, yüksek bir elektrik voltajına (örn. 15000 V) maruz kaldığında, bir katottan (negatif kutup) anoda (kutup) doğru ışık demeti (elektrik yüklerinden oluşur) pozitif).
Thomson, bu deneyle, gaz halindeki maddenin atomlarının içerdeki yüksek voltaja maruz bırakılmış, elektronları kopmuş ve plakaya yönlendirilmiştir. pozitif.
Thomson atom modeli tarafından önerilen hususlar
Thomson, katot ışın tüpü ile yaptığı deneylerle atomun ve yapısının nasıl olacağına dair kendi yorumunu önerdi. Yani ona göre:
- Atom bir küredir, ancak önerildiği gibi kütleli değildir. John Dalton atom modeli;
- Atom nötrdür, çünkü tüm maddeler nötrdür;
- Atomun negatif yüklü elektronları olduğundan, son yükün sıfır olması için pozitif parçacıklara sahip olması gerekir;
- Elektronlar atomda sabit veya hapsolmuş değildir, belirli koşullar altında başka bir atoma aktarılabilirler;
- Atom, negatif yüklü elektronların dağıtılacağı pozitif yüklü sürekli bir sıvı olarak düşünülebilir;
- ilişkilendirdi kuru üzümlü puding için model (elektronları temsil eden);
- Saçılan elektronlar aynı yüke sahip olduklarından, aralarında karşılıklı bir itme vardır ve bu da onları küre içinde eşit olarak dağıtır.
Thomson modelinin atoma önerdiği yenilikler
Thomson'ın atom modeli, atom için önerilen ikinci modeldi. İlk model John Dalton tarafından formüle edilmiştir.
Şimdi durma... Reklamdan sonra devamı var ;)
Thomson'ın modeli, atom hakkında o zamana kadar bilimsel temeli olmadığı için önerilmeyen yeni bilgilerle ilgiliydi, örneğin:
- Maddenin elektriksel doğası;
- Atomun bölünebilirliği;
- Atomda küçük, yüklü parçacıkların varlığı.
Thomson atomuna işaret edilen problemler
Önerinin yapıldığı sırada birkaç fizikçi Thomson atom modeli, Klasik Fizik teorilerine dayanarak, bu modelde bulunan bazı tutarsızlıklara dikkat çekti:
- Thomson, atomun, enerjinin etkisiyle değiştirilebilen elektronların düzgün dağılımı ile ilgili olarak bir kararlılığa sahip olduğunu öne sürdü. Ancak, Klasik Fizik, elektromanyetizma, sadece aynı yüke sahip parçacıklar arasındaki itmeye dayalı kararlı bir sistemin varlığına izin vermez;
- Thomson'a göre elektronlar atomda eşit olarak dağılmıştır, ancak hızlandırılmış bir şekilde kayması ve bu nedenle belirli frekanslarda elektromanyetik radyasyon yayması gerekir özel. Ancak bu gözlenmedi.
- Thomson'ın modeli, bileşimleri ve organizasyonları gibi atomik özellikleri açıklamada genellikle etkisizdi.
* Victor Ricardo Ferreira'nın Zihin Haritası
Kimya hocası
Benden Diogo Lopes Dias
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
GÜNLER, Diogo Lopes. "Thomson Atom Modeli"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/o-atomo-thomson.htm. 27 Haziran 2021'de erişildi.
Kimya

Niels Bohr, Bohr atomu, atom fiziği, kararlı atom, atom modeli, gezegen sistemi, elektrosferin katmanları, enerji seviyeleri, elektron kabukları, elektron enerjisi, Rutherford atom modeli, uyarılmış durum atomu.
Kimya
Atomlar ve Evrenin inşası, atom teorisi, her şeyin yapıldığı, maddenin atomlardan oluştuğu, Dört element teorisi, eski simyacılar, atom teorisi, temel parçacık.
