Kemisk balans är ett av de ämnen som faller mest i Enem och antagningsprov.
Aspekter av reversibla reaktioner behandlas i frågorna och kandidaterna utvärderas både genom beräkningar och genom de begrepp som involverar detta tema.
Med detta i åtanke gjorde vi denna lista med frågor med olika metoder för kemisk balans.
Utnyttja upplösningskommentarerna för att förbereda dig för tentorna och kolla steg-för-steg-instruktionerna om hur du löser frågorna.
Allmänna begrepp för kemisk jämvikt
1. (Uema) I ekvationen , efter att ha uppnått kemisk jämvikt, kan vi avsluta jämviktskonstanten
, om vilket det är korrekt att ange att:
a) ju högre värdet på Kc, desto lägre är utbytet av den direkta reaktionen.
b) Kç oavsett temperatur.
c) om hastigheterna för framåt- och inversreaktionerna är lika, är Kc = 0.
d) Kç det beror på de initiala molariteterna för reaktanterna.
e) ju större Kc-värdet är, desto större är koncentrationen av produkterna.
Rätt svar: e) Ju större värde Kc har, desto större är koncentrationen av produkterna.
Den direkta reaktionen representeras av siffran 1, där:
Den omvända reaktionen representeras av
Värdet av Kç den beräknas med förhållandet mellan koncentrationerna av produkter och reagens.
Täljaren (som innehåller produkterna) är direkt proportionell mot jämviktskonstanten. Därför desto högre är värdet på Kçju större utbyte av direktreaktionen, eftersom mer produkt bildas och följaktligen desto större koncentration av produkter.
Värdet av Kç varierar med temperaturen, för när vi ändrar dess värde kan den endotermiska (värmeabsorptions) eller exoterma (värmeavgivande) reaktionen vara och därmed kan mer reagens eller produkt konsumeras eller skapas, vilket ändrar jämviktskonstanten som beror på koncentrationen av reagens.
Kc beror på de molära mängderna av komponenterna när jämvikt upprättas och när hastigheterna för framåt- och bakåtreaktionerna är lika.
2. (UFRN) Den kemiska balansen kännetecknas av att vara dynamisk på mikroskopisk nivå. För att få kvantitativ information om omfattningen av kemisk jämvikt används jämviktskonstantmängden. Tänk på följande remsa:

Tillämpad på kemisk balans, karaktärens idé om balans:
a) Det är korrekt eftersom halva mängderna i kemisk jämvikt alltid är produkter och den andra hälften är reaktanter.
b) Det är inte korrekt, eftersom koncentrationerna av produkter och koncentrationer av reaktanter i kemisk jämvikt kan vara olika, men de är konstanta.
c) Det är korrekt eftersom, i kemisk jämvikt, är koncentrationerna av reaktanter och produkter alltid desamma, så länge jämvikt inte störs av en extern effekt.
d) Det är inte korrekt, eftersom koncentrationerna av produkterna i kemisk jämvikt alltid är högre än för reaktanterna, så länge jämvikt inte påverkas av en extern faktor.
e) Det är korrekt eftersom koncentrationerna av reaktanter och produkter i kemisk jämvikt inte alltid är desamma.
Rätt svar: b) Det är inte korrekt eftersom koncentrationerna av produkter och koncentrationer av reaktanter i kemisk jämvikt kan vara olika, men de är konstanta.
Vid jämvikt kan mängderna av produkter och reagens beräknas baserat på konstanten av balans och inte nödvändigtvis bör vara hälften av mängden produkter och den andra hälften reagens.
Jämviktskoncentrationerna är inte alltid desamma, de kan vara olika, men konstanta om inga störningar uppträder i jämvikten.
Jämviktskoncentrationerna bör bero på vilken reaktion som favoriseras, vare sig direkt eller invers. Vi kan veta detta med värdet på Kç: om Kç 1, direkt reaktion är favoriserad. redan om Kç
1 omvänd reaktion är favoriserad.
Kemiska balansdiagram
3. (UFPE) I början av 1900-talet skapade förväntningarna på första världskriget ett stort behov av kväveföreningar. Haber var banbrytande i produktionen av ammoniak från kväve i luften. Om ammoniak placeras i en sluten behållare, sönderdelas den enligt följande obalanserade kemiska ekvation: NH3(g) → N2 (g) + H2 (g). Variationerna i koncentrationer över tiden illustreras i följande figur:

Från analysen av figuren ovan kan vi konstatera att kurvorna A, B och C representerar den temporala variationen av koncentrationerna av följande reaktionskomponenter, respektive:
ah2, Nej2 och NH3
b) NH3, H2 och nej2
c) NH3, Nej2 och H2
d) Nej2, H2 och NH3
e) H2, NH3 och nej2
Rätt svar: d) N2, H2 och NH3.
1: a steget: balansera den kemiska ekvationen.
2 NH3(g) → N2 (g) + 3 H2 (g)
Med den balanserade reaktionen insåg vi att det tar 2 mol ammoniak att sönderdelas i kväve och väte. Mängden väte som produceras i reaktionen är också tre gånger större än den för ammoniak.
Andra steget: tolka diagramdata.
Om ammoniak sönderdelas är koncentrationen i diagrammet maximal och minskar, vilket ses i kurva C.
Produkterna, när de bildas, i början av reaktionen är koncentrationerna noll och ökar när reaktanten blir en produkt.
Eftersom mängden väte som produceras är tre gånger större än kväve, är kurvan för denna gas den största, som noterats i B.
Den andra produkten som bildas är kväve, vilket framgår av kurva A.
4. (Cesgranrio) Systemet som representeras av ekvationen var i balans. Jämviktstillståndet förändrades plötsligt genom tillsats av ämne G. Systemet reagerar för att återställa balansen. Vilket av följande diagram representerar bäst de förändringar som inträffade under den beskrivna processen?
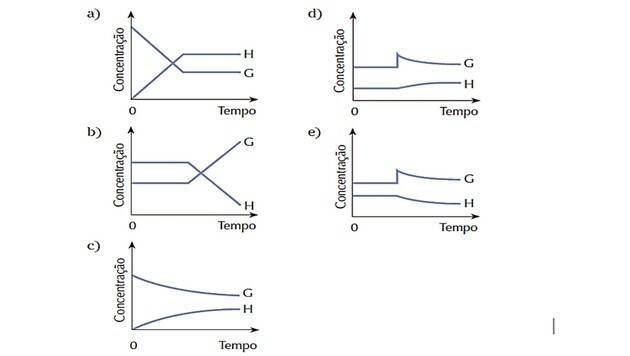
Rätt svar: d).

Eftersom systemet var i jämvikt i början förblev mängden ämnen G och H konstanta.
Störningen inträffade när koncentrationen av G ökade och systemet reagerade genom att transformera detta reaktant i mer produkt H, förskjuter balansen åt höger, det vill säga gynnar reaktionen direkt.
Vi observerar att reagenskurvan G minskar när den konsumeras och produktkurvan H ökar när den bildas.
När en ny jämvikt upprättas blir kvantiteterna konstanta igen.
Jämviktskonstant: förhållande mellan koncentration och tryck
5. (UFRN) Att veta att KP = Kç (RT)n, vi kan säga att KP = Kç, för:
stål2(g) + H2 (g) ↔ CO(g) + H2O(g)
b) H2 (g) + ½2 (g) ↔ H2O(1)
c) Nej2 (g) + 3 H2 (g) NH 2 NH3(g)
d) NEJ(g) + ½ O2(g) ↔ NEJ2(g)
e) 4 FeS(s) + 7 O2 (g) Fe 2 Fe2O3 (s) + 4 SO2(g)
Rätt svar: a) CO2(g) + H2 (g) ↔ CO(g) + H2O(g)
Till KP vara lika med Kç variationen i antalet mol måste vara lika med noll, eftersom varje tal som höjs till noll resulterar i 1:
KP = Kç (RT)0
KP = Kç x 1
KP = Kç
Förändringen i antalet mol beräknas av:
∆n = Antal mol produkter - Antal mol reagens
I denna beräkning deltar endast koefficienterna för ämnen i gasform.
Tillämpning på varje alternativ ekvation har vi:
| stål2(g) + H2 (g) ↔ CO(g) + H2O(g) | ∆n = [(1 + 1) - (1 + 1)] = 2 - 2 = 0 |
| b) H2 (g) + ½2 (g) ↔ H2O(1) | ∆n = [0 - (1 + 1/2)] = 0 - 3/2 = - 3/2 |
| c) Nej2 (g) + 3 H2 (g) NH 2 NH3 (g) | ∆n = [2 - (1 + 3)] = 2-4 = - 2 |
| d) NEJ(g) + ½2 (g) ↔ NEJ2 (g) | ∆n = [1 - (1 + 1/2)] = 1-3/2 = - 1/2 |
| e) 4 FeS(s) + 7 O2 (g) Fe 2 Fe2O3 (s) + 4 SO2 (g) | ∆n = [(0 + 4) - (0 + 7)] = 4-7 = - 3 |
Med dessa resultat kan vi observera att alternativet vars värde motsvarar det erforderliga resultatet är det i den första ekvationen.
6. (UEL-anpassad) För reaktionen som representeras av jämviktskonstanterna Kç och KP uttrycks av ekvationerna: (givet: p = partiellt tryck)
Rätt alternativ:
Jämviktskonstanten beräknas av:
Fasta föreningar, på grund av deras konstanta koncentrationer, deltar inte i beräkningen av Kçdärför är jämviktskonstanten för den givna ekvationen:
För jämviktskonstanten, i termer av tryck, deltar bara gaserna i beräkningen, så:
Beräkning av jämviktskonstanten
7. (Enem / 2015) Flera syror används i industrier som kasserar deras avlopp i vattendrag, såsom floder och sjöar, vilket kan påverka miljöbalansen. För att neutralisera surheten kan kalciumkarbonatsalt tillsättas utflödet, i lämpliga mängder, eftersom det producerar bikarbonat, vilket neutraliserar vattnet. De ekvationer som är involverade i processen presenteras:
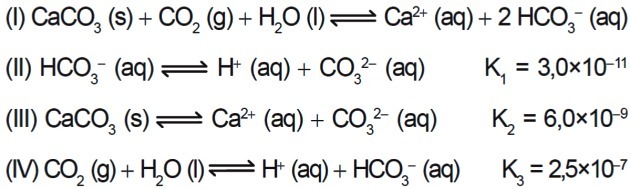
Baserat på värdena för jämviktskonstanterna för reaktionerna II, III och IV vid 25 ° C, vad är det numeriska värdet för jämviktskonstanten för reaktion I?
a) 4,5 x 10-26
b) 5,0 x 10-5
c) 0,8 x 10-9
d) 0,2 x 105
e) 2,2 x 1026
Rätt svar: b) 5,0 x 10-5
Första steget: använd Hess lag för att göra nödvändiga justeringar.
Givet en kemisk ekvation:
Konstanten beräknas av:
Men om vi vänder ekvationen får vi som ett resultat:
Och konstanten blir det omvända:
För att komma till ekvation 1, som ges i frågan, måste vi invertera ekvation II, som i föregående exempel.
2: a steget: Manipulera ekvationerna II, III och IV för att nå resultatet av ekvation I.
3: e steget: beräkna jämviktskonstanten för ekvation I.
Beräkning av KJag görs genom att multiplicera de konstanta värdena.
Som i beräkningen har vi lika baskrafter, vi upprepar basen och lägger till exponenterna.
Eftersom vi nu har en uppdelning med lika baskrafter upprepar vi basen och subtraherar exponenterna.
8. (UnB) Fosforpentaklorid är ett mycket viktigt reagens inom organisk kemi. Det bereds i gasfasen genom reaktionen:
En flaska med kapacitet på 3,00 liter innehåller vid jämvikt, vid 200 ° C: 0,120 mol PCl5(g)0,600 mol PCl3(g) och 0,0120 mol CL2(g). Vad är värdet på jämviktskonstanten vid denna temperatur?
Rätt svar: 50 (mol / L)-1
1: a steget: Montera uttrycket av jämviktskonstanten för reaktionen.
2: a steget: beräkna koncentrationerna i mol / L för varje komponent vid jämvikt.
Molekoncentrationsformel:
| PCl3 | Cl2 | PCl5 |
Tredje steget: ersätt koncentrationerna i det konstanta uttrycket och beräkna värdet på Kç.
Ansökningar om jämvikt
9. (Enem / 2016) Efter fullständigt slitage kan däcken brännas för att generera energi. Bland de gaser som genereras vid fullständig förbränning av vulkaniserat gummi är vissa föroreningar och orsakar surt regn. För att förhindra att de flyr ut i atmosfären kan dessa gaser bubblas in i en vattenlösning innehållande en lämplig substans. Tänk på ämneinformationen i tabellen.
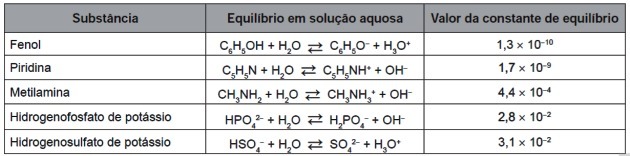
Bland de ämnen som anges i tabellen är den som effektivt kan avlägsna förorenande gaser (a)
a) Fenol.
b) Pyridin.
c) Metylamin.
d) Kaliumvätefosfat.
e) Kaliumvätesulfat.
Rätt svar: d) Kaliumvätefosfat.
kompaniet2, svaveloxider (SO2 och så3) och kväveoxider (NO och NO2) är de viktigaste förorenande gaserna.
När de reagerar med vatten i atmosfären finns det en syrabildning som orsakar en ökning av surheten i regnet, varför det kallas surt regn.
Jämviktskonstanterna i tabellen beräknas av förhållandet mellan koncentrationerna av produkter och reagens enligt följande:
Observera att jämviktskonstanten är proportionell mot koncentrationen av produkter: ju större kvantitet produkter, desto större är värdet av Kç.
Notera värdena för den första och sista kompositen i tabellen för Kç:
| pyridin | ||
| Kaliumvätesulfat |
Jämförelse av de två siffrorna ser vi att ju mindre negativ effekt, desto större är konstantens värde.
För att avlägsna föroreningar mer effektivt, OH- att reagera med H-joner+ närvarande i syror genom a neutraliseringsreaktion.
Bland de ämnen som presenteras är de som producerar hydroxylerna som behövs för att neutralisera sura föreningar: pyridin, metylamin och kaliumvätefosfat.
För att ta reda på vilken förening som är mest effektiv observerar vi jämviktskonstanterna: ju högre det konstanta värdet, desto större är koncentrationen av OH-.
Sålunda är den vattenhaltiga lösningen som innehåller ett ämne som är lämpligt för detta ändamål kaliumvätefosfat, eftersom det är mer basiskt och neutraliserar syror mer effektivt.
För att lära dig mer, läs dessa texter.:
- jonisk balans
- Neutraliseringsreaktion
10. (Enem / 2009) Tvål är salter av långkedjiga karboxylsyror som används för att underlätta, under tvättprocesser, avlägsnande av ämnen med låg vattenlöslighet, t.ex. oljor och fett. Följande figur representerar strukturen hos en tvålmolekyl.
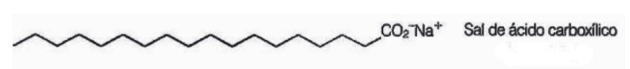
I lösning kan tvålanjoner hydrolysera vatten och därigenom bilda motsvarande karboxylsyra. Till exempel för natriumstearat upprättas följande balans:
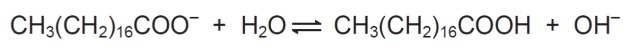
Eftersom den bildade karboxylsyran är dåligt löslig i vatten och mindre effektiv vid avlägsnande av fett, mediumets pH måste kontrolleras på ett sådant sätt att balansen ovanför inte flyttas åt höger.
Baserat på informationen i texten är det korrekt att dra slutsatsen att tvålar fungerar på ett sätt:
a) Mer effektivt vid grundläggande pH.
b) Mer effektivt vid surt pH.
c) Mer effektivt vid neutralt pH.
d) Effektiv över alla pH-intervall.
e) Mer effektivt vid surt eller neutralt pH.
Svar: a) Mer effektivt vid grundläggande pH.
I den visade balansen ser vi att natriumstearat vid reaktion med vatten bildar en karboxylsyra och hydroxyl.
Syftet med att kontrollera pH är inte att tillåta bildning av karboxylsyra, och detta görs genom att flytta balansen genom att ändra OH-koncentrationen-.
ju mer OH- i lösning finns det en störning på produktsidan och det kemiska systemet reagerar genom att konsumera ämnet som hade koncentrationen ökat, i detta fall hydroxyl.
Följaktligen kommer det att omvandlas av produkter till reagens.
Därför fungerar tvålar mest effektivt vid basalt pH eftersom överskott av hydroxyl flyttar balansen åt vänster.
Om pH var surt skulle det finnas en högre koncentration av H+ som skulle påverka balansen genom att konsumera OH- och balansen skulle verka genom att producera mer hydroxyl, flytta balansen åt vänster och producera mer karboxylsyra, vilket inte är av intresse i den presenterade processen.
Kemisk jämviktsförskjutning
11. (Enem / 2011) Läskedrycker har alltmer blivit mål för folkhälsopolitiken. Limprodukter innehåller fosforsyra, ett ämne som är skadligt för fixering av kalcium, det mineral som är huvudkomponenten i tandmatrisen. Karies är en dynamisk process av obalans i processen för tandmineralisering, förlust av mineraler på grund av surhet. Det är känt att huvudkomponenten i tandemaljen är ett salt som kallas hydroxiapatit. Läsket, på grund av närvaron av sackaros, sänker biofilmens (bakteriell plack) pH, vilket orsakar demineralisering av tandemaljen. Spyttförsvarsmekanismer tar 20 till 30 minuter att normalisera pH-nivån och remineralisera tanden. Följande kemiska ekvation representerar denna process:
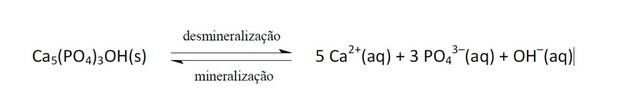 GROISMAN, S. Effekten av läsk på tänderna bedöms utan att det tas ur kosten. Tillgänglig i: http://www.isaude.net. Åtkomst: 1 maj 2010 (anpassad).
GROISMAN, S. Effekten av läsk på tänderna bedöms utan att det tas ur kosten. Tillgänglig i: http://www.isaude.net. Åtkomst: 1 maj 2010 (anpassad).
Med tanke på att en person konsumerar läskedrycker dagligen kan en process av tandmineralisering uppstå på grund av den ökade koncentrationen av
a) OH–, som reagerar med Ca-joner2+, flyttar balansen åt höger.
b) H+, som reagerar med OH-hydroxylerna–, flyttar balansen åt höger.
c) OH–, som reagerar med Ca-joner2+, flyttar balansen åt vänster.
d) H+, som reagerar med OH-hydroxylerna–, flyttar balansen åt vänster.
e) Ca2+, som reagerar med OH-hydroxylerna–, flyttar balansen åt vänster.
Rätt svar: b) H+, som reagerar med OH-hydroxylerna–, flyttar balansen åt höger.
När pH sjunker beror det på att surheten har ökat, det vill säga koncentrationen av H-joner+, som uttalandet säger, finns det fosforsyra.
Dessa joner reagerar med OH- orsakar att detta ämne konsumeras och följaktligen flyttar balansen åt höger, eftersom systemet agerar genom att producera fler av dessa avlägsnade joner.
Jämviktsförskjutningen mellan reaktanter och produkter inträffade på grund av minskningen av OH-koncentrationen-.
Om Ca-jonerna2+ och åh- hade koncentrationen ökat, skulle det flytta balansen åt vänster, eftersom systemet skulle reagera genom att konsumera dem och bilda mer hydroxiapatit.
Att ändra den tidigare balansen, relaterad till köldmedieläckage under de beskrivna förhållandena, resulterar i:
a) CO-frisättning2 för miljön.
b) Höj temperaturen på behållaren.
c) Höjning av behållarens inre tryck.
d) Höjning av CO-koncentrationen2 i vätskan.
e) Bildande av en betydande mängd H2O.
Rätt svar: a) CO-utsläpp2 för miljön.
Inne i flaskan löstes koldioxiden i vätskan på grund av högt tryck.
När flaskan öppnas är trycket inuti behållaren (vilket var större) lika med trycket i miljön och därmed finns det en flykt från koldioxid.
Jämviktsförskjutningen mellan reaktanter och produkter inträffade på grund av tryckfallet: när trycket minskar, flyttas jämvikten till den största volymen (antal mol).
Reaktionen skiftade åt vänster och CO2 som löstes i vätskan släpptes, läckte ut när flaskan öppnades.