För klassificera en sigma-länk, det är viktigt att veta hur man känner igen det i en molekyls struktur. Sigma-bindningen är faktiskt en kovalent bindning som uppstår när två ofullständiga atomorbitaler (med endast en elektron) interpenetrera på samma axel. Ett exempel är när en p-typ (helix) orbital interpenetrerar med en annan p-orbital.

p-orbitaler som tränger in i en p-sigma-bindning
I praktiken (i övningar), erkännandet och klassificeringen av en sigma-länk görs från strukturformeln av ett ämne, som i den strukturella representationen nedan:

Strukturformel av hydrocyansyra
Innan du klassificerar en sigma-länk, det är nödvändigt att veta hur man känner igen det i en strukturformel. För detta, kom bara ihåg sätt som en kovalent bindning är representerad: samtalet enkel representeras av ett enda streck (-), den par representeras av två (=) och länken trippel- representeras av tre (≡). Sigma-bindningen är närvarande i någon av de tre representationerna av kovalenta bindningar enligt följande:
Enkel: har ett sigma-band;
Par: Av de två länkarna är bara en sigma;
Trippel: En av de tre länkarna är sigma.
Att veta hur man känner igen en sigma-länk, nästa steg är att lära sig att rangordna den. För detta måste vi veta vad som är den ofullständiga banan för varje atom som är involverad i bindningen:
H - presenterar den ofullständiga orbitalen, så i klassificeringen representeras den av s.
Ametaler- har en ofullständig p-orbital, så i klassificeringen representeras de av p, med undantag för följande element:
Kol: Din ofullständiga omlopp beror på typen av hybridisering att han lider. Möjligheterna är: sp hybridisering3 (hur mycket gör det fyra enkla samtal), sp2 (hur mycket gör det två enkla och en dubbelbindningar) eller sp (hur mycket det genomför två dubbelbindningar eller en enkel och en trippel). I klassificeringen av en sigma-bindning kan kol således representeras av sp3, sp2 eller sp beroende på samtalet du ringer.
Beryllium:lida sp-typ hybridisering, således, i klassificeringen, representeras av sp.
Bor:lida sp-typ hybridisering2, således, i klassificeringen representeras den av sp.2.
Med all denna information är det enklaste att klassificera sigma-länkarna i en struktur. Låt oss se några exempel:
Exempel 1: sigma-anslutningar i vatten

Strukturell formel för vatten
Sluta inte nu... Det finns mer efter reklam;)
Ovanstående strukturformel visar att vatten har två sigma-obligationer (två enkla), var de mellan syret (representerad av s) det är Väte (representerad av s). Således har vi två sigma-länkar klassificerade i:
s-p
Exempel 2: Sigma binder i fosfortriklorid

Strukturformel av fosfortriklorid
Ovanstående strukturformel visar att fosfortriklorid har tre samtalsigmas (tre enkla), var de in i fosfor (representerad av s) det är klor (representerad av s). Således har vi tre sigma-länkar klassificerade i:
p-p
Exempel 3: sigma-bindningar i bortrifluorid
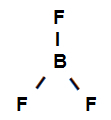
Strukturformel för bortrifluorid
Ovanstående strukturformel visar att bortrifluorid har tre sigma-länkar (tre enkla), var de in i boret (representerad av sp2) det är Fluor (representerad av s). Således har vi tre sigma-länkar klassificerade i:
p-sp2
Exempel 4: sigma-bindningar i etanol
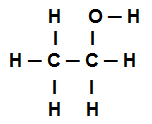
Etanol strukturformel
Den strukturella formeln för etanol ovan visar att vi har närvaron av åtta samtal sigmas (åtta enkla länkar). Är de:
En bland syre (representerad av p) och väte (representerad av s). Således klassificeras länken i sigma s-p.
En av två kol som endast utför sigma-anslutningar (och sedan representerad av sp3). Således klassificeras länken i sp3-P3.
En bland kolet (representerad av sp3) och syret (representerad av s). Således klassificeras sigma-länken i p-sp3.
fem mellan kol (representerad av sp3) och väte (representerad av s). Således klassificeras alla fem i s-sp3.
Exempel 5: Sigma binder i dikloreten

Dikloroeten strukturformel
Strukturformeln för dikloreten ovan visar att vi har närvaron av fem sigma-länkar (de fyra enkelbindningarna och en av dubbelbindningarna). Är de:
En av två kol som utför två enkla och en dubbelbindningar (och sedan representerad av sp2). Således klassificeras sigma-länken i sp2-P2.
Fyra är mellan kol(representerad av sp2)och väte (representerad av s). Således klassificeras alla fyra i s-sp2.
Av mig Diogo Lopes Dias
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
DAGAR, Diogo Lopes. "Klassificering av en sigma-länk"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/quimica/classificacao-uma-ligacao-sigma.htm. Åtkomst den 28 juni 2021.



