Капацитет који везе имају да привуку електричне набоје дефинисан је као поларитет, који поприма другачији карактер у зависности од везе на којој је присутан.
Најчешће везе које укључују органска једињења настају између атома угљеника или између атома угљеника и водоника: Ц ─ Ц и Ц ─ Х (угљоводоници). Ову врсту везе класификујемо као ковалентну, присутна је у свим везама органских једињења насталих само угљеником и водоником.
Када у молекулу органског једињења постоји још један хемијски елемент осим угљеника и водоника, његови молекули ће имати одређени поларитет. Овај елемент називамо хетероатомом, а то могу бити: азот (Н), кисеоник (О), између осталог.
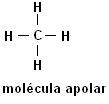
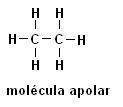
Метан (ЦХ4) Етан (Ц.2Х.6)
Имајте на уму да у обе структуре нема хетероатома, у овом случају су молекули класификовани као неполарни.


Присуство кисеоника као хетероатома чини да молекули показују поларитет. Први молекул је једињење етанол (ЦХ3ЦХ2ох), присуство хидроксил - ОХ даје овом једињењу поларни карактер, чак и ако у својој структури садржи неполарни део.
Написала Лириа Алвес
Дипломирао хемију
Бразилски школски тим
Види више! равни изомер
Органска хемија - Хемија - Бразил Сцхоол
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/moleculas-organicas-polares-apolares.htm

