У наставку размотрите генеричку реверзибилну реакцију, при чему мала слова одговарају уравнотеженим коефицијентима реакције, а велика слова су реактанти, а сви производи су гасовити:

Узимајући у обзир сваки од смерова реакције одвојено, њихове стопе развоја (Тд) дате су:
* Директна реакција: аА + бБ → цЦ + дД
Сведиректан = Кдиректан. [ТХЕ]Тхе. [Б]Б.
* Обрнута реакција: цЦ + дД → аА + бБ
Свеинверзна = Кобрнуто. [Ц]ц. [Д]д
Константа хемијске равнотеже у погледу концентрације у количини материје (Кц) и у погледу парцијалног притиска (КП.) биће дато дељењем К.директан од К.обрнуто.
Тако имамо:
К.директан. [ТХЕ]Тхе. [Б]Б. = 1 → К.директан__ = __[Ц]ц. [Д]д___
К.обрнуто. [Ц]ц. [Д]д К.обрнуто [ТХЕ]Тхе. [Б]Б.
Бити, К.ц =_Кдиректан_
К.обрнуто
Тако имамо:
К.ц =__[Ц]ц. [Д]д___ или К.П. =__(Праца)ц. (пД)д___ |
Где је п парцијални притисак сваке супстанце у равнотежи.
На тај начин се свака концентрација подиже на експонент који одговара коефицијенту односне супстанце у реакцији и Кц нема јединицу *.
Поред тога, веома важан аспект који треба истаћи је онај у овом изразуне смеју бити заступљене ни чврсте компоненте ни чисте течности., јер у овом изразу учествују само ствари које могу претрпети варијације. Концентрација у количини материје супстанце у чврстом стању је константна и самим тим је већ укључена у вредност самог К.ц. Исто важи и за чисте течности попут воде. Укратко, у експресији учествују само супстанце у гасовитом стању и у воденом раствору.
Обратите пажњу на доленаведене примере:
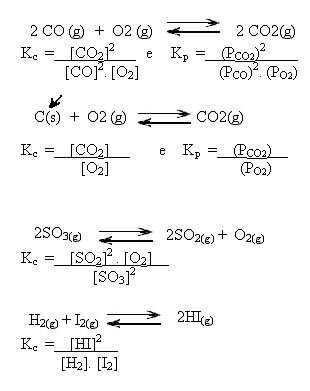
К вредностиц може нам показати да ли су концентрације реактаната и производа једнаке или је један већи од другог:
- ако К.ц или К.П. једнак је јединици (Кц = 1), то значи да је концентрација реагенса и производа једнака;
- Ако је вредност од К.ц или К.П. бити висок, то значи да су производи у већој концентрацији, јер у изразу Кц производи су у нумератору;
- Ако је вредност од К.ц или К.П. ниска, то значи да су реагенси у већој концентрацији, јер у изразу Кц реагенси су у имениоцу.
* К.ц и К.П. то су бездимензионални бројеви, односно чисти бројеви, без јединице која је повезана са било којом величином или односом између величина.
Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm


