ТХЕ заједничка концентрација, такође названа концентрација у г/Л, је однос између масе растворене супстанце у запремини раствора.
Математички, заједничка концентрација се изражава кроз формулу:
Ц = м/в
Где,
Ц: уобичајена концентрација;
м: маса растворене супстанце;
В: запремина раствора.
Најчешће коришћена јединица за уобичајену концентрацију је г/Л, пошто се маса растворене супстанце израчунава у грамима (г), а запремина раствора у литрима (Л).
На пример, морска вода има велику количину растворених соли, а натријум хлорид (НаЦл), популарно познат као кухињска со, је један од њих.
Концентрација натријум хлорида у морској води је у просеку 2,5 г/Л. Дакле, има 2,5 грама соли, што је раствор, у сваком 1 литру морске воде, што је раствор.
Како израчунати уобичајену концентрацију?
Раствор је хомогена смеша коју формира супстанца у мањој количини, која се назива растворена материја, растворена у растварачу, који је у већој количини.
Дакле, уобичајена концентрација се односи на количину растворене супстанце у датој запремини раствора. Што је више растворене супстанце растворено у раствору, то је више концентрисано. У супротном, то јест, мало растворене материје указује на то да је раствор разблажен.
Пример 1: Колика је концентрација у г/Л раствора сребрног јодида (АгИ) који садржи 2,6 г у 1Л раствора?
Када добијемо количину растворене супстанце и запремину раствора, једноставно убацимо вредности у заједничку формулу концентрације да бисмо пронашли њену вредност.
Дакле, у раствору сребрног јодида од 2,6 г/Л има 2,6 г растворене супстанце у сваком 1 литру раствора.
Пример 2: Приликом испаравања растварача из 500 мЛ физиолошког раствора концентрације 6 г/Л, колика је маса растворене супстанце која се добија?
Имајте на уму да у неким прорачунима можемо пронаћи описану уобичајену концентрацију тако да можемо израчунати масу растворене супстанце.
Такође је потребно обратити пажњу на јединице. Пошто је уобичајена концентрација дата у г/Л, у овом случају морамо да претворимо јединицу запремине пре него што применимо формулу.
Како 1 Л садржи 1000 мЛ, тако 500 мЛ одговара 0,5 Л.
Тако се при испаравању растварача из раствора са концентрацијом од 6 г/Л добија 12 г растворене супстанце.
Стекните више знања уз садржај:
- Концентрација раствора
- моларна концентрација
- Разблаживање раствора
Решене уобичајене вежбе концентрације
Користите следећа питања да проверите претходно стечено знање.
Питање 1
(Уницамп) Растварач је потпуно упарен из 250 мЛ воденог раствора МгЦл2 концентрације 8,0 г/Л. Колико грама растворене супстанце се добија?
а) 8.0
б) 6.0
ц) 4.0
д) 2.0
е) 1.0
Тачна алтернатива: д) 2.0.
питање 2
Погледајте слику испод.
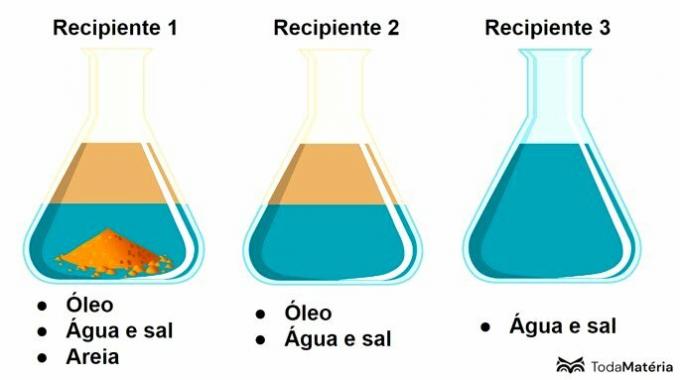
У овој шеми, контејнер 3 садржи а
а) хетерогена смеша
б) чиста супстанца
ц) Решење
г) колоидна смеша
Тачна алтернатива: ц) Решење.
Контејнер 3 садржи раствор, који је хомогена смеша формирана од растворене супстанце и растварача, где је со растворена супстанца, а вода растварач.
Генерално, можемо рећи да је растворена супстанца компонента у најмањој количини, а растварач је присутан у највећој количини.
Контејнер 1 представља хетерогену смешу са 3 фазе, а контејнер 2 одговара хетерогену смешу 2 фазе.
питање 3
Раствор је припремљен растварањем 4,0 г магнезијум хлорида МгЦл2 до постизања концентрације од 2,0 г/Л. Која запремина раствора је припремљена?
а) 1 л
б) 2 л
в) 4 л
г) 6 Л
Тачна алтернатива: б) 2 Л.
Погледајте више проблема са коментарисаним решењем на уобичајене вежбе концентрације.
Библиографске референце
ФОНСЕКА, М. Р. М. Хемија, 1. 1. ед. Сао Пауло: Атика, 2013.
САНТОС, В.Л.П; МОЛ, Г.С. Грађанска хемија, 1. 2. ед. Сао Пауло: Едитора АЈС, 2013.
УСБЕРЦО, Ј. Повежи хемију, 1. 2. ед. Сао Пауло: Сараива, 2014.
- Вежбе о заједничкој концентрацији са коментарисаним повратним информацијама
- хемијски раствори
- Раствор и растварач: шта су, разлике и примери
- Концентрација раствора
- Растворљивост
- Моларност или моларна концентрација: шта је то, формула и како израчунати
- Разблаживање раствора
- Вежбе о својствима материје